1.制取氯乙烷(CH3-CH2Cl)的最好方法是( )
| A. | 乙烷与氯气发生取代反应 | B. | 乙烯与氯气发生加成反应 | ||
| C. | 乙烯与氯化氢发生加成反应 | D. | 甲烷与氯气发生取代反应 |
18.某有机物的结构简式为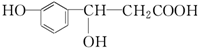 ,它可以发生反应的类型有( )
,它可以发生反应的类型有( )
①加成反应 ②消去反应 ③水解反应 ④酯化反应 ⑤氧化反应 ⑥加聚反应.
 ,它可以发生反应的类型有( )
,它可以发生反应的类型有( )①加成反应 ②消去反应 ③水解反应 ④酯化反应 ⑤氧化反应 ⑥加聚反应.
| A. | ①②③④ | B. | ①②④⑤ | C. | ①②⑤⑥ | D. | ③④⑤⑥ |
17.有机化合物种类繁多的主要原因是( )
| A. | 有机化合物主要来自自然界众多的有机体 | |
| B. | 可以人工合成 | |
| C. | 有机物分子中的碳原子成键方式具有多样性 | |
| D. | 可以由无机物进行转化 |
16.下列有机物或有机物组合,在一定条件下不能发生聚合反应的是( )
| A. | 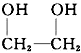 和HOOC-COOH 和HOOC-COOH | B. | HC≡CH | C. | 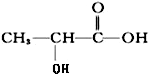 | D. | CH3COOH和C2H5OH |
15.下列关于物质鉴别的方法中不正确的是( )
| A. | 可用酸性高锰酸钾溶液鉴别甲烷和乙烯气体 | |
| B. | 可用淀粉溶液鉴别KI和KBr溶液 | |
| C. | 可用澄清石灰水检验H2和CH4的燃烧产物 | |
| D. | 可用溴水鉴别苯和四氯化碳 |
14.可逆反应A(g)+B(s)?C(g)+D(g)在恒温恒容的密闭容器中进行,下列选项中不能说明该反应已经达到平衡状态的是( )
| A. | 消耗amolA物质的同时消耗amolC物质 | |
| B. | 混合气体的质量不再改变 | |
| C. | B物质的浓度不再改变 | |
| D. | 容器内的压强不再改变 |
13.下列有关化学用语表示正确的是( )
0 156971 156979 156985 156989 156995 156997 157001 157007 157009 157015 157021 157025 157027 157031 157037 157039 157045 157049 157051 157055 157057 157061 157063 157065 157066 157067 157069 157070 157071 157073 157075 157079 157081 157085 157087 157091 157097 157099 157105 157109 157111 157115 157121 157127 157129 157135 157139 157141 157147 157151 157157 157165 203614
| A. | Al3+的结构示意图: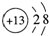 | |
| B. | 甲酸甲酯的结构简式:C2H4O2 | |
| C. | 醋酸的电离方程式:CH3COOH═CH3COO-+H+ | |
| D. | 中子数为145、质子数为94的钚(Pu)原子:${\;}_{94}^{145}$Pu |
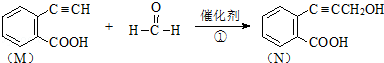
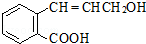 )发生缩聚反应产物的结构简式为
)发生缩聚反应产物的结构简式为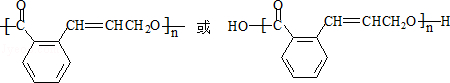 ;
; 有机物Ⅱ的结构简式为CH3C≡CCH=CHCH2CH3;A、B可以发生类似①的反应生成有机物Ⅰ,则该反应的化学方程式为CH3C≡CH+CH3CH2CHO$\stackrel{催化剂}{→}$CH3C≡CCH(OH)CH2CH2CH3.
有机物Ⅱ的结构简式为CH3C≡CCH=CHCH2CH3;A、B可以发生类似①的反应生成有机物Ⅰ,则该反应的化学方程式为CH3C≡CH+CH3CH2CHO$\stackrel{催化剂}{→}$CH3C≡CCH(OH)CH2CH2CH3. .
. +O2$→_{△}^{Cu}$
+O2$→_{△}^{Cu}$ +2H2O.
+2H2O. +2nNaOH$→_{△}^{Cu}$n
+2nNaOH$→_{△}^{Cu}$n +n
+n .+nH2O.
.+nH2O.