1.在酸性溶液中,能大量共存的离子是( )
| A. | Mg2+、Fe3+、NO3-、SCN- | B. | Al3+、Fe2+、Cl-、SO42- | ||
| C. | K+、Na+、Cl-、AlO2- | D. | Na+、Ca2+、NO3-、SO42- |
20.下列事实中,不能说明氯的非金属性比硫强的是( )
| A. | 高氯酸(HClO4)的酸性比硫酸强 | B. | 次氯酸的氧化性比稀硫酸强 | ||
| C. | 氯化氢比硫化氢的热稳定性好 | D. | 硫离子还原性比氯离子还原性强 |
19.下列关于铝的叙述中,不正确的是( )
| A. | 铝是地壳里含量最多的金属元素 | B. | 铝容易失去电子,表现还原性 | ||
| C. | 在常温下,铝不能与氧气反应 | D. | 在空气中用酒精灯点不着 |
16.在冰醋酸、葡萄糖、甲酸甲酯的混合物中,含碳的质量分数为( )
| A. | 30% | B. | 40% | C. | 50% | D. | 无法确定 |
15.仅用下表提供的玻璃仪器(非玻璃仪器任选)或实验装置就能达到相应实验目的是( )
| 选项 | A | B | C | D |
| 实验 目的 | 除去KCl中少量MnO2 | 用10mol•L-1盐酸配制100mL 0.1mol•L-1盐酸 | 用含有少量NH4Cl杂质的NaCl溶液制备氯化钠晶体 | 除去乙烯中少量SO2 |
| 实验仪器或装置 | 烧杯、玻璃棒、分液漏斗 | 100mL容量瓶、玻璃棒、烧杯 |  |  |
| A. | A | B. | B | C. | C | D. | D |
13.某学生对SO2与漂粉精的反应进行实验探究:
(1)写出C12和Ca(OH)2制取漂粉精的化学方程式2Cl2+2Ca(OH)2=CaCl2+Ca(ClO)2+2H2O;
(2)向水中持续通入SO2,未观察到白雾.推测现象i的白雾由HCl小液滴形成,进行如下实验:
a.用湿润的碘化钾淀粉试纸检验白雾,无变化;
b.用酸化的AgNO3溶液检验白雾,产生白色沉淀.
①实验a目的是验证Cl2是否存在;
②由实验a、b不能判断白雾中含有HC1,理由是与硝酸酸化的AgNO3产生的白色沉淀也可能是Ag2SO4或Ag2SO3;
(3)将A瓶中混合物过滤、洗涤,得到沉淀X
①向沉淀X中加入稀HC1,无明显变化.取上层清液,加入BaC12溶液,产生白色沉淀.则沉淀X中含有的物质是CaSO4
②用离子方程式解释现象iii中黄绿色褪去的原因:SO2+Cl2+2H2O=4H++SO42-+2Cl-.
(4)测定漂粉精有效成分的质量分数.称取2.000g漂粉精于锥形瓶中,加水溶解,调节溶液的pH,以淀粉为指示剂,用0.2000mol•L-1 KI溶液进行滴定,溶液出现稳定浅蓝色时为滴定终点.反应原理为:3C1O-+I-═3C1-+IO3-IO3-+5I-+3H2O═6OH-+3I2
实验测得数据如下表所示.
该漂白粉中有效成分的质量分数为7.15%.
0 156969 156977 156983 156987 156993 156995 156999 157005 157007 157013 157019 157023 157025 157029 157035 157037 157043 157047 157049 157053 157055 157059 157061 157063 157064 157065 157067 157068 157069 157071 157073 157077 157079 157083 157085 157089 157095 157097 157103 157107 157109 157113 157119 157125 157127 157133 157137 157139 157145 157149 157155 157163 203614
| 操作 | 现象 |
| 取适量漂粉精固体,加入100mL水 | 部分固体溶解,溶液略有颜色 |
| 过滤,测漂粉精溶液的pH | pH试纸先变蓝,后褪色 |
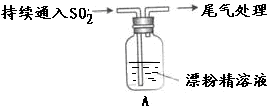 | 液面上方出现白雾; 稍后,出现浑浊,溶液变为黄绿色; 稍后,产生大量白色沉淀,黄绿色褪去 |
(2)向水中持续通入SO2,未观察到白雾.推测现象i的白雾由HCl小液滴形成,进行如下实验:
a.用湿润的碘化钾淀粉试纸检验白雾,无变化;
b.用酸化的AgNO3溶液检验白雾,产生白色沉淀.
①实验a目的是验证Cl2是否存在;
②由实验a、b不能判断白雾中含有HC1,理由是与硝酸酸化的AgNO3产生的白色沉淀也可能是Ag2SO4或Ag2SO3;
(3)将A瓶中混合物过滤、洗涤,得到沉淀X
①向沉淀X中加入稀HC1,无明显变化.取上层清液,加入BaC12溶液,产生白色沉淀.则沉淀X中含有的物质是CaSO4
②用离子方程式解释现象iii中黄绿色褪去的原因:SO2+Cl2+2H2O=4H++SO42-+2Cl-.
(4)测定漂粉精有效成分的质量分数.称取2.000g漂粉精于锥形瓶中,加水溶解,调节溶液的pH,以淀粉为指示剂,用0.2000mol•L-1 KI溶液进行滴定,溶液出现稳定浅蓝色时为滴定终点.反应原理为:3C1O-+I-═3C1-+IO3-IO3-+5I-+3H2O═6OH-+3I2
实验测得数据如下表所示.
| 滴定次数 | 1 | 2 | 3 |
| KI溶液体积/mL | 19.98 | 20.02 | 20.00 |
 下列关于晶体的说法正确的组合是( )
下列关于晶体的说法正确的组合是( ) 木糖的分子式为C5H10O5,属于多羟基醛,木糖在浓硫酸作用下生成糠醛(结构简式如图).
木糖的分子式为C5H10O5,属于多羟基醛,木糖在浓硫酸作用下生成糠醛(结构简式如图). .
.
