11.在100mL(NH4)2SO4和Al2(SO4)3的混合溶液中,加入足量的BaCl2的溶液,生成9.32g沉淀,再加入足量NaOH溶液并加热,生成NH4448mL(标准状况),则原溶液中Al3+的浓度为( )
| A. | 0.10mol/L | B. | 0.20mol/L | C. | 0.30mol/L | D. | 0.40mol/L |
10.下列物质中,含有极性键的离子化合物是( )
| A. | CaCl2 | B. | Na2O2 | C. | NaOH | D. | K2S |
9.表是元素周期表的一部分,针对表中的 种元素回答下列有关问题:
(1)在这些元素中,最活泼金属元素的原子结构示意图为 ,最高价氧化物对应的水化物中,酸性最强的是HClO4(用化学式表示).
,最高价氧化物对应的水化物中,酸性最强的是HClO4(用化学式表示).
(2)②、③、⑤、⑥、⑦形成的气态氢化物中最稳定的是HF(填化学式).
(3)④与②组成的某种化合物和①与②组成的某种化合物反应生成氧气,写出这两种化合物的电子式 ,
, .
.
(4)用电子式表示元素④与⑥构成化合物的形成过程: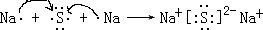 .
.
| 族 周期 | ⅠA | ⅡA | ⅢA | ⅣA | ⅤA | ⅥA | ⅦA | 0 |
| 二 | ① | ② | ③ | |||||
| 三 | ④ | ⑤ | ⑥ | ⑦ | ||||
| 四 | ⑧ |
 ,最高价氧化物对应的水化物中,酸性最强的是HClO4(用化学式表示).
,最高价氧化物对应的水化物中,酸性最强的是HClO4(用化学式表示).(2)②、③、⑤、⑥、⑦形成的气态氢化物中最稳定的是HF(填化学式).
(3)④与②组成的某种化合物和①与②组成的某种化合物反应生成氧气,写出这两种化合物的电子式
 ,
, .
.(4)用电子式表示元素④与⑥构成化合物的形成过程:
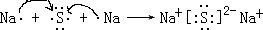 .
.
5.下列各组离子在溶液中能大量共存的是( )
| A. | NH4+ SO42- NO3- | B. | Ba2+ SO42- NO3- | ||
| C. | Na+ H+ CO32- | D. | Cu2+ OH- Cl- |
4.一丝不苟,养成良好的实验操作习惯,是确保安全与实验成功的重要前提.下列四项基本实验操作中,正确的是( )
| A. |  闻气味 | B. |  倾倒液体 | C. |  取固体药品 | D. |  稀释浓硫酸 |
3.下列关于微粒半径的叙述中,正确的是( )
| A. | 金属阳离子的半径大于它的原子半径 | |
| B. | 金属阳离子的半径小于它的原子半径 | |
| C. | 非金属阴离子的半径小于其原子半径 | |
| D. | 核外电子排布相同的不同微粒,核电荷数越大半径越小 |
2.探究Cu和浓硫酸的反应,下列装置或操作正确的是( )

0 156968 156976 156982 156986 156992 156994 156998 157004 157006 157012 157018 157022 157024 157028 157034 157036 157042 157046 157048 157052 157054 157058 157060 157062 157063 157064 157066 157067 157068 157070 157072 157076 157078 157082 157084 157088 157094 157096 157102 157106 157108 157112 157118 157124 157126 157132 157136 157138 157144 157148 157154 157162 203614

| A. | 用装置甲、乙制备和收集SO2 | |
| B. | 用装置甲、丙制备和稀释CuSO4溶液 | |
| C. | 用装置乙、丁收集和检验SO2的漂白性 | |
| D. | 用装置甲、丁制备和探究SO2的漂白性 |

 .
. +NaHCO3→
+NaHCO3→ +H2O+CO2↑.
+H2O+CO2↑.