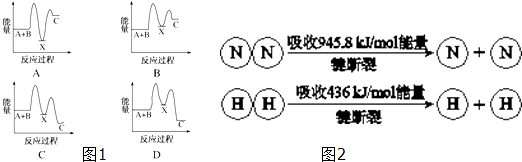
5.在一定温度下,体积不变的密闭容器中,可逆反应X(g)+3Y(g)?2Z(g)达到平衡的标志是( )
| A. | 气体总质量保持不变 | B. | 气体密度保持不变 | ||
| C. | X、Y、Z的物质的量不再发生变化 | D. | X、Y、Z的分子数之比为1:3:2 |
2.关于吸热反应和放热反应,下列说法正确的是( )
| A. | 需要加热才能进行的化学反应一定是吸热反应 | |
| B. | 放热反应不需要加热即可发生 | |
| C. | 放热反应常温下易发生 | |
| D. | 反应是放热还是吸热,要看反应物和生成物所具有的总能量的相对大小,不能看反应条件 |
1.下列分子式只能表示一种物质的是( )
| A. | C2H4 Br2 | B. | C3H8 | C. | C4H9Cl | D. | C |
20.三氯甲烷(CHCl3)又称氯仿,可用作麻醉剂,但在光照条件下易被氧化成剧毒的(COCl2).其反应式为2CHCl3+O2 $\stackrel{光}{→}$2COCl2+2HCl,为防止事故发生,在使用三氯甲烷前要检验一下其是否变质,检验用的最佳试剂是( )
| A. | NaOH溶液 | B. | 溴水 | C. | AgNO3溶液 | D. | 淀粉碘化钾溶液 |
19.标况下,11.2L乙烷和丁烷的混合气体完全燃烧需氧气47.6L,乙烷的体积分数为( )
| A. | 25% | B. | 50% | C. | 75% | D. | 80% |
18.C3H8分子中的共价键总数为( )
| A. | 10 | B. | 12 | C. | 8 | D. | 11 |
16.有四种短周期元素,它们的结构、性质等信息如下表所述:
请根据表中信息填写:
(1)A原子的核外电子排布式为1s22s22p63s1.
(2)B元素在周期表中的位置为第3周期ⅢA族;离子半径:B小于A(填“大于”或“小于”).
(3)C原子的电子排布图是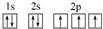 ,其原子核外有3个未成对电子,能量最高的电子为p轨道上的电子,其轨道呈哑铃形.
,其原子核外有3个未成对电子,能量最高的电子为p轨道上的电子,其轨道呈哑铃形.
(4)D原子的电子排布式为1s22s22p63s23p5或[Ne]3s23p5,D-的结构示意图是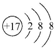 .
.
0 156956 156964 156970 156974 156980 156982 156986 156992 156994 157000 157006 157010 157012 157016 157022 157024 157030 157034 157036 157040 157042 157046 157048 157050 157051 157052 157054 157055 157056 157058 157060 157064 157066 157070 157072 157076 157082 157084 157090 157094 157096 157100 157106 157112 157114 157120 157124 157126 157132 157136 157142 157150 203614
| 元素 | 结构、性质等信息 |
| A | 是短周期中(除稀有气体外)原子半径最大的元素,该元素的某种合金是原子反应堆的导热剂 |
| B | B与A同周期,其最高价氧化物的水化物呈两性 |
| C | 元素的气态氢化物极易溶于水,可用作制冷剂 |
| D | 是海水中除氢、氧元素外含量最多的元素,其单质或化合物也是自来水生产过程中常用的消毒杀菌剂 |
(1)A原子的核外电子排布式为1s22s22p63s1.
(2)B元素在周期表中的位置为第3周期ⅢA族;离子半径:B小于A(填“大于”或“小于”).
(3)C原子的电子排布图是
 ,其原子核外有3个未成对电子,能量最高的电子为p轨道上的电子,其轨道呈哑铃形.
,其原子核外有3个未成对电子,能量最高的电子为p轨道上的电子,其轨道呈哑铃形.(4)D原子的电子排布式为1s22s22p63s23p5或[Ne]3s23p5,D-的结构示意图是
 .
. 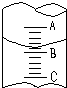 ①图表示10mL量筒中液面的位置,A与B,B与C刻度间相差1mL,如果刻度A为4,则量筒中液体的体积是①,由于放置位置不当读数时俯视,读出的数值为②则①②的正确数值为:C
①图表示10mL量筒中液面的位置,A与B,B与C刻度间相差1mL,如果刻度A为4,则量筒中液体的体积是①,由于放置位置不当读数时俯视,读出的数值为②则①②的正确数值为:C