15.下列反应中,反应物中各元素都参加氧化还原反应的是( )
| A. | 2HgO$\frac{\underline{\;\;△\;\;}}{\;}$2Hg+O2↑ | B. | CuO+H2$\frac{\underline{\;\;△\;\;}}{\;}$Cu+H2O | ||
| C. | 2H2S+SO2=3S+2H2O | D. | Cl2+2NaOH=NaCl+NaClO+H2O |
14.在水溶液中能够大量共存的离子组是( )
| A. | H+、Na+、C1-、NO3- | B. | K+、Ag+、C1-、NO3- | ||
| C. | H+、Na+、CO32-、SO42- | D. | H+、Fe2+、C1-、OH- |
13.下列离子方程式正确的是( )
| A. | 铜和硝酸银溶液反应:Cu+Ag+=Cu2++Ag | |
| B. | 铁和稀硫酸反应:2Fe+6H+=2Fe3++3H2↑ | |
| C. | 碳酸钙与稀盐酸反应:CO32-+2H+=CO2↑+H2O | |
| D. | 硫酸钠溶液和氯化钡溶液反应:Ba2++SO42-=BaSO4↓ |
12.设NA为阿伏加德罗常数的值,下列叙述正确的是( )
| A. | 标准状况下,22.4 L H2O含有分子数为NA | |
| B. | 分子总数为NA的N2气体体积约为22.4 L | |
| C. | 常温常压下,1.6 g CH4含分子数为0.1NA | |
| D. | 常温常压下,3.2g氧气所含氧原子数为0.1NA |
11.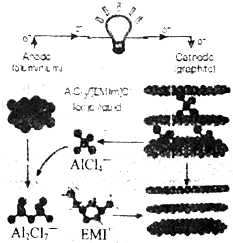 2015年4月,由中美科学家共同完成的“快速充放电铝离子电池”,具有高效耐用、可超快充电、可燃性低、成本低等特点.该电池以金属铝作为负极,三维结构的泡沫石墨材料为正极,AlCl4-可在其中或在脱嵌,由有机离子 (EMI+不参与反应)Al2Cl7-和AlCl4-组成的离子液体做电解质溶液,该电池放电时的原理如图所示,下列说法正确的是( )
2015年4月,由中美科学家共同完成的“快速充放电铝离子电池”,具有高效耐用、可超快充电、可燃性低、成本低等特点.该电池以金属铝作为负极,三维结构的泡沫石墨材料为正极,AlCl4-可在其中或在脱嵌,由有机离子 (EMI+不参与反应)Al2Cl7-和AlCl4-组成的离子液体做电解质溶液,该电池放电时的原理如图所示,下列说法正确的是( )
 2015年4月,由中美科学家共同完成的“快速充放电铝离子电池”,具有高效耐用、可超快充电、可燃性低、成本低等特点.该电池以金属铝作为负极,三维结构的泡沫石墨材料为正极,AlCl4-可在其中或在脱嵌,由有机离子 (EMI+不参与反应)Al2Cl7-和AlCl4-组成的离子液体做电解质溶液,该电池放电时的原理如图所示,下列说法正确的是( )
2015年4月,由中美科学家共同完成的“快速充放电铝离子电池”,具有高效耐用、可超快充电、可燃性低、成本低等特点.该电池以金属铝作为负极,三维结构的泡沫石墨材料为正极,AlCl4-可在其中或在脱嵌,由有机离子 (EMI+不参与反应)Al2Cl7-和AlCl4-组成的离子液体做电解质溶液,该电池放电时的原理如图所示,下列说法正确的是( )| A. | 放电时,负极的电极反应式:Al-3e-+7AlCl4-═Al2C17- | |
| B. | 充电过程中,AlCl4-脱嵌并从阴极向阳极迁移 | |
| C. | 充电过程中阳极的电极反应式为:Cn+AlCl4--e-═Cn,其中C的化合价升高 | |
| D. | 该离子液体也可用于钢制品上电镀铝,但阴极材料要换成镀件 |
10.下列各组物质中互为同分异构体的是( )
| A. | 1H与2H | B. | O2与O3 | C. | 乙烯与丙烯 | D. | 正丁烷与异丁烷 |
8.关于实验室制取乙烯的操作,下列叙述不正确的是( )
| A. | 温度计要插入反应混合液中 | |
| B. | 圆底烧瓶中要放入少量碎瓷片 | |
| C. | 圆底烧瓶中注入酒精和稀硫酸的体积为1:3 | |
| D. | 加热时使液体温度迅速升高到170℃ |
7.下列离子方程式书写不正确的是( )
| A. | Fe与稀盐酸反应:Fe+2H+═Fe3++H2↑ | |
| B. | 盐酸与NaOH溶液反应:H++OH-═H2O | |
| C. | CaCO3与稀HNO3反应:CaCO3+2H+═Ca2++CO2↑+H2O | |
| D. | BaCl2溶液与Na2SO4溶液反应:Ba2++SO42-═BaSO4↓ |
6.下列气体中能形成酸雨的是( )
0 156951 156959 156965 156969 156975 156977 156981 156987 156989 156995 157001 157005 157007 157011 157017 157019 157025 157029 157031 157035 157037 157041 157043 157045 157046 157047 157049 157050 157051 157053 157055 157059 157061 157065 157067 157071 157077 157079 157085 157089 157091 157095 157101 157107 157109 157115 157119 157121 157127 157131 157137 157145 203614
| A. | N2 | B. | CO | C. | SO2 | D. | O3 |



