5.下列叙述正确的是( )
①热稳定性:H2O>HF>H2S
②SrSO4是难溶于水的白色固体
③第ⅠA、ⅡA族元素的阳离子与同周期稀有气体元素的原子具有相同的核外电子排布
④元素周期表中从ⅢB族到ⅡB族10个纵行的元素都是金属元素
⑤因为常温下白磷可自然,而氮气须在放电时才与氧气反应,所以非金属性:P>N
⑥Li在氧气中剧烈燃烧,产物是Li2O2,其溶液是一种强碱.
①热稳定性:H2O>HF>H2S
②SrSO4是难溶于水的白色固体
③第ⅠA、ⅡA族元素的阳离子与同周期稀有气体元素的原子具有相同的核外电子排布
④元素周期表中从ⅢB族到ⅡB族10个纵行的元素都是金属元素
⑤因为常温下白磷可自然,而氮气须在放电时才与氧气反应,所以非金属性:P>N
⑥Li在氧气中剧烈燃烧,产物是Li2O2,其溶液是一种强碱.
| A. | 只有②④ | B. | 只有①⑤⑥ | C. | 只有②④⑥ | D. | 只有③⑤ |
4. 如图,p、q为直流电源两极,A由+2价金属单质X制成,B、C、D为铂电极,接通电源,金属X沉积于B极,同时C、D产生气泡.试回答:
如图,p、q为直流电源两极,A由+2价金属单质X制成,B、C、D为铂电极,接通电源,金属X沉积于B极,同时C、D产生气泡.试回答:
(1)p为正极,A极发生了氧化(填反应类型)反应.
(2)D为阴极,试管里收集到H2.
(3)C极的电极方程式是4OH--4e-=O2↑+2H2O.
(4)在电解过程中,测得C、D两极上产生的气体的实验数据如下:
仔细分析上表,请说出得到以上实验数据可能的原因是开始时阴、阳两极气体体积比为3:1,10分钟时约为2:1,说明开始时氧气溶解于溶液中.
(5)当电路中通过0.004mol电子时,B电极上沉积金属X的质量为0.128g,则此金属的摩尔质量为64g•mol-1.
(6)当反应进行一段时间后,A、B电极附近溶液的pH不变(填“增大”、“减小”或“不变”).
 如图,p、q为直流电源两极,A由+2价金属单质X制成,B、C、D为铂电极,接通电源,金属X沉积于B极,同时C、D产生气泡.试回答:
如图,p、q为直流电源两极,A由+2价金属单质X制成,B、C、D为铂电极,接通电源,金属X沉积于B极,同时C、D产生气泡.试回答:(1)p为正极,A极发生了氧化(填反应类型)反应.
(2)D为阴极,试管里收集到H2.
(3)C极的电极方程式是4OH--4e-=O2↑+2H2O.
(4)在电解过程中,测得C、D两极上产生的气体的实验数据如下:
| 时间(min) | 1 | 2 | 3 | 4 | 5 | 6 | 7 | 8 | 9 | 10 |
| 阴极生成 气体体积(cm3) | 6 | 12 | 20 | 29 | 39 | 49 | 59 | 69 | 79 | 89 |
| 阳极生成 气体体积(cm3) | 2 | 4 | 7 | 11 | 16 | 21 | 26 | 31 | 36 | 41 |
(5)当电路中通过0.004mol电子时,B电极上沉积金属X的质量为0.128g,则此金属的摩尔质量为64g•mol-1.
(6)当反应进行一段时间后,A、B电极附近溶液的pH不变(填“增大”、“减小”或“不变”).
2.下列叙述错误的是( )
| A. | 通常情况下,甲烷跟强酸、强碱、强氧化剂不反应 | |
| B. | 甲烷化学性质比较稳定,不能被任何氧化剂氧化 | |
| C. | 甲烷跟氯气反应无论生成CH3Cl、CH2Cl2、CHC13还是CCl4,都是取代反应 | |
| D. | 常温下CH3Cl为气体 |
1.对 的叙述正确的是( )
的叙述正确的是( )
 的叙述正确的是( )
的叙述正确的是( )| A. | 有两种结构 | B. | 只有一种结构 | C. | 含有非极性键 | D. | 有四种结构 |
20.下列一定是放热反应的是( )
| A. | 氧化还原反应 | B. | 离子反应 | C. | 复分解反应 | D. | 缓慢氧化 |
18.下列说法不正确的是( )
0 156946 156954 156960 156964 156970 156972 156976 156982 156984 156990 156996 157000 157002 157006 157012 157014 157020 157024 157026 157030 157032 157036 157038 157040 157041 157042 157044 157045 157046 157048 157050 157054 157056 157060 157062 157066 157072 157074 157080 157084 157086 157090 157096 157102 157104 157110 157114 157116 157122 157126 157132 157140 203614
| A. | 物质发生化学反应都伴随着能量变化 | |
| B. | 化学反应的速率和限度均可通过改变化学反应条件而改变 | |
| C. | 可逆反应只是代表少数反应 | |
| D. | 化学反应达到平衡状态时,正反应速率与逆反应速率相等 |
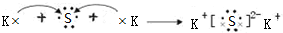 ,其化合物中化学键的类型是离子键.
,其化合物中化学键的类型是离子键.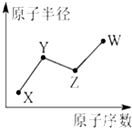 U、V、W、X、Y、Z是六种常见的短周期主族元素,其中W、X、Y、Z原子半径随
U、V、W、X、Y、Z是六种常见的短周期主族元素,其中W、X、Y、Z原子半径随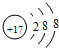 ;
;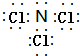 ;
;