6.如图是氯化钠晶体和二氧化碳晶体的结构示意图,关于两种晶体说法正确的是( )
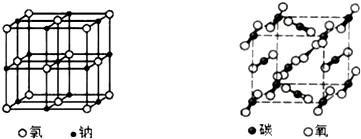

| A. | 两种晶体内均含有共价键 | B. | 构成两种晶体的微粒均是原子 | ||
| C. | 两者的硬度、熔沸点差别较大 | D. | 两种晶体均属于离子晶体 |
5.在下列反应中,HNO3既表现出氧化性,又表现出酸性的是( )
| A. | H2S+2HNO3═S↓+2NO2↑十2H2O | B. | CuO+2HNO3═Cu (NO3)2十H2O | ||
| C. | 4HNO3$\frac{\underline{\;\;△\;\;}}{\;}$4NO2↑十O2↑十2H2O | D. | 3Cu+8HNO3═3Cu (NO3) 2+2NO↑十4H2O |
4.在恒温恒容条件下,发生化学反应H2 (g)+I2(g)?2HI (g),下列选项中不能作为达到平衡状态标志的是( )
| A. | 混合气体颜色不再变化 | |
| B. | 单位时间内生成nmol氢气的同时生成nmol碘蒸气 | |
| C. | 若该反应在隔热密闭体积恒定的容器中进行反应,体系的温度不再变化 | |
| D. | 2v正(H2)=v逆(HI) |
3.R+的结构示意图为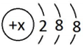 ,则R元素在元素周期表中位于( )
,则R元素在元素周期表中位于( )
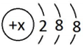 ,则R元素在元素周期表中位于( )
,则R元素在元素周期表中位于( )| A. | 第三周期0族 | B. | 第四周期IA族 | C. | 第三周期IA族 | D. | 第三周期VIIA族 |
20.现有部分短周期元素的性质或原子结构如表:
(1)元素X的一种同位素可测定文物年代,表示这种同位素原子组成的符号是614C,元素Z的离子结构示意图为 ,元素Y在周期表中的位置是第二周期VA族.
,元素Y在周期表中的位置是第二周期VA族.
(2)元素Y与氢元素形成一种离子YH4+,则检测溶液中存在该离子的方法是:向溶液(或待测液)中加入NaOH溶液后加热,能产生使湿润的红色石蕊试纸变蓝的气体,说明溶液中存在NH4+离子,反之,不存在NH4+离子.
(3)元素X与元素Y相比,非金属性较强的是N (用元素符号表示),下列表述能证明这一事实的是bc.
a.常温下X的单质和Y的单质状态不同
b.Y的最高价氧化物对应的水化物的酸性比X的最高价氧化物对应的水化物的酸性强
c.X与Y形成的化合物中X元素呈正价态.
0 156939 156947 156953 156957 156963 156965 156969 156975 156977 156983 156989 156993 156995 156999 157005 157007 157013 157017 157019 157023 157025 157029 157031 157033 157034 157035 157037 157038 157039 157041 157043 157047 157049 157053 157055 157059 157065 157067 157073 157077 157079 157083 157089 157095 157097 157103 157107 157109 157115 157119 157125 157133 203614
| 元素编号 | 元素性质或原子结构 |
| X | 最外层电子数是次外层电子数的2倍 |
| Y | 常温下单质为双原子分子,其氢化物水溶液呈碱性 |
| Z | 第三周期元素的简单离子中半径最小 |
 ,元素Y在周期表中的位置是第二周期VA族.
,元素Y在周期表中的位置是第二周期VA族.(2)元素Y与氢元素形成一种离子YH4+,则检测溶液中存在该离子的方法是:向溶液(或待测液)中加入NaOH溶液后加热,能产生使湿润的红色石蕊试纸变蓝的气体,说明溶液中存在NH4+离子,反之,不存在NH4+离子.
(3)元素X与元素Y相比,非金属性较强的是N (用元素符号表示),下列表述能证明这一事实的是bc.
a.常温下X的单质和Y的单质状态不同
b.Y的最高价氧化物对应的水化物的酸性比X的最高价氧化物对应的水化物的酸性强
c.X与Y形成的化合物中X元素呈正价态.


 ;
;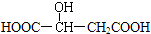 .
.