10.短周期元素X、Y、Z、W的原子序数依次递增,其原子的最外层电子数之和为15.X与Y、Z、W位于相邻周期,Z是地壳中含量最高的金属元素,W原子最外层电子数是X原子内层电子数的3倍.下列叙述正确的是( )
| A. | 原子半径的大小顺序:r(W)>r(Z)>r(Y)>r(X) | |
| B. | Z的最高价氧化物对应的水化物一定能溶于X的最高价氧化物对应的水化物 | |
| C. | X、W的简单气态氢化物都一定易溶于水 | |
| D. | Y的最高价氧化物对应的水化物的碱性比Z的强 |
8.某矿石的主要成分是由前20号元素中的4种组成,其化学式为WmYnZpZq.X、Y、Z、W分布在三个周期,原子序数依次增大,W、Y为金属元素,X原子的最外层电子数是次外层电子数的3倍,W的单质能与冷水剧烈反应,Y、Z原子的最外层电子数之和与X、W原子的最外层电子数之和相等,Y、Z位于同周期,Z的单质是一种良好的半导体.下列说法正确的是( )
| A. | 气态氢化物的稳定性:X<Z | |
| B. | Y的氯化物为离子化合物 | |
| C. | W位于第3周期IA族,其原子半径比其他元素的都大 | |
| D. | 将2 mol W的单质和1 mol Y的单质投入足量的水中会产生2.5 mol气体 |
7.当一个可逆反应进行到正反应速率与逆反应速率相等的时候,就达到了“化学平衡”.对于化学平衡的下列说法中正确的是( )
①化学反应达到化学平衡时,反应物与生成物的浓度(含量)保持不变;
②化学反应达到化学平衡时,整个反应处于停滞状态;
③平衡状态是指可逆反应在给定条件下进行的程度.
①化学反应达到化学平衡时,反应物与生成物的浓度(含量)保持不变;
②化学反应达到化学平衡时,整个反应处于停滞状态;
③平衡状态是指可逆反应在给定条件下进行的程度.
| A. | 只有① | B. | 只有①② | C. | 只有①③ | D. | ①②③ |
6.已知弱酸的电离平衡常数如下表:下列选项正确的是( )
| 弱酸 | H2CO3 | 水杨酸(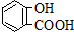 ) ) |
| 电离平衡常数(25℃) | Ka1=4.3×10-7 Ka2=5.6×10-11 | Ka1=1.3×10-3 Ka2=1.1×10-11 |
| A. | 常温下,等浓度、等体积的NaHCO3溶液pH小于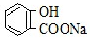 溶液pH 溶液pH | |
| B. | 常温下,等浓度、等体积的Na2CO3溶液和  溶液中所含离子总数前者小于后者 溶液中所含离子总数前者小于后者 | |
| C. |  +2NaHCO3→ +2NaHCO3→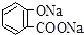 +2H2O+2CO2↑ +2H2O+2CO2↑ | |
| D. |  最多可与2molCO2反应 最多可与2molCO2反应 |
4.乳酸(2-羟基丙酸)为无色液体,与水混溶,弱挥发性.它在多种生物化学过程中起作用.某学习小组研究利用发酵法制乳酸以及探讨乳酸的部分性质.
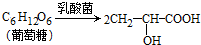
实验(一):乳酸的制取
步骤1:取14.40g葡萄糖(相对分子质量为180)于烧杯中,加人乳酸菌(厌氧)发酵,72小时后,过滤,将滤液转移到仪器A中,定容,得到500mL原液;
步骤2:取20.00mL原液于锥形瓶中,加人酚酞指示剂,用浓度为0.1000mol/L的NaOH溶液滴定至终点,重复4次,数据记录如下表.(假定原液中其他物质不与NaOH反应)
(1)仪器A是500mL容量瓶;
(2)如何判断已到达滴定终点当滴入最后一滴标准液时,锥形瓶中无色溶液变红色,且半分钟内不褪色;
(3)乳酸的产率为30%.
实验(二):乳酸的性质
已知乳酸的Ka=1.4×10-4,碳酸的Ka1=4.47×10-7.
(4)设计实验证明乳酸是弱酸:取0.1mol/L乳酸溶液于烧杯中,用PH计测定其PH值,若PH大于1,说明乳酸是弱酸或(常温下取0.1mol/L乳酸钠溶液于烧杯中,用pH计测定其PH值,若PH大于7,说明乳酸是弱酸)或(取PH=a乳酸溶液于烧杯中,加水稀释10n倍,用PH计测定其PH值,若PH小于a+n说明乳酸是弱酸);
(5)小组利用如图所示的仪器和药品,通过实验来比较乳酸和碳酸的酸性强弱.
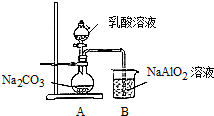
①可观察到烧杯中的现象是溶液出现白色浑浊;
写出烧杯中发生的化学反应方程式2NaAlO2+3H2O+CO2═2Al(OH)3↓+Na2CO3或NaAlO2+2H2O+CO2═Al(OH)3↓+NaHCO3;
②学习小组中有成员提出上述实验设计不够严谨,请你提出改进的措施在A与B之间增加一个装有碳酸氢钠溶液的洗气瓶.

实验(一):乳酸的制取
步骤1:取14.40g葡萄糖(相对分子质量为180)于烧杯中,加人乳酸菌(厌氧)发酵,72小时后,过滤,将滤液转移到仪器A中,定容,得到500mL原液;
步骤2:取20.00mL原液于锥形瓶中,加人酚酞指示剂,用浓度为0.1000mol/L的NaOH溶液滴定至终点,重复4次,数据记录如下表.(假定原液中其他物质不与NaOH反应)
| 次数 | 1 | 2 | 3 | 4 |
| 滴定体积(mL) | 19.22 | 19.18 | 19.80 | 19.20 |
(2)如何判断已到达滴定终点当滴入最后一滴标准液时,锥形瓶中无色溶液变红色,且半分钟内不褪色;
(3)乳酸的产率为30%.
实验(二):乳酸的性质
已知乳酸的Ka=1.4×10-4,碳酸的Ka1=4.47×10-7.
(4)设计实验证明乳酸是弱酸:取0.1mol/L乳酸溶液于烧杯中,用PH计测定其PH值,若PH大于1,说明乳酸是弱酸或(常温下取0.1mol/L乳酸钠溶液于烧杯中,用pH计测定其PH值,若PH大于7,说明乳酸是弱酸)或(取PH=a乳酸溶液于烧杯中,加水稀释10n倍,用PH计测定其PH值,若PH小于a+n说明乳酸是弱酸);
(5)小组利用如图所示的仪器和药品,通过实验来比较乳酸和碳酸的酸性强弱.

①可观察到烧杯中的现象是溶液出现白色浑浊;
写出烧杯中发生的化学反应方程式2NaAlO2+3H2O+CO2═2Al(OH)3↓+Na2CO3或NaAlO2+2H2O+CO2═Al(OH)3↓+NaHCO3;
②学习小组中有成员提出上述实验设计不够严谨,请你提出改进的措施在A与B之间增加一个装有碳酸氢钠溶液的洗气瓶.
3.现有短周期元素X、Y、Z、W,X、Y位于同主族,Y、Z位于同周期,Z、W位于同主族,X与Z、W都不在同一周期,Z的核电荷数是W的两倍,下列说法正确的是( )
0 156899 156907 156913 156917 156923 156925 156929 156935 156937 156943 156949 156953 156955 156959 156965 156967 156973 156977 156979 156983 156985 156989 156991 156993 156994 156995 156997 156998 156999 157001 157003 157007 157009 157013 157015 157019 157025 157027 157033 157037 157039 157043 157049 157055 157057 157063 157067 157069 157075 157079 157085 157093 203614
| A. | 有X、Y、W三种元素组成的化合物中既有离子键又有非极性共价键 | |
| B. | 简单离子半径由大到小的顺序是:Z>W>Y>X | |
| C. | 简单氢化物的沸点:W>Z,还原性:W>Z | |
| D. | Y、Z、W三元素形成的两种常见化合物的溶液中,水的电离程度相同 |
 )是一种有机合成中间体,A的合成路线如图所示,其中B~I分别代表一种有机物.
)是一种有机合成中间体,A的合成路线如图所示,其中B~I分别代表一种有机物.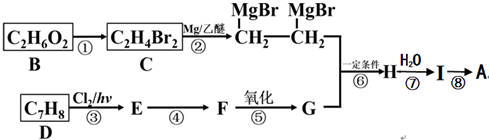
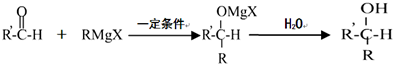
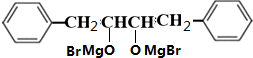 ;
;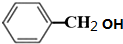 +O2$→_{△}^{铜}$2H2O+2
+O2$→_{△}^{铜}$2H2O+2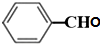 ;
;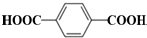 在催化剂的作用下生成聚合物--涤纶,写出涤纶的
在催化剂的作用下生成聚合物--涤纶,写出涤纶的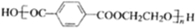 ;
; (任写一种).
(任写一种).