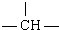2.下列措施能使纯水中水的电离平衡向右移动的是( )
| A. | 加人少量KOH固体 | B. | 滴人少量盐酸 | ||
| C. | 加入少量硫化钠固体 | D. | 加人少量纯水 |
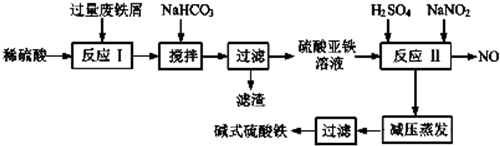
20.工业上利用废铁屑(含少量氧化铝、氧化铁等)生产碱式硫酸铁[Fe(OH)SO4]的工艺流程如图:
已知部分阳离子以氧氧化物形式沉淀时溶液的pH如下表.
回答下列问题:
(1)加入过量废铁屑的目的是使铁离子充分被还原为亚铁离子,同时防止亚铁离子被空气中氧气氧化(用离子方程式表示);加入少量NaHCO3的目的是Al3++3HCO3-=Al(OH)3↓+3CO2↑;该工艺中“搅拌”的作用是使反应物充分接触,加快反应速率,使反应充分进行;
(2)反应Ⅱ中的离子方程式为Fe2++2H++NO2-=Fe3++NO↑+H2O,该流程中可以循环、回收利用的物质是NO;
(3)生产碱式硫酸铁溶液蒸发时需要在减压条件下的原因是碱式硫酸铁受热易分解;
(4)在医药上常用硫酸亚铁与硫酸、硝酸的混合液反应制备碱式硫酸铁.根据我国质量标准,产品中不得含有Fe2+及NO3-,为检测所得产品中是否含有Fe2+,应使用的试剂A.(填写字母)

已知部分阳离子以氧氧化物形式沉淀时溶液的pH如下表.
| 沉淀物 | Fe(OH)3 | Fe(OH)2 | Al(OH)3 |
| 开始沉淀 | 2.3 | 7.5 | 3.4 |
| 完全沉淀 | 3.2 | 9.0 | 4.4 |
(1)加入过量废铁屑的目的是使铁离子充分被还原为亚铁离子,同时防止亚铁离子被空气中氧气氧化(用离子方程式表示);加入少量NaHCO3的目的是Al3++3HCO3-=Al(OH)3↓+3CO2↑;该工艺中“搅拌”的作用是使反应物充分接触,加快反应速率,使反应充分进行;
(2)反应Ⅱ中的离子方程式为Fe2++2H++NO2-=Fe3++NO↑+H2O,该流程中可以循环、回收利用的物质是NO;
(3)生产碱式硫酸铁溶液蒸发时需要在减压条件下的原因是碱式硫酸铁受热易分解;
(4)在医药上常用硫酸亚铁与硫酸、硝酸的混合液反应制备碱式硫酸铁.根据我国质量标准,产品中不得含有Fe2+及NO3-,为检测所得产品中是否含有Fe2+,应使用的试剂A.(填写字母)
| A.酸性KMnO4溶液 B.KSCN溶液 | C.氯水 D.NaOH溶液. |
19.下列每组内的三种物质中最后一种物质均为过量(充分反应后,该物质有剩余),分别向各组物质中加适量水,使它们充分反应后,静置、过滤,所得滤渣中有两种物质的是( )
| A. | CuCl2、Cu(NO3)2、Ba(OH)2 | B. | Al、Fe、CuSO4 | ||
| C. | MgSO4、Mg(NO3)2、Ba(OH)2 | D. | Al、Cu、FeSO4 |
15.如图原电池的电池反应为Zn+Cu2+═Zn2++Cu,该原电池及电解质溶液可能是( )

0 156875 156883 156889 156893 156899 156901 156905 156911 156913 156919 156925 156929 156931 156935 156941 156943 156949 156953 156955 156959 156961 156965 156967 156969 156970 156971 156973 156974 156975 156977 156979 156983 156985 156989 156991 156995 157001 157003 157009 157013 157015 157019 157025 157031 157033 157039 157043 157045 157051 157055 157061 157069 203614

| X | Y | 电解质溶液 | |
| A | Zn | Cu | ZnCl2溶液 |
| B | Cu | Zn | 稀H2SO4 |
| C | Cu | Zn | CuSO4溶液 |
| D | Zn | Zn | CuSO4溶液 |
| A. | A | B. | B | C. | C | D. | D |
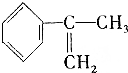 、液溴、浓硫酸和其他无机试剂,请用5个化学方程式表示下列转化过程:
、液溴、浓硫酸和其他无机试剂,请用5个化学方程式表示下列转化过程: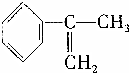 →
→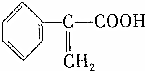
 ;
;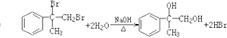 ;
; ;
; ;
;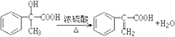 .
.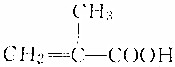 具有相同官能团的同分异构体的结构简式为CH2=CH-CH2COOH,CH3-CH=CH-COOH.
具有相同官能团的同分异构体的结构简式为CH2=CH-CH2COOH,CH3-CH=CH-COOH.