1.下表是部分短周期元素的原子半径及主要化合价:
试回答下列问题:
(1)五种元素中原子半径最大的元素在周期表中位置是第三周期IA族.
(2)Y的氢化物比Q的氢化物沸点高的原因是NH3的分子间存在氢键.
(3)X或与R按1:1的原子个数比形成化合物甲,甲中存在的化学键有离子键和非极性键(或离子键,共价键;X可与W组成含18e-的化合物乙,则乙的电子式为 ;X可与Z组成一种有恶臭味的气体丙,丙分子中各原子最外层均满足8e-结构,且含有非极性键.1mol丙气体可与2mol氧气完全反应,生成一种气体,且反应前后气体的总体积不变,该生成物能使澄清石灰水变浑浊,请写出丙分子的结构式O=C=C=C=O.
;X可与Z组成一种有恶臭味的气体丙,丙分子中各原子最外层均满足8e-结构,且含有非极性键.1mol丙气体可与2mol氧气完全反应,生成一种气体,且反应前后气体的总体积不变,该生成物能使澄清石灰水变浑浊,请写出丙分子的结构式O=C=C=C=O.
| 元素代号 | W | R | X | Y | Z | Q |
| 原子半径/nm | 0.037 | 0.186 | 0.074 | 0.075 | 0.077 | 0.110 |
| 主要化合价 | +1 | +1 | -2 | -3,+5 | +2、+4 | -3、+5 |
(1)五种元素中原子半径最大的元素在周期表中位置是第三周期IA族.
(2)Y的氢化物比Q的氢化物沸点高的原因是NH3的分子间存在氢键.
(3)X或与R按1:1的原子个数比形成化合物甲,甲中存在的化学键有离子键和非极性键(或离子键,共价键;X可与W组成含18e-的化合物乙,则乙的电子式为
 ;X可与Z组成一种有恶臭味的气体丙,丙分子中各原子最外层均满足8e-结构,且含有非极性键.1mol丙气体可与2mol氧气完全反应,生成一种气体,且反应前后气体的总体积不变,该生成物能使澄清石灰水变浑浊,请写出丙分子的结构式O=C=C=C=O.
;X可与Z组成一种有恶臭味的气体丙,丙分子中各原子最外层均满足8e-结构,且含有非极性键.1mol丙气体可与2mol氧气完全反应,生成一种气体,且反应前后气体的总体积不变,该生成物能使澄清石灰水变浑浊,请写出丙分子的结构式O=C=C=C=O.
19.已知在相同状况下,要使同一化学键断裂需要吸收的能量等于形成该化学键放出的能量.下列说法正确的是( )
| A. | 电解熔融的Al2O3可以制得金属铝和氧气,该反应是一个放出能量的反应 | |
| B. | 水分解产生氢气和氧气时放出能量 | |
| C. | 相同状况下,反应2CO+O2═2CO2是一个放热反应,则反应2CO2═2CO+O2是一个吸热反应 | |
| D. | 氯化氢分解成氢气和氯气时需要吸收能量,实验氯化氢的总能量高于氢气和氯气的总能量 |
17.下列有关化学键的叙述,正确是的( )
| A. | 共价化合物中可以含有离子键 | |
| B. | 单质分子中均不存在化学键 | |
| C. | 含活泼金属元素的化合物可能是共价化合物 | |
| D. | 含有共价键的化合物一定是共价化合物 |
16.下列说法正确的是( )
| A. | 离子化合物中一定不含共价键 | |
| B. | 共价化合物中一定不含离子键 | |
| C. | 全部由非金属元素形成的化合物一定是共价化合物 | |
| D. | 金属元素和非金属元素之间形成的化学键一定是离子键 |
15.下列每组物质中含有的化学键类型相同的是( )
| A. | NaCl、HCl、H2O、NaOH | B. | Cl2、Na2S、HCl、CO2 | ||
| C. | HBr、CCl4、H2O、CO2 | D. | Na2O2、H2O2、H2O、O2 |
14.实验室制备硝酸铝晶体[Al(NO3)3•9H2O]可使用下列方法:
铝片$\stackrel{适量NaOH溶液饱}{→}$澄清溶液$→_{过滤、洗涤}^{饱和NH_{4}HCO_{3}溶液}$白色沉淀$→_{溶解、浓缩、降温、结晶}^{适量HNO_{3}}$Al(NO3)3•9H2O
反映上述有关反应的离子方程式错误的是( )
0 156842 156850 156856 156860 156866 156868 156872 156878 156880 156886 156892 156896 156898 156902 156908 156910 156916 156920 156922 156926 156928 156932 156934 156936 156937 156938 156940 156941 156942 156944 156946 156950 156952 156956 156958 156962 156968 156970 156976 156980 156982 156986 156992 156998 157000 157006 157010 157012 157018 157022 157028 157036 203614
铝片$\stackrel{适量NaOH溶液饱}{→}$澄清溶液$→_{过滤、洗涤}^{饱和NH_{4}HCO_{3}溶液}$白色沉淀$→_{溶解、浓缩、降温、结晶}^{适量HNO_{3}}$Al(NO3)3•9H2O
反映上述有关反应的离子方程式错误的是( )
| A. | 2Al+2OH-+2H2O=2AlO2-+3H2↑ | |
| B. | 2HCO3-+2AlO2-+H2O=2CO2↑+2Al(OH)3↓ | |
| C. | NH4++AlO2-+2H2O=NH3•H2O+Al(OH)3↓ | |
| D. | 3H++Al(OH)3=Al3++3H2O |
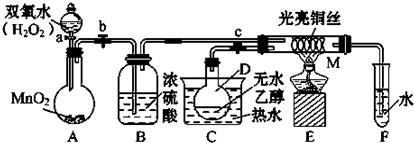
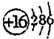 .
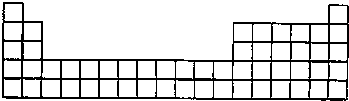
.
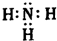 .化合物X的电子式
.化合物X的电子式 .
. .C2A4的水溶液呈碱(填“酸”“碱”或“中”)性,1mol C2A4最多可以与2mol HCl或NaOH发生中和反应生成正盐.C2A4 和A2D2 既具有氧化性,又具有还原性,从化合价的角度解释C2A4 和A2D2 既具有氧化性又具有还原性的原因N2H4中N显-2,H2O2中O显-1,均为相应元素的中间价态,所以既有氧化性,又有还原性
.C2A4的水溶液呈碱(填“酸”“碱”或“中”)性,1mol C2A4最多可以与2mol HCl或NaOH发生中和反应生成正盐.C2A4 和A2D2 既具有氧化性,又具有还原性,从化合价的角度解释C2A4 和A2D2 既具有氧化性又具有还原性的原因N2H4中N显-2,H2O2中O显-1,均为相应元素的中间价态,所以既有氧化性,又有还原性 ,该化合物与CA3和A2D的熔点由高到低的顺序为H2O>NH3>CH4(用化学式表示).
,该化合物与CA3和A2D的熔点由高到低的顺序为H2O>NH3>CH4(用化学式表示). .CA3、A2D、EA3的热稳定性由强到弱的顺序为H2O>NH3>PH3(用化学式表示).
.CA3、A2D、EA3的热稳定性由强到弱的顺序为H2O>NH3>PH3(用化学式表示).
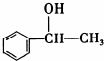 ,它不能发生的有机反应类型有④、⑥.
,它不能发生的有机反应类型有④、⑥.
 .
. .
. .
.