8. 如图是某小组验证碳酸钠性质的实验方案.
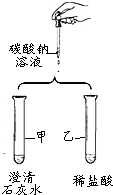
如图是某小组验证碳酸钠性质的实验方案.
(1)甲试管中反应的化学方程式为Na2CO3+Ca(OH)2═2NaOH+CaCO3↓;
(2)乙试管中的现象是大量气泡.
实验后他们将废液倒入废液缸,小欣发现废液澄清.
【提出问题】废液中的溶质含有哪些成分?
【查阅资料】①CaCl2溶液呈中性
②CaCl2+Na2CO3═2NaCl+CaCO3↓
【提出猜想】可能是Ⅰ.CaCl2、NaClⅡ.CaCl2、NaCl HCl
【设计实验】验证你的猜想
【讨论】如果废液是浑浊的,过滤后滤液中肯定没有物质是HCl.
 如图是某小组验证碳酸钠性质的实验方案.
如图是某小组验证碳酸钠性质的实验方案.(1)甲试管中反应的化学方程式为Na2CO3+Ca(OH)2═2NaOH+CaCO3↓;
(2)乙试管中的现象是大量气泡.
实验后他们将废液倒入废液缸,小欣发现废液澄清.
【提出问题】废液中的溶质含有哪些成分?
【查阅资料】①CaCl2溶液呈中性
②CaCl2+Na2CO3═2NaCl+CaCO3↓
【提出猜想】可能是Ⅰ.CaCl2、NaClⅡ.CaCl2、NaCl HCl
【设计实验】验证你的猜想
| 实验步骤 | 实验现象 | 结论 |
| 取少量的废液于试管中,滴加2~3滴石蕊试液,振荡. | 无现象 | 废液的pH=7; 猜想Ⅰ成立. |
7.在一定体积的10%的氢氧化钠溶液中滴加10%的盐酸,反应中溶液的温度与加入盐酸的体积变化如下:
根据上表分析:
(1)写出上述反应的化学方程式NaOH+HCl═NaCl+H2O,该反应属于放热(“吸热”或“放热”)反应;
(2)当加入盐酸体积为8mL时,溶液的pH大于7;
(3)当加入盐酸l0mL以上,溶液温度逐渐下降的原因是:过量盐酸起冷却降温作用,反应停止热量散失.
| 加入盐酸积V/mL | 2 | 4 | 6 | 8 | 10 | 12 | 14 | 16 | 18 | 20 |
| 测得溶液温度/℃ | 15.2 | 19.6 | 22.0 | 26.0 | 28.2 | 26.7 | 25.7 | 24.7 | 23.7 | 22.9 |
(1)写出上述反应的化学方程式NaOH+HCl═NaCl+H2O,该反应属于放热(“吸热”或“放热”)反应;
(2)当加入盐酸体积为8mL时,溶液的pH大于7;
(3)当加入盐酸l0mL以上,溶液温度逐渐下降的原因是:过量盐酸起冷却降温作用,反应停止热量散失.
5.下列的各组离子在酸性溶液中能大量共存的是( )
| A. | Ca2+、K+、Cl-、NO3- | B. | Na+、Ba2+、SO32-、ClO- | ||
| C. | Fe2+、K+、SO42-、NO3- | D. | Na+、Fe3+、S2-、Cl- |
4.如图是学校实验室从化学试剂商店买回的硫酸试剂标签上的部分内容.据此下列说法正确的是( )

0 156841 156849 156855 156859 156865 156867 156871 156877 156879 156885 156891 156895 156897 156901 156907 156909 156915 156919 156921 156925 156927 156931 156933 156935 156936 156937 156939 156940 156941 156943 156945 156949 156951 156955 156957 156961 156967 156969 156975 156979 156981 156985 156991 156997 156999 157005 157009 157011 157017 157021 157027 157035 203614

| A. | 该硫酸试剂可以做干燥剂,干燥任何气体 | |
| B. | 稀释该硫酸时,应将蒸馏水沿玻璃棒缓慢注入其中 | |
| C. | 常温下,2.7g Al与足量的稀硫酸反应得到H23.36L | |
| D. | 配制200mL 4.6mol•L-1的稀硫酸需取该硫酸50.0mL |
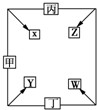 甲、乙、丙、丁四种单质在点燃条件下反应生成X、Y、Z、W四种化合物,其转化关系如图所示.又如:
甲、乙、丙、丁四种单质在点燃条件下反应生成X、Y、Z、W四种化合物,其转化关系如图所示.又如: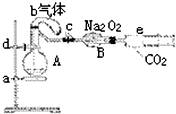 如图所示装置中,a是盛有标况下224mL空气(氧气占五分之一)和10mL 1.2mol/L硝酸的烧瓶,b是未充气(实验开始前内部没有气体)装有0.384g铜粉的气球,c是夹紧了的弹簧夹,d中盛有足量的过氧化钠,e是充有二氧化碳的注射器.整套装置经过气密性检查已合格.
如图所示装置中,a是盛有标况下224mL空气(氧气占五分之一)和10mL 1.2mol/L硝酸的烧瓶,b是未充气(实验开始前内部没有气体)装有0.384g铜粉的气球,c是夹紧了的弹簧夹,d中盛有足量的过氧化钠,e是充有二氧化碳的注射器.整套装置经过气密性检查已合格.

 ;FHCOOCH=CH2;
;FHCOOCH=CH2;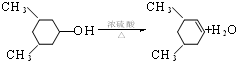 ; 反应④HCOOCH=CH2+H2O$→_{△}^{浓硫酸}$HCOOH+CH3CHO.
; 反应④HCOOCH=CH2+H2O$→_{△}^{浓硫酸}$HCOOH+CH3CHO.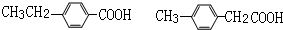 .
.
 A、B、C、D、E、F是初中化学常见的六种物质,其中A和B、C和D组成的元素种类相同,E是重要的建筑材料,F可用于清除铁锈.它们之间的转化关系如图所示(图中“-”表示两端的物质能发生化学反应;“→”表示物质间存在转化关系,图中已略去部分物质).回答下列问题:
A、B、C、D、E、F是初中化学常见的六种物质,其中A和B、C和D组成的元素种类相同,E是重要的建筑材料,F可用于清除铁锈.它们之间的转化关系如图所示(图中“-”表示两端的物质能发生化学反应;“→”表示物质间存在转化关系,图中已略去部分物质).回答下列问题: