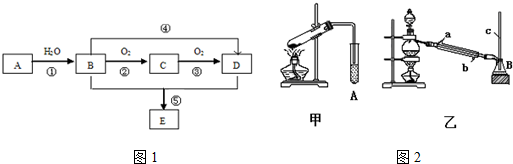
20.下列关于有机物结构、性质的叙述正确的是( )
| A. | 丙烯与环丁烷互为同系物 | |
| B. | 碳氢化合物中的化学键都是极性键 | |
| C. | 乙醇与金属钠反应时,乙醇分子中的C-H键断裂 | |
| D. | 苯不能使溴的四氯化碳溶液褪色,说明苯分子中没有与乙烯分子中类似的碳碳双键 |
19.物质的量浓度相同的硫酸铝钾[KA1(S04)2]和Ba(0H)2两种溶液按1:2的体积比混合,下列分析中正确的是( )
| A. | 得到沉淀的物质的量最大 | B. | 得到沉淀的质量最大 | ||
| C. | 反应后溶液仍含有Al3+ | D. | 反应后溶液仍含有AlO2- |
18.下列实验操作过程中,最终不一定得到沉淀物的是( )
| A. | 混合碳酸氢钙与氢氧化钠溶液 | B. | 混合硫酸铝与氢氧化钠溶液 | ||
| C. | 混合浓氨水和硫酸铝溶液 | D. | 混合盐酸和硝酸银溶液 |
17.“你挑着担,我牵着马,迎来日出送走晚霞…”西游记的主题歌给我们的启示主要是各尽所能的团队精神,不断战胜困难坚持到底的精神.在学习过程中我们也要学会主动交流,学会合作.几个同学做完分组实验后,针对将碘水中碘萃取出来的实验展开了热烈的讨论.请你判断,下列说法错误的是( )
| A. | 分液漏斗使用前要检验它是否漏水 | |
| B. | 萃取剂要求不溶于水,且比水更容易使碘溶解,用家里的植物油也行 | |
| C. | 注入碘水和莽取剂,倒转分液漏斗反复用力振荡后要立即分液 | |
| D. | 分液时打开旋塞使下层液体流出,上层液体从上口倒出 |
16.下列溶液中有关物质的量浓度关系正确的是( )
| A. | 10℃时pH=12的Na0H溶液与40℃时pH=12的Na0H溶液中:c(OH-)相等 | |
| B. | 25℃时pH=10的NaOH溶液与pH=10的氨水中:c(Na+)═c(NH4+) | |
| C. | 物质的量浓度相等的CH3COOH和CH3COONa溶液等体积混合:c(CH3COO-)+2c(OH-)═2c(H+)+c(CH3COOH) | |
| D. | 向10mLpH=12的Na0H溶液中滴加pH=2的HA溶液达中性:则混合液体积V总≥20mL |
11.汽车尾气中CO、NOx 以及燃煤废弃中的SO2都是大气污染物,对它们的治理具有重要意义.吸收SO2和NO,获得Na2S2O4和NH4NO3产品的流程图如图1(Ce为铈元素):
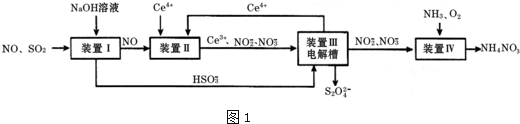
(1)装置Ⅰ中,NaOH溶液吸收SO2也可生成Na2SO3和NaHSO3的混合溶液
①写出NaOH溶液吸收SO2生成等物质的量的Na2SO3和NaHSO3混合溶液时总反应的离子方程式2SO2+3OH-=HSO3-+SO32-+H2O
②已知混合液pH随n(SO32-):n(HSO3-)变化关系如表:
当混合液中n(SO32-):n(HSO3-)=1:1时,c(Na+)>c(HSO3-)+2c(SO32-)(填“>”“=”或“<”)
(2)装置Ⅱ中,酸性条件下,NO被Ce4+氧化的产物主要是NO3-、NO2-,写出只生成NO2-的离子方程式NO+2H2O+3Ce4+=3Ce3++NO3-+4H+
(3)装置Ⅲ的作用之一是再生Ce4+,其原理如图所示.

①生成的Ce4+从电解槽的a(填字母序号)口流出;
②生成S2O42-的电极反应式为2HSO3-+2H++2e-=S2O42-+2H2O;
(4)已知进入装置Ⅳ的溶液中,NO2-的浓度为a g•L-1,要使1m3该溶液中的NO2-完全转化为NO3-,至少需向装置Ⅳ中通入标准状况下的O2$\frac{5600a}{23}$ L.(用含a代数式表示)
0 156837 156845 156851 156855 156861 156863 156867 156873 156875 156881 156887 156891 156893 156897 156903 156905 156911 156915 156917 156921 156923 156927 156929 156931 156932 156933 156935 156936 156937 156939 156941 156945 156947 156951 156953 156957 156963 156965 156971 156975 156977 156981 156987 156993 156995 157001 157005 157007 157013 157017 157023 157031 203614

(1)装置Ⅰ中,NaOH溶液吸收SO2也可生成Na2SO3和NaHSO3的混合溶液
①写出NaOH溶液吸收SO2生成等物质的量的Na2SO3和NaHSO3混合溶液时总反应的离子方程式2SO2+3OH-=HSO3-+SO32-+H2O
②已知混合液pH随n(SO32-):n(HSO3-)变化关系如表:
| n(SO32-):n(HSO3-) | 91:9 | 1:1 | 9:91 |
| pH | 8.2 | 7.2 | 6.2 |
(2)装置Ⅱ中,酸性条件下,NO被Ce4+氧化的产物主要是NO3-、NO2-,写出只生成NO2-的离子方程式NO+2H2O+3Ce4+=3Ce3++NO3-+4H+
(3)装置Ⅲ的作用之一是再生Ce4+,其原理如图所示.

①生成的Ce4+从电解槽的a(填字母序号)口流出;
②生成S2O42-的电极反应式为2HSO3-+2H++2e-=S2O42-+2H2O;
(4)已知进入装置Ⅳ的溶液中,NO2-的浓度为a g•L-1,要使1m3该溶液中的NO2-完全转化为NO3-,至少需向装置Ⅳ中通入标准状况下的O2$\frac{5600a}{23}$ L.(用含a代数式表示)
 ;
;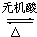 CH3COOH+(CH3)2CHOH.
CH3COOH+(CH3)2CHOH.
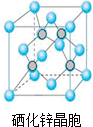 硒(Se)是一种有抗癌、抗氧化作用的元素,可以形成多种化合物.
硒(Se)是一种有抗癌、抗氧化作用的元素,可以形成多种化合物.