19.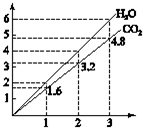 两种气态烃组成的混合气体,完全燃烧后得到CO2和H2O的物质的量随着混合烃物质的量的变化如图所示,则下列对混合烃的判断正确的是( )
两种气态烃组成的混合气体,完全燃烧后得到CO2和H2O的物质的量随着混合烃物质的量的变化如图所示,则下列对混合烃的判断正确的是( )
①可能有C2H4 ②一定没有C2H6 ③一定有C3H8
④一定有CH4 ⑤可能有C2H6 ⑥可能有C2H2.
 两种气态烃组成的混合气体,完全燃烧后得到CO2和H2O的物质的量随着混合烃物质的量的变化如图所示,则下列对混合烃的判断正确的是( )
两种气态烃组成的混合气体,完全燃烧后得到CO2和H2O的物质的量随着混合烃物质的量的变化如图所示,则下列对混合烃的判断正确的是( )①可能有C2H4 ②一定没有C2H6 ③一定有C3H8
④一定有CH4 ⑤可能有C2H6 ⑥可能有C2H2.
| A. | ②⑤⑥ | B. | ④⑥ | C. | ①②④ | D. | ②③ |
17.在光照条件下,将1mol CH4与Cl2反应,得到等物质的量的4种取代产物,则消耗的Cl2的物质的量为( )
| A. | 0.5mol | B. | 2mol | C. | 2.5mol | D. | 4mol |
16.下列比较中正确的是( )
| A. | 原子半径 Cl>Si>Na | B. | 金属性 Na>Mg>Al | ||
| C. | 碱性 LiOH>NaOH>KOH | D. | 酸性 H3PO4>H2SO4>HClO4 |
14.已知X、Y、Z均为短周期元素,它们之间可形成X2Z和YZ2两种化合物,X、Y、Z的原子序数依次增大,X原子K层的电子数只有一个,Y位于X的下一周期,它的最外层电子数比K层多2个,而Z原子核外的最外层电子数比次外层少2个,请回答下列问题;
(1)它们的元素符号分别为:XH,YC,ZS.
(2)用价层电子对互斥理论判断:
(3)N2O双称笑气,N2O与YZ2具有相似的分子结构,请分析原因:二者互为等电子体.
(1)它们的元素符号分别为:XH,YC,ZS.
(2)用价层电子对互斥理论判断:
| 物质 | 分子的价层电子对数 | 中心原子的杂化轨道类型 | 分子的立体构型名称 |
| X2Z | V形 | ||
| YZ2 |
13.W、X、Y、Z四种短周期元素的原子序数:X>W>Z>Y.W原子的最外层没有p电子,X原子核外s电子数与p电子数之比为1:1,Y原子最外层s电子数之比为1:1,Z原子的p电子数比Y原子的多2个.
(1)四种元素原子半径从大到小的顺序为Na>Mg>C>O(用元素符号表示).
(2)请用“>”或“<”填空:
(3)写出X元素的单质与Z、Y所形成的化合物反应的化学方程式,并标出电子转移的方向和数目: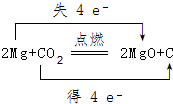 .
.
(1)四种元素原子半径从大到小的顺序为Na>Mg>C>O(用元素符号表示).
(2)请用“>”或“<”填空:
| 第一电离能 | 电负性 | 氢化物沸点 | 最高价氧化物对应水化物的碱性 |
| W<X | Z>Y | Y<Z | W>X |
 .
.
12.现有部分短周期元素的性质或原子结构如下表:
(1)写出元素X的离子结构示意图: .写出元素Z的简单气态氢化物的电子式:
.写出元素Z的简单气态氢化物的电子式: .
.
(2)写出元素Y的最高价氧化物对应的水化物与KOH反应的化学方程式:KOH+Al(OH)3=KAlO2+2H2O.
(3)T、Y、Z三种元素的单质中化学性质明显不同于其他单质的是Al(填元素符号,下同);元素T与氯化素相比,非金属性较强的是F,下列表述中能证明这一事实的是c(填字母).
a.常温下氯气的颜色比T单质的颜色深
b.T的单质通入氯化钠水溶液中不能置换出来
c.氯与T形成化合物中,氯元素呈正价.
| 元素 | 元素性质或原子的结构 |
| T | 2p轨道能级电子数比s能级电子数多1个 |
| X | L层p能级电子数比s能级电子数多2个 |
| Y | 第三周期元素的简单离子中半径最小 |
| Z | L层有3个未成对电子 |
 .写出元素Z的简单气态氢化物的电子式:
.写出元素Z的简单气态氢化物的电子式: .
.(2)写出元素Y的最高价氧化物对应的水化物与KOH反应的化学方程式:KOH+Al(OH)3=KAlO2+2H2O.
(3)T、Y、Z三种元素的单质中化学性质明显不同于其他单质的是Al(填元素符号,下同);元素T与氯化素相比,非金属性较强的是F,下列表述中能证明这一事实的是c(填字母).
a.常温下氯气的颜色比T单质的颜色深
b.T的单质通入氯化钠水溶液中不能置换出来
c.氯与T形成化合物中,氯元素呈正价.
11.下列有关原子结构和化学用语中,对电子运动状态描述最详尽的是( )
0 156831 156839 156845 156849 156855 156857 156861 156867 156869 156875 156881 156885 156887 156891 156897 156899 156905 156909 156911 156915 156917 156921 156923 156925 156926 156927 156929 156930 156931 156933 156935 156939 156941 156945 156947 156951 156957 156959 156965 156969 156971 156975 156981 156987 156989 156995 156999 157001 157007 157011 157017 157025 203614
| A. | ${\;}_{8}^{16}$O | B. | 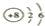 | C. | 1s22s22p4 | D. | 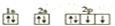 |
 实验室发现一瓶标签破损的溶液,如图所示,同学猜想,该溶液可能是C.(填字母序号)
实验室发现一瓶标签破损的溶液,如图所示,同学猜想,该溶液可能是C.(填字母序号)