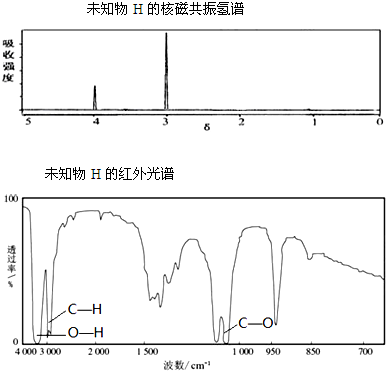
10.实验探究是体验知识的产生和形成过程的基本途径.下面是某同学完成的探究实验报告的一部分:
实验名称:卤素单质的氧化性强弱比较
实验药品:NaBr溶液、KI溶液、氯水、溴水、碘水、四氯化碳、淀粉碘化钾试纸 请回答:
(1)完成该实验需用到的实验仪器是试管、胶头滴管.
(2)②中反应的化学方程式为2NaBr+Cl2=2NaCl+Br2.③中反应的离子方程式为2I-+Cl2=2Cl-+I2.
(3)CCl4在实验中所起的作用是萃取剂.
(4)该同学的实验设计不足之是没有比较Br2和I2的氧化性强弱,改进的办法是把第③步改为:将溴水滴在KI淀粉试纸上,观察试纸是否变蓝色(或KI溶液+溴水+1 mL CCl4,振荡,静置,观察四氯化碳层颜色).(填相应的实验步骤)
实验名称:卤素单质的氧化性强弱比较
| 实验步骤 | 实验结论 |
| ①氯水+1mLCCl4,振荡,静置,观察四氯化碳层颜色 | 氧化性从强到弱的顺序:氯、溴、碘 |
| ②NaBr溶液+氯水+1mLCCl4,振荡,静置,观察四氯化碳层颜色 | |
| ③KI溶液+氯水+1mLCCl4,振荡,静置,观察四氯化碳层颜色 |
(1)完成该实验需用到的实验仪器是试管、胶头滴管.
(2)②中反应的化学方程式为2NaBr+Cl2=2NaCl+Br2.③中反应的离子方程式为2I-+Cl2=2Cl-+I2.
(3)CCl4在实验中所起的作用是萃取剂.
(4)该同学的实验设计不足之是没有比较Br2和I2的氧化性强弱,改进的办法是把第③步改为:将溴水滴在KI淀粉试纸上,观察试纸是否变蓝色(或KI溶液+溴水+1 mL CCl4,振荡,静置,观察四氯化碳层颜色).(填相应的实验步骤)
9.下列叙述正确的是( )
| A. | 副族元素没有非金属元素 | |
| B. | 除短周期外,其他周期均为18种元素 | |
| C. | 同周期相邻的第ⅡA族和第ⅢA族的元素,原子序数只相差1 | |
| D. | 核外电子排布相同的微粒化学性质也相同 |
8.下列说法中正确的是( )
| A. | 元素的种类由原子的质量数决定 | |
| B. | HF、HCl、HBr、HI的还原性从左到右依次减弱 | |
| C. | 第三周期非金属元素所形成的所有含氧酸的酸性从左到右一定依次增强 | |
| D. | 元素周期律是元素原子核外电子排布周期性变化的结果 |
7.用FeCl3溶液无法区别的一组试剂是( )
| A. | KSCN溶液、KCl溶液 | B. | NaOH溶液、NaCl溶液 | ||
| C. | 稀盐酸、稀硝酸 | D. | AgNO3溶液、稀HNO3 |
6.有关下列化合物的说法正确的是( )
| A. | SO2可大量用于漂白食品 | B. | 干冰、AgI均可用于人工降雨 | ||
| C. | 四氧化三铁常用作红色油漆和涂料 | D. | 小苏打的主要成份是Na2CO3 |
5.实验室制备Al(OH)3最好选用的试剂是( )
| A. | Al2O3和稀盐酸 | B. | Al2O3和水 | C. | Al2(SO4)3和NaOH | D. | AlCl3和氨水 |
4.同周期的三种主族元素X、Y、Z,它们的最高价氧化物对应的水化物分别是HXO4、H2YO4、H3ZO4,则下列判断正确的是( )
| A. | 含氧酸的酸性:H3ZO4>H2YO4>HXO4 | |
| B. | 非金属性:X<Y<Z | |
| C. | 气态氢化物的稳定性按X、Y、Z顺序增强 | |
| D. | 元素的最低负价的绝对值按X、Y、Z顺序增大 |
3.C+CO2?2CO,该反应吸收热量,反应速率为v1;N2+3H2?2NH3,该反应放出热量,反应速率为v2.对于上述反应,当温度升高时,v1和v2的变化情况为( )
| A. | 同时增大 | B. | 同时减小 | C. | 增大,减小 | D. | 减小,增大 |
1.(1)常温下,浓度均为0.1mol•L-1的下列五种钠盐溶液的pH如表
上述盐溶液中的阴离子,结合H+能力最强的是CO32-,根据表中数据,浓度均为0.01mol•L-1的下列四种酸的溶液分别稀释100倍,pH变化最大的是C(填编号).
A.HCN B.HClO C.CH3COOH D.H2CO3
(2)碳酸氢钠是一种强(填“强”或“弱”)电解质,写出HCO3-水解的离子方程式:HCO3-+H2O?H2CO3+OH-,常温下,0.1mol•L-1NaHCO3溶液的pH大于8,则溶液中Na+、HCO3-、H2CO3、CO32-、OH- 五种微粒的浓度由大到小的顺序为:c(Na+)>c(HCO3-)>c(OH-)>c(H2CO3)>c(CO32-).
(3)实验室中常用NaOH来进行洗气和提纯.
几种离子开始沉淀时的pH如下表:
当向含相同浓度Cu2+、Mg2+、Fe2+离子的溶液中滴加NaOH溶液时,Cu2+;(填离子符号)先沉淀,要使0.2mol/L硫酸铜溶液中Cu2+沉淀较为完全(使Cu2+浓度降至原来的千分之一),则应向溶液里加入氢氧化钠溶液使溶液pH为6.(KspCu(OH)2=2×10-20mol2•L-2)
(4)难溶电解质FeS在水溶液中存在着溶解平衡:FeS(s)?Fe2+(aq)+S2-(aq),在一定温度Ksp=c(Fe2+)c(S2-)=6.25×10-18,在该温度下,氢硫酸饱和溶液中存在c2(H+)c(S2-)=1.0×10-22.将适量FeCl2投入氢硫酸饱和溶液中,欲使溶液中c(Fe2+)=1.0mol/L,应调节溶液的pH=2.4(已知lg2=0.3)
0 156826 156834 156840 156844 156850 156852 156856 156862 156864 156870 156876 156880 156882 156886 156892 156894 156900 156904 156906 156910 156912 156916 156918 156920 156921 156922 156924 156925 156926 156928 156930 156934 156936 156940 156942 156946 156952 156954 156960 156964 156966 156970 156976 156982 156984 156990 156994 156996 157002 157006 157012 157020 203614
| 溶质 | CH3COONa | NaHCO3 | Na2CO3 | NaClO | NaCN |
| pH | 8.8 | 9.7 | 11.6 | 10.3 | 11.1 |
A.HCN B.HClO C.CH3COOH D.H2CO3
(2)碳酸氢钠是一种强(填“强”或“弱”)电解质,写出HCO3-水解的离子方程式:HCO3-+H2O?H2CO3+OH-,常温下,0.1mol•L-1NaHCO3溶液的pH大于8,则溶液中Na+、HCO3-、H2CO3、CO32-、OH- 五种微粒的浓度由大到小的顺序为:c(Na+)>c(HCO3-)>c(OH-)>c(H2CO3)>c(CO32-).
(3)实验室中常用NaOH来进行洗气和提纯.
几种离子开始沉淀时的pH如下表:
| 离子 | Fe2+ | Cu2+ | Mg2+ |
| pH | 7.6 | 5.2 | 10.4 |
(4)难溶电解质FeS在水溶液中存在着溶解平衡:FeS(s)?Fe2+(aq)+S2-(aq),在一定温度Ksp=c(Fe2+)c(S2-)=6.25×10-18,在该温度下,氢硫酸饱和溶液中存在c2(H+)c(S2-)=1.0×10-22.将适量FeCl2投入氢硫酸饱和溶液中,欲使溶液中c(Fe2+)=1.0mol/L,应调节溶液的pH=2.4(已知lg2=0.3)
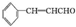 )在自然界存在于桂油中,是一种常用的植物调味油,工业上主要是按如下路线合成的:
)在自然界存在于桂油中,是一种常用的植物调味油,工业上主要是按如下路线合成的: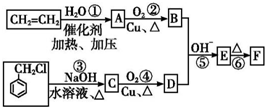

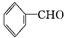 ;检验其中官能团的试剂为银氨溶液或新制的Cu(OH)2悬浊液.
;检验其中官能团的试剂为银氨溶液或新制的Cu(OH)2悬浊液.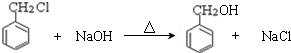 .
.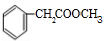 .
.