6.如表标出的是元素周期表的一部分元素,回答下列问题:
(1)表中用字母标出的元素中,化学性质最不活泼的是Ar(用元素符号表示,下同),其原子结构示意图为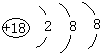 .
.
(2)表中用字母标出的元素中,能形成两性氢氧化物的元素是Al (用元素符号表示),写出该元素的单质与C最高价氧化物的水化物反应的化学方程式2Al+2NaOH+2H2O=2NaAlO2+3H2↑.
(3)在C、D、E形成的氢氧化物中,碱性最强的是NaOH(用化学式表示);在F、G、H形成的氢化物中最稳定的是HCl(用化学式表示).
(4)A和B可形成最简单的有机化合物,其结构式为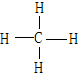 ;它的空间构型是正四面体.
;它的空间构型是正四面体.
(5)在H、K对应的单质中,氧化性较弱的是Br2(用化学式表示).
(6)J元素是过渡元素铁,工业上常用赤铁矿(主要成分为Fe2O3)为原料,采用高炉炼铁的方式炼铁,其原理是,把赤铁矿、焦碳和石灰石一起加入高炉,在高温下,把铁从赤铁矿中还原出来,写出该反应的化学方程式Fe2O3+3CO$\frac{\underline{\;高温\;}}{\;}$2Fe+3CO2.
| 1 | A | |||||||||||||||||
| 2 | B | |||||||||||||||||
| 3 | C | D | E | F | G | H | I | |||||||||||
| 4 | J | K | ||||||||||||||||
| 5 | ||||||||||||||||||
| 6 | ||||||||||||||||||
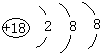 .
.(2)表中用字母标出的元素中,能形成两性氢氧化物的元素是Al (用元素符号表示),写出该元素的单质与C最高价氧化物的水化物反应的化学方程式2Al+2NaOH+2H2O=2NaAlO2+3H2↑.
(3)在C、D、E形成的氢氧化物中,碱性最强的是NaOH(用化学式表示);在F、G、H形成的氢化物中最稳定的是HCl(用化学式表示).
(4)A和B可形成最简单的有机化合物,其结构式为
 ;它的空间构型是正四面体.
;它的空间构型是正四面体.(5)在H、K对应的单质中,氧化性较弱的是Br2(用化学式表示).
(6)J元素是过渡元素铁,工业上常用赤铁矿(主要成分为Fe2O3)为原料,采用高炉炼铁的方式炼铁,其原理是,把赤铁矿、焦碳和石灰石一起加入高炉,在高温下,把铁从赤铁矿中还原出来,写出该反应的化学方程式Fe2O3+3CO$\frac{\underline{\;高温\;}}{\;}$2Fe+3CO2.
4.下列有关燃料电池的说法正确的是( )
| A. | 氢氧燃料电池可将热能直接转变为电能 | |
| B. | 燃料电池的能量转化率可达100% | |
| C. | 燃料电池与干电池或蓄电池的主要差别在于反应物不是储存在电池内部,而是由外设装备提供燃料和氧化剂 | |
| D. | 氢氧燃料电池工作时氢气在正极被氧化 |
2. (1)接触法制硫酸工艺中,其主反应在450℃并有催化剂存在下进行:2SO2(g)+O2(g)?2SO3(g)△H=-190kJ/mol
(1)接触法制硫酸工艺中,其主反应在450℃并有催化剂存在下进行:2SO2(g)+O2(g)?2SO3(g)△H=-190kJ/mol
①下列描述中能说明上述反应已达平衡的是bd.
a.υ(O2)正=2v(SO3)逆
b.容器中气体的平均相对分子质量不随时间而变化
c.容器中气体的密度不随时间而变化
d.容器中气体的分子总数不随时间而变化
②在一个固定容积为5L的密闭容器中充入0.20molSO2和0.10molO2半分钟后达到平衡,测得容器中含SO30.18mol,则υ(O2)=0.036mol•L-1•min-1;若继续通入0.4molSO2和0.2molO2则平衡向正反应方向移动(填“向正反应方向”、“向逆反应方向”或“不”),再次达到平衡后,0.54mol<n(SO3)<0.6mol.
(2)工业生产尿素的原理是以NH3和CO2为原料合成尿素[CO(NH2)],反应的化学方程式为2NH3(g)+CO2(g)?CO(NH2)(1)+H2O(l),该反应的平衡常数和温度关系如下:
①△H< 0 (填“>”、“<”或“=”)
②在一定温度和压强下,若原料气中的NH3和CO2的物质的量之比(氨碳比)$\frac{{n(N{H_3})}}{{n(C{O_2})}}=x$,下图是氨碳比(x)与CO2平衡转化率(a)的关系.a随着x增大而增大的原因是NH3的量增大,平衡正向移动,则增大CO2的转化率.
(3)图中的B点处,NH3的平衡转化率为32%.
 (1)接触法制硫酸工艺中,其主反应在450℃并有催化剂存在下进行:2SO2(g)+O2(g)?2SO3(g)△H=-190kJ/mol
(1)接触法制硫酸工艺中,其主反应在450℃并有催化剂存在下进行:2SO2(g)+O2(g)?2SO3(g)△H=-190kJ/mol①下列描述中能说明上述反应已达平衡的是bd.
a.υ(O2)正=2v(SO3)逆
b.容器中气体的平均相对分子质量不随时间而变化
c.容器中气体的密度不随时间而变化
d.容器中气体的分子总数不随时间而变化
②在一个固定容积为5L的密闭容器中充入0.20molSO2和0.10molO2半分钟后达到平衡,测得容器中含SO30.18mol,则υ(O2)=0.036mol•L-1•min-1;若继续通入0.4molSO2和0.2molO2则平衡向正反应方向移动(填“向正反应方向”、“向逆反应方向”或“不”),再次达到平衡后,0.54mol<n(SO3)<0.6mol.
(2)工业生产尿素的原理是以NH3和CO2为原料合成尿素[CO(NH2)],反应的化学方程式为2NH3(g)+CO2(g)?CO(NH2)(1)+H2O(l),该反应的平衡常数和温度关系如下:
| T/°C | 165 | 175 | 185 | 195 |
| K | 111.9 | 74.1 | 50.6 | 34.8 |
②在一定温度和压强下,若原料气中的NH3和CO2的物质的量之比(氨碳比)$\frac{{n(N{H_3})}}{{n(C{O_2})}}=x$,下图是氨碳比(x)与CO2平衡转化率(a)的关系.a随着x增大而增大的原因是NH3的量增大,平衡正向移动,则增大CO2的转化率.
(3)图中的B点处,NH3的平衡转化率为32%.
19.下列说法正确的是( )
0 156816 156824 156830 156834 156840 156842 156846 156852 156854 156860 156866 156870 156872 156876 156882 156884 156890 156894 156896 156900 156902 156906 156908 156910 156911 156912 156914 156915 156916 156918 156920 156924 156926 156930 156932 156936 156942 156944 156950 156954 156956 156960 156966 156972 156974 156980 156984 156986 156992 156996 157002 157010 203614
| A. | N-H键键能的含义是把1molNH3中的共价键全部拆开所吸收的能量 | |
| B. | ClO-的空间构型为平面三角形 | |
| C. | 卤素单质从F2到I2,在常温常压下的聚集状态由气态、液态到固态的原因是原子半径逐渐增大 | |
| D. | 熔点由高到低的顺序为:金刚石>MgO>NaCl>CCl4 |
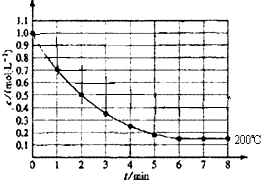 在一密闭容器中放入1molX(g)发生反应:X(g)?4Y(g)+Z(g),如图表示在 200℃时,X的浓度随时间变化的曲线.
在一密闭容器中放入1molX(g)发生反应:X(g)?4Y(g)+Z(g),如图表示在 200℃时,X的浓度随时间变化的曲线.
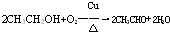 .
.
 .
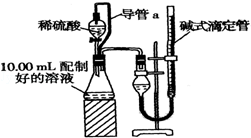
.
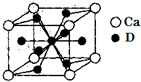 A、B、C、D是元素周期表中前36号元素,它们的核电荷数依次增大.第二周期元素A原子的核外成对电子数是未成对电子数的2倍且有3个能级,B原子的最外层p轨道的电子为半充满结构,C是地壳中含量最多的元素.D是第四周期元素,其原子核外最外层电子数与氢原子相同,其余各层电子均充满.请回答下列问题:
A、B、C、D是元素周期表中前36号元素,它们的核电荷数依次增大.第二周期元素A原子的核外成对电子数是未成对电子数的2倍且有3个能级,B原子的最外层p轨道的电子为半充满结构,C是地壳中含量最多的元素.D是第四周期元素,其原子核外最外层电子数与氢原子相同,其余各层电子均充满.请回答下列问题: