17.常温下,一定量的乙酸溶液与氢氧化钠溶液发生中和反应,下列说法正确的( )
| A. | c(CH3COO-)=c(Na+)时,参加反应的乙酸与氢氧化钠的物质的量之比为1:1 | |
| B. | c(CH3COO-)>c(Na+)>c(H+)>c(OH-)时,不一定是醋酸过量 | |
| C. | c(Na+)>c(CH3COO-)>c(OH-)>c(H+)时,一定是氢氧化钠过量 | |
| D. | c(CH3COO-)=c(Na+)时,该溶液一定呈中性 |
16.甲~辛等元素在周期表中的位置如表所示.下列说法不正确的是( )
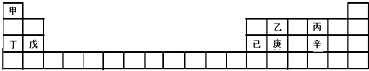

| A. | 甲、丁、戊的单质都是金属 | |
| B. | 乙、丙、辛都是非金属元素 | |
| C. | 乙、庚、辛都能形成氧化物 | |
| D. | 已的氧化物既可溶于KOH溶液又可溶于H2SO4溶液 |
15.下列有机化合物中,属于醇的有( )
| A. | CH3CH3 | B. | CH2=CHCl | C. | CH3CH2OH | D. | CH3COOCH2CH3 |
14.反应3X(g)+Y(g)?Z(g)+2W(g)在2L密闭容器中进行,5min后Y减少了0.1mol,则此反应的平均速率v为( )
| A. | V(Y)=0.02mol•L-1•min-1 | B. | V(Z)=0.10mol•L-1•min-1 | ||
| C. | V(X)=0.03mol•L-1•min-1 | D. | V(W)=0.02mol•L-1•s-1 |
13.短周期元素X、Y、Z、W的原子序数依次增大,X原子的最外层电子数是其内层电子总数的3倍,Y原子的最外层只有2个电子,Z单质可制成半导体材料,W与X属于同一主族.下列叙述正确的是( )
| A. | 元素X的简单气态氢化物的热稳定性比W的弱 | |
| B. | 元素W的最高价氧化物对应水化物的酸性比Z的弱 | |
| C. | 化合物YX、ZX2、WX3中化学键的类型相同 | |
| D. | 原子半径的大小顺序:rY>rZ>rW>rX |
12.甲烷中混有乙烯,欲除去乙烯得到纯净的甲烷,可依次通过盛有下列哪一组试剂的洗气瓶( )
| A. | 澄清石灰水、浓H2SO4 | B. | 酸性KMnO4溶液、浓H2SO4 | ||
| C. | 溴水、浓H2SO4 | D. | 浓H2SO4、NaOH溶液 |
11.某实验小组进行了“影响化学反应速率”的探究实验,原始数据记录如下:
(1)比较三组数据,初步得出的结论是:当其他条件不变时,H2SO4(填化学式)的浓度增加,反应速率加快(填“加快”、“减慢”或“不变”); 对比①、②两组实验,你认为影响反应速率的因素是固体接触面积.
(2)写出该反应的离子方程式Zn+2H+═Zn2++H2↑,
(3)经过试验对比,同学们在①组试验的试管中,滴入几滴CuSO4溶液后,锌粒表面有紫红色物质生成,同时发现试管中产生气泡的速度明显加快,请你分析,产生这种现象加快反应速率的原因是因为发生了原电池反应.
| Zn的质量 | H2SO4的浓度 | 收集20mL H2所需的时间 | |
| ① | 10g(锌粒) | 0.1mol/L | 153s |
| ② | 10g(锌粉) | 0.1mol/L | 125s |
| ③ | 10g(锌粉) | 0.2mol/L | 62s |
(2)写出该反应的离子方程式Zn+2H+═Zn2++H2↑,
(3)经过试验对比,同学们在①组试验的试管中,滴入几滴CuSO4溶液后,锌粒表面有紫红色物质生成,同时发现试管中产生气泡的速度明显加快,请你分析,产生这种现象加快反应速率的原因是因为发生了原电池反应.
9.下列有关电解质溶液的说法正确的是( )
0 156776 156784 156790 156794 156800 156802 156806 156812 156814 156820 156826 156830 156832 156836 156842 156844 156850 156854 156856 156860 156862 156866 156868 156870 156871 156872 156874 156875 156876 156878 156880 156884 156886 156890 156892 156896 156902 156904 156910 156914 156916 156920 156926 156932 156934 156940 156944 156946 156952 156956 156962 156970 203614
| A. | pH相同的 ①CH3COOK ②KHCO3 ③KClO三种溶液的c(K+):①>②>③ | |
| B. | 0.1mol/L NaHC2O4溶液与0.1mol/L NaOH溶液等体积混合,所得溶液中:C(Na+)>c(C2O42-)>c(HC2O4- )>c(OH-)>c(H+) | |
| C. | 常温下,0.1 mol/L Na2S溶液中存在:c(OH-)═c(H+)+c(HS-)+c(H2S) | |
| D. | 向0.2 mol•L-1的氨水中加入少量氯化铵固体,则溶液中$\frac{c(O{H}^{-})}{c(N{H}_{3}•{H}_{2}O)}$增大 |
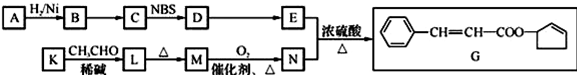
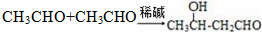
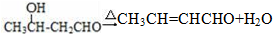
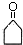 .
.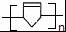 .
.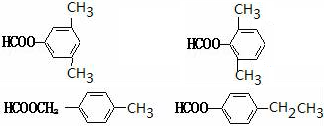 任意2种.
任意2种.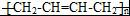 ).请设计合成路线(其他无机原料任选)并用如下方式表示:A$→_{反应条件}^{反应试剂}$B$→_{反应条件}^{反应试剂}$…目标产物HOCH2CH2CH2CH3$→_{△}^{浓硫酸}$CH2=CHCH2CH3$\stackrel{NBS}{→}$CH2=CHCHBrCH3$→_{△}^{NaOH醇溶液}$CH2=CHCH=CH2$\stackrel{催化剂}{→}$
).请设计合成路线(其他无机原料任选)并用如下方式表示:A$→_{反应条件}^{反应试剂}$B$→_{反应条件}^{反应试剂}$…目标产物HOCH2CH2CH2CH3$→_{△}^{浓硫酸}$CH2=CHCH2CH3$\stackrel{NBS}{→}$CH2=CHCHBrCH3$→_{△}^{NaOH醇溶液}$CH2=CHCH=CH2$\stackrel{催化剂}{→}$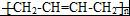 .
.