17.NA为阿伏伽德罗常数的值.下列说法正确的是( )
| A. | 1L 0.1mol/L的NaOH溶液中氧原子个数为0.1NA | |
| B. | 3g SiO2中Si-O数目为0.1NA | |
| C. | 0.1 mol钠与足量O2充分反应时,转移的电子数为0.1NA | |
| D. | 0.2 mol SO2与0.1mol O2充分反应,产物的分子数为0.1NA |
15.A、B、D、E、F为短周期元素,非金属元素A最外层电子数与其周期数相同,B的最外层电子数是其所在周期数的2倍.B在D中充分燃烧能生成其最高价化合物BD2.E+与D2-具有相同的电子数.A在F中燃烧,产物溶于水得到一种强酸.
(1)A在周期表位置第一周期第IA族,写出一种工业制备单质F的离子方程式:2Cl-+2H2O$\frac{\underline{\;电解\;}}{\;}$2OH-+H2↑+Cl2↑.
(2)B、D、E组成的一种盐中,E的质量分数为43%,其俗名为纯碱(或苏打),其水溶液与F单质反应的化学方程式为Cl2+2Na2CO3+H2O═NaClO+NaCl+2NaHCO3.
(3)由这些元素组成的物质,其组成和结构信息如表:
a的化学式为NaH;b的化学式为Na2O2和Na2C2;c的电子式为 ,d是金属晶体
,d是金属晶体
(4)由A和B元素组成的二元化合物是 沼气的主要成分,其与氧气在酸性电解质溶液中组成燃料电池消耗标况下11.2L氧气时转移电子数为2mol.
(1)A在周期表位置第一周期第IA族,写出一种工业制备单质F的离子方程式:2Cl-+2H2O$\frac{\underline{\;电解\;}}{\;}$2OH-+H2↑+Cl2↑.
(2)B、D、E组成的一种盐中,E的质量分数为43%,其俗名为纯碱(或苏打),其水溶液与F单质反应的化学方程式为Cl2+2Na2CO3+H2O═NaClO+NaCl+2NaHCO3.
(3)由这些元素组成的物质,其组成和结构信息如表:
| 物质 | 组成和结构信息 |
| a | 含有A的二元离子化合物 |
| b | 含有非极性共价键的二元离子化合物,且原子数之比为1:1 |
| c | 化学组成为BDF2 |
| d | 只存在一种类型作用力且可导电的单质晶体 |
 ,d是金属晶体
,d是金属晶体(4)由A和B元素组成的二元化合物是 沼气的主要成分,其与氧气在酸性电解质溶液中组成燃料电池消耗标况下11.2L氧气时转移电子数为2mol.
13.元素单质及其化合物有广泛用途,请根据周期表中第三周期元素相关知识回答下列问题:
(1)按原子序数递增的顺序(稀有气体除外),以下说法正确的是b.
a.原子序数和离子半径均减小 b.金属性减弱,非金属性增强
c.氧化物对应的水合物碱性减弱,酸性增强 d.单质的熔点降低
(2)原子最外层电子数与次外层电子数相同的元素名称为氩
(3)已知:
工业制镁时的反应方程式是MgCl2$\frac{\underline{\;电解\;}}{\;}$Mg+Cl2↑;制铝时,电解Al2O3不电解AlCl3的原因是熔融状态下氯化铝以分子存在,不导电,所以用电解熔融氧化铝的方法冶炼.
(4)晶体硅(熔点1410℃)是良好的半导体材料.由粗硅制纯硅过程如下:
Si(粗)$→_{460}^{Cl_{2}}$SiCl4$\stackrel{蒸馏}{→}$SiCl4(纯)$→_{1100℃}^{H_{2}}$Si(纯)
写出SiCl4的电子式: ;在上述由SiCl4制纯硅的反应中,测得每生成1.12kg纯硅需吸收akJ热量,该反应的热化学方程式:SiCl4(g)+2H2(g)$\frac{\underline{\;高温\;}}{\;}$Si(s)+4HCl(g)△H=-0.025kJ/mol
;在上述由SiCl4制纯硅的反应中,测得每生成1.12kg纯硅需吸收akJ热量,该反应的热化学方程式:SiCl4(g)+2H2(g)$\frac{\underline{\;高温\;}}{\;}$Si(s)+4HCl(g)△H=-0.025kJ/mol
(5)P2O5是非氧化性干燥剂,下列气体不能用浓硫酸干燥,可用P2O5干燥的b:
a. NH3 b. HI c. SO2 d. CO2
(6)KClO3可用于实验室制O2,若不加催化剂,400℃时分解只生成两种盐,其中一种是无氧酸盐,另一种盐的阴阳离子个数比为1:1.写出该反应的化学方程式:4KClO3$\frac{\underline{\;400℃\;}}{\;}$KCl+3KClO4.
(1)按原子序数递增的顺序(稀有气体除外),以下说法正确的是b.
a.原子序数和离子半径均减小 b.金属性减弱,非金属性增强
c.氧化物对应的水合物碱性减弱,酸性增强 d.单质的熔点降低
(2)原子最外层电子数与次外层电子数相同的元素名称为氩
(3)已知:
| 化合物 | MgO | Al2O3 | MgCl2 | AlCl3 |
| 类型 | 离子化合物 | 离子化合物 | 离子化合物 | 共价化合物 |
| 熔点/℃ | 2800 | 2050 | 714 | 191 |
(4)晶体硅(熔点1410℃)是良好的半导体材料.由粗硅制纯硅过程如下:
Si(粗)$→_{460}^{Cl_{2}}$SiCl4$\stackrel{蒸馏}{→}$SiCl4(纯)$→_{1100℃}^{H_{2}}$Si(纯)
写出SiCl4的电子式:
 ;在上述由SiCl4制纯硅的反应中,测得每生成1.12kg纯硅需吸收akJ热量,该反应的热化学方程式:SiCl4(g)+2H2(g)$\frac{\underline{\;高温\;}}{\;}$Si(s)+4HCl(g)△H=-0.025kJ/mol
;在上述由SiCl4制纯硅的反应中,测得每生成1.12kg纯硅需吸收akJ热量,该反应的热化学方程式:SiCl4(g)+2H2(g)$\frac{\underline{\;高温\;}}{\;}$Si(s)+4HCl(g)△H=-0.025kJ/mol(5)P2O5是非氧化性干燥剂,下列气体不能用浓硫酸干燥,可用P2O5干燥的b:
a. NH3 b. HI c. SO2 d. CO2
(6)KClO3可用于实验室制O2,若不加催化剂,400℃时分解只生成两种盐,其中一种是无氧酸盐,另一种盐的阴阳离子个数比为1:1.写出该反应的化学方程式:4KClO3$\frac{\underline{\;400℃\;}}{\;}$KCl+3KClO4.
12.在100ml硝酸和硫酸的混合液中,两种酸的物质的量浓度之和是0.6mol/l.向混合液中加入足量的铜粉,加热充分反应,所得溶液中铜离子的物质的量浓度最大值为(忽略反应前后溶液体积变化)( )
| A. | 0.30mol/l | B. | 0.225mol/l | C. | 0.45mol/l | D. | 0.36mol/l |
11.设NA为阿伏伽德罗常数的值.下列说法正确的是( )
| A. | 标准状况下,11.2L苯中含有分子的数目为0.5NA | |
| B. | 0.1mol丙烯酸中含有双键的数目为0.1NA | |
| C. | 1.6g由氧气和臭氧组成的混合物中含有氧原子的数目为0.1NA | |
| D. | 在过氧化钠与水的反应中,每生成0.1mol氧气,转移电子的数目为0.4NA |
9.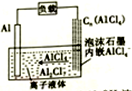 最近报道的一种能快速充放电的离子电池,其中的电解质为离子液体{AlCl4-/[EMI]+},放电时有关离子转化如图所示.下列说法正确的是 ( )
最近报道的一种能快速充放电的离子电池,其中的电解质为离子液体{AlCl4-/[EMI]+},放电时有关离子转化如图所示.下列说法正确的是 ( )
 最近报道的一种能快速充放电的离子电池,其中的电解质为离子液体{AlCl4-/[EMI]+},放电时有关离子转化如图所示.下列说法正确的是 ( )
最近报道的一种能快速充放电的离子电池,其中的电解质为离子液体{AlCl4-/[EMI]+},放电时有关离子转化如图所示.下列说法正确的是 ( )| A. | 放电时,负极发生2AlCl4--e-═Al2Cl7-+Cl- | |
| B. | 放电时,有机阳离子[EMI]+向铝电极方向移动 | |
| C. | 充电时,阴极发生:4Al2Cl7-+3e-═Al+7AlCl4- | |
| D. | 充电时,泡沫石墨极与外电源的负极相连 |
8.某香料的合成原料(Y)的分子结构如图,下列有关Y的叙述正确的是( )

0 156763 156771 156777 156781 156787 156789 156793 156799 156801 156807 156813 156817 156819 156823 156829 156831 156837 156841 156843 156847 156849 156853 156855 156857 156858 156859 156861 156862 156863 156865 156867 156871 156873 156877 156879 156883 156889 156891 156897 156901 156903 156907 156913 156919 156921 156927 156931 156933 156939 156943 156949 156957 203614

| A. | Y的化学式为C9H10O | |
| B. | Y可以发生加成反应和银镜反应 | |
| C. | Y分子中最多有7个碳原子处于同一平面 | |
| D. | Y的同分异构体中,属于芳香烃化合物、且苯环上仅含有一个侧链的醇类物质有5种 |
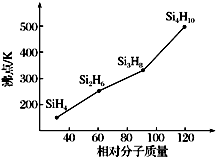 太阳能电池常用材料除单晶硅,还有铜铟镓硒等化合物.
太阳能电池常用材料除单晶硅,还有铜铟镓硒等化合物.
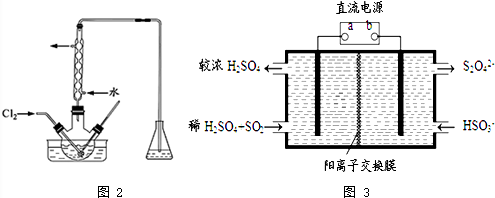
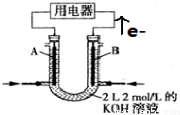 将CH4设计成燃料电池,装置如图所示(A、B为多孔碳棒)
将CH4设计成燃料电池,装置如图所示(A、B为多孔碳棒)