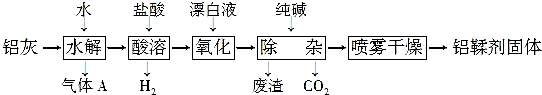
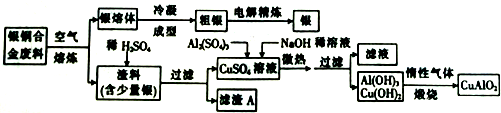
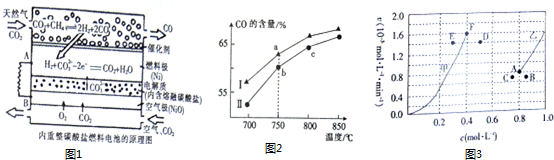
17.空气污染已成为人类社会面临的重大威胁.下列气体中,不会造成空气污染的是( )
| A. | NO2 | B. | Cl2 | C. | N2 | D. | SO2 |
11.短周期元素A、B、C、D的原子序数依次增大且互不同主族,A元素在自然界中存在两种气态单质,其中一种能吸收短波紫外线,A、B两元素的族序数之差为3,C、D不相邻,C的最外层电子数是次外层电子数的一半,下列判断正确的是( )
| A. | 简单离子的半径大小:D>B>A | |
| B. | B的单质既能和酸反应,又能和碱反应 | |
| C. | A分别与C、D形成的化合物均易溶于水 | |
| D. | 最高价氧化物对应水化物的酸性:C>D |
10.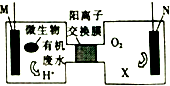 为解决淀粉厂废水中BOD严重超标的问题,有人设计了电化学降解法.如图是利用一种微生物将有机物将废水中有机物[主要成分是(C6H10O5)n]的化学能转化为电能的装置,下列说法中正确的是( )
为解决淀粉厂废水中BOD严重超标的问题,有人设计了电化学降解法.如图是利用一种微生物将有机物将废水中有机物[主要成分是(C6H10O5)n]的化学能转化为电能的装置,下列说法中正确的是( )
 为解决淀粉厂废水中BOD严重超标的问题,有人设计了电化学降解法.如图是利用一种微生物将有机物将废水中有机物[主要成分是(C6H10O5)n]的化学能转化为电能的装置,下列说法中正确的是( )
为解决淀粉厂废水中BOD严重超标的问题,有人设计了电化学降解法.如图是利用一种微生物将有机物将废水中有机物[主要成分是(C6H10O5)n]的化学能转化为电能的装置,下列说法中正确的是( )| A. | N极是负极 | |
| B. | 该装置工作时,H+从右侧经阳离子交换膜移向左侧 | |
| C. | 负极的电极反应为:(C6H10O5)n+7H2O-24ne-═6nCO2↑+24nH+ | |
| D. | 物质X是OH- |
8. ClO2是一种高效水处理剂,某实验小组用如图所示装置制取并收集ClO2.已知:
ClO2是一种高效水处理剂,某实验小组用如图所示装置制取并收集ClO2.已知:
(1)仪器a名称是圆底烧瓶.装置A中反应的化学方程式为2KClO3+H2C2O4=K2CO3+CO2↑+2ClO2↑+H2O.用H2C2O4、稀硫酸和KClO3制备ClO2的最大优点是二氧化氯被二氧化碳稀释,可防止二氧化氯爆炸.
(2)装置C的作用是防止倒吸,装置B中用冰水浴的目的是冷凝并分离出二氧化氯.
(3)工业上生产HClO4和NaClO2的工艺流程如图所示.

①操作2的名称是蒸馏;
②设计简单实验证明HClO2为弱酸:在常温下测定NaClO2溶液的PH值,若PH值大于7,则为HClO2弱酸.
(4)ClO2很不稳定,需用随制,产物用水吸收得到ClO2溶液,为测定所得溶液中ClO2的含量,进行下列实验:
步骤1:准确量取V1 mLClO2溶液于锥形瓶中.
步骤2:用稀硫酸调节ClO2溶液的pH≤2.0,加入足量的KI晶体,静置片刻.
步骤3:加入指示剂,用c mol•L-1•的Na2S2O3溶液滴定至终点,消耗Na2S2O3溶液V2mL.
实验中加入的指示剂是淀粉溶液,达到滴定终点时的现象是溶液由蓝色变为无色,且保持30s不变.
原溶液中ClO2的含量为$\frac{13.5cV{\;}_{2}}{V{\;}_{1}}$g/L(用含字母的代数式表示)g•L-1.(已知:2ClO2+8H++10I-═2Cl-+5I2+4H2,2S2O32-+I2═2I-+S2O32-)
0 156757 156765 156771 156775 156781 156783 156787 156793 156795 156801 156807 156811 156813 156817 156823 156825 156831 156835 156837 156841 156843 156847 156849 156851 156852 156853 156855 156856 156857 156859 156861 156865 156867 156871 156873 156877 156883 156885 156891 156895 156897 156901 156907 156913 156915 156921 156925 156927 156933 156937 156943 156951 203614
 ClO2是一种高效水处理剂,某实验小组用如图所示装置制取并收集ClO2.已知:
ClO2是一种高效水处理剂,某实验小组用如图所示装置制取并收集ClO2.已知:| 信息 | 内容 |
| ① | ClO2为黄绿色气体,极易溶于水,熔点为-59℃,沸点为11℃,具有强氧化性 |
| ② | ClO2易爆炸,若用惰性气体等稀释,则爆炸的可能性大降低 |
| ③ | HClO4、HClO2均是强酸,HClO4为无色透明液体,沸点为90℃;HClO2很不稳定,容易分解 |
(2)装置C的作用是防止倒吸,装置B中用冰水浴的目的是冷凝并分离出二氧化氯.
(3)工业上生产HClO4和NaClO2的工艺流程如图所示.

①操作2的名称是蒸馏;
②设计简单实验证明HClO2为弱酸:在常温下测定NaClO2溶液的PH值,若PH值大于7,则为HClO2弱酸.
(4)ClO2很不稳定,需用随制,产物用水吸收得到ClO2溶液,为测定所得溶液中ClO2的含量,进行下列实验:
步骤1:准确量取V1 mLClO2溶液于锥形瓶中.
步骤2:用稀硫酸调节ClO2溶液的pH≤2.0,加入足量的KI晶体,静置片刻.
步骤3:加入指示剂,用c mol•L-1•的Na2S2O3溶液滴定至终点,消耗Na2S2O3溶液V2mL.
实验中加入的指示剂是淀粉溶液,达到滴定终点时的现象是溶液由蓝色变为无色,且保持30s不变.
原溶液中ClO2的含量为$\frac{13.5cV{\;}_{2}}{V{\;}_{1}}$g/L(用含字母的代数式表示)g•L-1.(已知:2ClO2+8H++10I-═2Cl-+5I2+4H2,2S2O32-+I2═2I-+S2O32-)
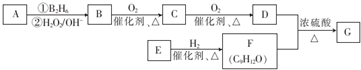
 ;该反应的反应类型为酯化反应或取代反应.
;该反应的反应类型为酯化反应或取代反应.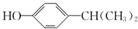 .
.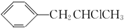 为原料也可合成F,请参考题目中的相关信息写出相应的合成路线图(反应条件中的试剂写在箭头上方,其他写在箭头下方):
为原料也可合成F,请参考题目中的相关信息写出相应的合成路线图(反应条件中的试剂写在箭头上方,其他写在箭头下方):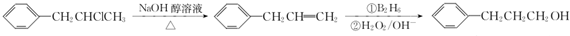 .
.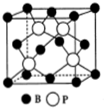 氮、磷、砷是同族元素,该族元素单质及其化合物在农药、化肥等方面有重要应用.
氮、磷、砷是同族元素,该族元素单质及其化合物在农药、化肥等方面有重要应用.