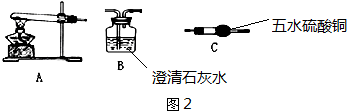
18.下列说法不正确的是( )
| A. | 纤维素、蔗糖、葡萄糖和脂肪在一定条件下都可发生水解反应 | |
| B. | 分子式是C3H8O的所有同分异构体共3种 | |
| C. | 用乙醇和浓H2SO4制备乙烯时,不可用水浴加热控制反应的温度 | |
| D. | 迷迭香酸结构如图: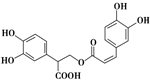 1 mol 迷迭香酸最多能和含6 mol NaOH的水溶液完全反应 1 mol 迷迭香酸最多能和含6 mol NaOH的水溶液完全反应 |
17.将FeO与Cu(NO3)2的混合物9.08g全部溶于300mL、1mol/L的盐酸中,有部分Fe2+被酸性条件下的NO3-氧化(其化学反应方程式为:3Fe2++NO3-+4H+=3Fe3++NO↑+2H2O),放出NO气体448mL(标准状况);继续向溶液中通入一定量的Cl2恰好将溶液中的Fe2+完全氧化;再加入10g过量的铁粉,充分反应放出H2,过滤,得到不溶固体.下列叙述不正确的是( )
| A. | Cu(NO3)2的物质的量为0.01mol | B. | 通入Cl2的体积(标准状况)为448mL | ||
| C. | 放出H2的体积(标准状况)为112mL | D. | 得到不溶固体的质量为6.72g |
16.设NA表示阿伏加德罗常数的值.下列说法正确的是( )
| A. | 常温常压下,1 mol Na2O2中含有的阴、阳离子总数是3NA | |
| B. | 标准状况下,2.24 L苯中含C-H数目为0.6NA | |
| C. | 3.2 g由氧气和臭氧组成的混合物中含有的分子数目为0.1NA | |
| D. | Cl2与NaOH溶液反应每生成1 molNaCl,转移电子的数目为2NA |
15.下列物质性质与应用不存在对应关系的是( )
| A. | K2FeO4具有强氧化性,可用作水处理剂 | |
| B. | 氢氧化铝具有弱碱性,可用作制胃酸中和剂 | |
| C. | 碳具有还原性,可用作锌锰干电池的正极材料 | |
| D. | 常温下浓硫酸能使铝发生钝化,可用铝制容器贮运浓硫酸 |
14.氨气在纯氧中燃烧(如图所示),生成化学性质稳定的气体X和水.下列说法正确的是( )
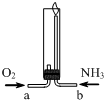

| A. | 气体X的分子式为NO | |
| B. | N2、N4为元素N的两种同素异形体 | |
| C. | 该反应条件下,氨气的还原性小于水 | |
| D. | 两种气体通入的先后顺序是NH3、O2 |
10.T℃时,在甲、乙、丙三个容积均为2L的恒容密闭容器中投入SO2(g)和O2(g),发生反应:2SO2(g)+O2(g)?2SO3(g),5min时甲达到平衡.其起始量及SO2的平衡转化率如下表所示.下列叙述不正确的是( )
| 容器 | 甲 | 乙 | 丙 | |
| 起始量 | n(SO2)/mol | 0.4 | 0.8 | 0.8 |
| n(O2)/mol | 0.24 | 0.24 | 0.48 | |
| SO2的平衡转化率 | 80% | α1 | α2 | |
| A. | 0~5min内,甲中SO2的反应速率为0.032mol•L-1•min-1 | |
| B. | T℃时,该反应的平衡常数K=400 | |
| C. | 平衡时,甲、丙中气体密度分别为ρ1、ρ2,则ρ2>2ρ1 | |
| D. | 平衡时,SO2的转化率:α1<80%<α2 |
9.瑞典ASES公司设计的用于驱动潜艇的液氨-液氧燃料电池示意图如图所示,下列有关说法正确的是( )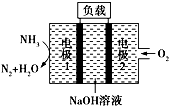
0 156742 156750 156756 156760 156766 156768 156772 156778 156780 156786 156792 156796 156798 156802 156808 156810 156816 156820 156822 156826 156828 156832 156834 156836 156837 156838 156840 156841 156842 156844 156846 156850 156852 156856 156858 156862 156868 156870 156876 156880 156882 156886 156892 156898 156900 156906 156910 156912 156918 156922 156928 156936 203614

| A. | 电池工作时,电极2上发生氧化反应 | |
| B. | 电池工作一段时间后停止,溶液pH值比开始时明显增大 | |
| C. | 电极1发生的电极反应为2NH3+6OH--6e-═N2↑+6H2O | |
| D. | 用该电池做电源电解精炼铜,理论上每消耗0.2 mol NH3的同时阳极会得到19.2g纯铜 |