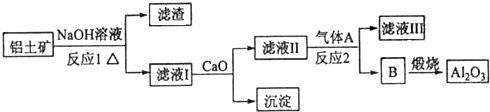
7.下列说法正确的是( )
| A. | C元素的相对分子质量是12,则1mol C的质量为12g/mol | |
| B. | 1mol Cl2的体积为22.4L | |
| C. | 1mol CO2中含有3个原子 | |
| D. | 已知NaOH溶液的物质的量浓度为0.5mol/L,则2L该溶液中含NaOH 1mol |
6.在标准状况下,气体摩尔体积约为22.4L/mol,则标准状况下1.5molH2的体积约为( )
| A. | 44.8L | B. | 5L | C. | 11.2L | D. | 33.6L |
3.下列说法错误的是( )
| A. | 硅胶疏松多孔,可用作催化剂的载体 | |
| B. | 日用铝制品表面覆盖着氧化膜,对内部金属起保护作用 | |
| C. | 镧镍合金能大量吸收H2形成金属氢化物,可作储氢材料 | |
| D. | 氮的固定只有在高温、高压、催化剂的条件下才能实现 |
2.新型净水剂高铁酸钠(Na2FeO4)可通过以下反应制备:Fe2O3+3Na2O2$\frac{\underline{\;熔融\;}}{\;}$2Na2FeO4+Na2O,下列说法正确的是( )
| A. | 在Na2FeO4中Fe为+4价,具有强氧化性,能杀菌消毒 | |
| B. | Na2O2既是氧化剂又是还原剂 | |
| C. | Na2FeO4既是氧化产物又是还原产物 | |
| D. | 3mol Na2O2发生反应,有12mol电子转移 |
1.甲烷分子中的四个氢原子都可以被取代.若甲烷分子中的四个氢原子都被苯基取代,则可得到分子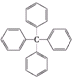 .对该分子的描述正确的是( )
.对该分子的描述正确的是( )
 .对该分子的描述正确的是( )
.对该分子的描述正确的是( )| A. | 分子式为C25H20 | B. | 其不是芳香烃 | ||
| C. | 所有碳原子都在同一平面上 | D. | 该物质为脂环烃 |
19.硫元素的价电子较多,与氯能形成多种化合物.将Cl2通入熔融的硫磺可以制得S2Cl2,S2Cl2是黄红色油状发烟液体,遇水分解出无色有刺激性气味的气体,且溶液变浑浊;而S2Cl2与NaOH 溶液反应可生成三种盐,得到澄清溶液.S2Cl2在合成橡胶,硬水软化等方面有着重要应用.有关S2Cl2的叙述正确的有( )
0 156741 156749 156755 156759 156765 156767 156771 156777 156779 156785 156791 156795 156797 156801 156807 156809 156815 156819 156821 156825 156827 156831 156833 156835 156836 156837 156839 156840 156841 156843 156845 156849 156851 156855 156857 156861 156867 156869 156875 156879 156881 156885 156891 156897 156899 156905 156909 156911 156917 156921 156927 156935 203614
| A. | S2Cl2的结构简式:S-Cl-S-Cl | |
| B. | 13.5g S2Cl2和NaOH反应电子转移数为0.1NA | |
| C. | S2Cl2和NaOH水溶液反应,氧化与还原产物物质的量之比为1:1 | |
| D. | S2Cl2和水反应中,氧化剂还原剂物质的量之比为1:1 |