6. 2015年10月5日,中国科学家屠哟坳首次获诺贝尔生理学或医学奖,以表彰她创制新型抗疟药-青蒿素和双氢青蒿素,其中青蒿素的结构简式如图所示,则青蒿素分子中碳、氧原子的个数比为( )
2015年10月5日,中国科学家屠哟坳首次获诺贝尔生理学或医学奖,以表彰她创制新型抗疟药-青蒿素和双氢青蒿素,其中青蒿素的结构简式如图所示,则青蒿素分子中碳、氧原子的个数比为( )
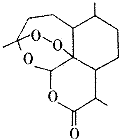
 2015年10月5日,中国科学家屠哟坳首次获诺贝尔生理学或医学奖,以表彰她创制新型抗疟药-青蒿素和双氢青蒿素,其中青蒿素的结构简式如图所示,则青蒿素分子中碳、氧原子的个数比为( )
2015年10月5日,中国科学家屠哟坳首次获诺贝尔生理学或医学奖,以表彰她创制新型抗疟药-青蒿素和双氢青蒿素,其中青蒿素的结构简式如图所示,则青蒿素分子中碳、氧原子的个数比为( )| A. | 2:1 | B. | 3:1 | C. | 12:5 | D. | 16:5 |
5.下列卤代烃不能通过烯烃与相应卤化氢加成得到的是( )
| A. | CH3-CH2-Br | B. | 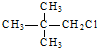 | ||
| C. | 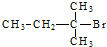 | D. | 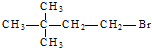 |
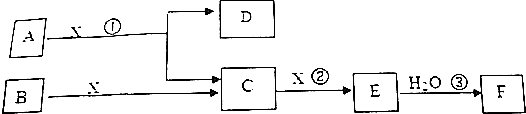
4.已知A、B、C、D、E是短周期主族元素,原子序数依次增大.其中A、E的单质在常温下呈气态,B的原子最外层电子数是其电子层数的2倍,C在同周期主族元素中原子半径最大,D的周期序数与主族序数相同.下列说法正确的是( )
0 156735 156743 156749 156753 156759 156761 156765 156771 156773 156779 156785 156789 156791 156795 156801 156803 156809 156813 156815 156819 156821 156825 156827 156829 156830 156831 156833 156834 156835 156837 156839 156843 156845 156849 156851 156855 156861 156863 156869 156873 156875 156879 156885 156891 156893 156899 156903 156905 156911 156915 156921 156929 203614
| A. | B位于元素周期表中第二周期第ⅥA族 | |
| B. | 工业上可以用电解CE溶液的方法同时获得C、E单质 | |
| C. | C、D的最高价氧化物对应的水化物之间能发生化学反应 | |
| D. | 化合物AE与CE具有相同类型的化学键 |
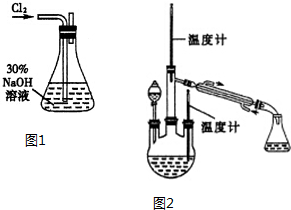 肼是重要的化工原料.某探究小组利用下列反应制取水合肼(N2H4•H20).
肼是重要的化工原料.某探究小组利用下列反应制取水合肼(N2H4•H20).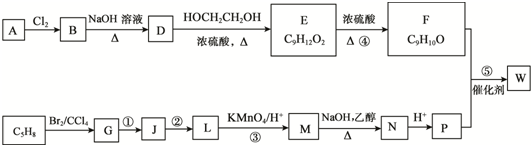
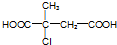 .
. (R1~R4表示烃基)
(R1~R4表示烃基) .
. .
. .
. .
.