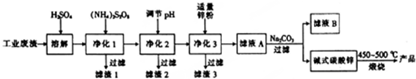
16.活性氧化锌是一种多功能性的新型无机材料,其颗粒大小在1~100nm,利用某工业废液(含有ZnO、FeO、FeO2、CuO、MnO)制备超细活性氧化锌的工艺流程如图所示.
有关氢氧化物开始沉淀和完全沉淀的pH如表.
回答下列问题:
(1)净化1的目的之一是将Mn2+转化为MnO2而除去,此过程中(NH4)2SrO2作氧化剂(填“氧化剂”会“还原剂”),已知该反应中Sr${O}_{4}^{2-}$会转化为${SO}_{4}^{2-}$,若反应生成1molMnO2,则会消耗1mol (NH4)2SrO2.
(2)滤渣2的主要成分有两种,分别为Fe(OH)3和Al(OH)3,滤液B的溶质主要为Na2SO4.(填化学式).
(3)净化2应调节溶液pH的范围是5.2~5.4,调节pH可选用的试剂为ad(填字母).
a.ZnO b.CaO c.CaCO3 d.ZnCO3
(4)碱式碳酸锌在煅烧前需要洗涤烘干,检验碱式碳酸锌是否洗涤干净的操作方法是取少许最后一次洗涤液于试管中,滴加硝酸钡溶液,若无白色沉淀生成,则洗涤干净,否则未洗涤干净.
(5)煅烧碱式碳酸锌【ZnCO3•2Zn(OH)2•H2O】的化学方程式为ZnCO3•2Zn(OH)•2H2O$\frac{\underline{\;450~500℃\;}}{\;}$3ZnO+CO2↑+3H2O↑.

有关氢氧化物开始沉淀和完全沉淀的pH如表.
| 氢氧化物 | Fe(OH)3 | Fe(OH)2 | Cu(OH)2 | Al(OH)2 | Zn(OH)2 |
| 开始沉淀时的pH | 2.7 | 7.5 | 5.4 | 4.0 | 6.4 |
| 完全沉淀时的pH | 3.7 | 9.5 | 6.6 | 5.2 | 8.0 |
(1)净化1的目的之一是将Mn2+转化为MnO2而除去,此过程中(NH4)2SrO2作氧化剂(填“氧化剂”会“还原剂”),已知该反应中Sr${O}_{4}^{2-}$会转化为${SO}_{4}^{2-}$,若反应生成1molMnO2,则会消耗1mol (NH4)2SrO2.
(2)滤渣2的主要成分有两种,分别为Fe(OH)3和Al(OH)3,滤液B的溶质主要为Na2SO4.(填化学式).
(3)净化2应调节溶液pH的范围是5.2~5.4,调节pH可选用的试剂为ad(填字母).
a.ZnO b.CaO c.CaCO3 d.ZnCO3
(4)碱式碳酸锌在煅烧前需要洗涤烘干,检验碱式碳酸锌是否洗涤干净的操作方法是取少许最后一次洗涤液于试管中,滴加硝酸钡溶液,若无白色沉淀生成,则洗涤干净,否则未洗涤干净.
(5)煅烧碱式碳酸锌【ZnCO3•2Zn(OH)2•H2O】的化学方程式为ZnCO3•2Zn(OH)•2H2O$\frac{\underline{\;450~500℃\;}}{\;}$3ZnO+CO2↑+3H2O↑.
10.氯气和盐酸分别与铁反应,每个铁原子失去的电子数是( )
| A. | 前者大于后者 | B. | 前者小于后者 | C. | 相等 | D. | 不能确定 |
9.下列有关物质除杂的方法中可行的是( )
0 156717 156725 156731 156735 156741 156743 156747 156753 156755 156761 156767 156771 156773 156777 156783 156785 156791 156795 156797 156801 156803 156807 156809 156811 156812 156813 156815 156816 156817 156819 156821 156825 156827 156831 156833 156837 156843 156845 156851 156855 156857 156861 156867 156873 156875 156881 156885 156887 156893 156897 156903 156911 203614
| A. | 除去石英中混有的少量铝粉,可加入氢氧化钠溶液溶解后过滤 | |
| B. | 向含少量FeBr2的FeCl2溶液中,加入适量氯水,再加CCl4萃取,以除去FeCl2溶液中的FeBr2 | |
| C. | 除去乙酸乙酯中混有的少量乙酸,加入饱和氢氧化钠溶液振荡后分液 | |
| D. | 除去CuCl2溶液中混有的少量FeCl3,可向溶液中加入CuO后再过滤 |
 如图所示装置中,甲、乙、丙三个烧杯依次分别盛放足量的NaCl溶液、AgNO3溶液、x溶液,a、b、c、d电极均为石墨电极.接通电源,经过一段时间后,乙中c电极质量增加.据此回答问题:
如图所示装置中,甲、乙、丙三个烧杯依次分别盛放足量的NaCl溶液、AgNO3溶液、x溶液,a、b、c、d电极均为石墨电极.接通电源,经过一段时间后,乙中c电极质量增加.据此回答问题: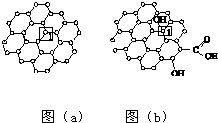 石墨烯[如图(a)所示]是一种由单层碳原子构成的平面结构新型碳材料,石墨烯中部分碳原子被氧化后,其平面结构会发生改变,转化为氧化石墨烯[如图(b)所示].
石墨烯[如图(a)所示]是一种由单层碳原子构成的平面结构新型碳材料,石墨烯中部分碳原子被氧化后,其平面结构会发生改变,转化为氧化石墨烯[如图(b)所示].