17.某化合物由两种单质直接反应生成,将其加(通)入Ba(HCO3)2溶液中同时有气体和沉淀产生.下列化合物中符合上述条件的是( )
| A. | SO3 | B. | HCl | C. | FeCl2 | D. | Na2O2 |
15.下列说法不正确的是( )
| A. | 煤的液化是在一定条件下使煤和氢气作用,把煤转化成液体燃料的过程 | |
| B. | 石油中含有C5~C12的烷烃,可以通过石油的分馏得到汽油 | |
| C. | 蒙古牧民喜欢用银器盛放鲜牛奶有其科学道理:用银器盛放鲜牛奶,溶入的极微量的银离子,可杀死牛奶中的细菌,防止牛奶变质 | |
| D. | 检验淀粉水解产物中有没有葡萄糖,可以在水解后的溶液中直接加新制氢氧化铜来检验 |
14.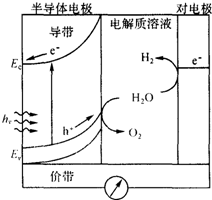 太阳能发电和阳光分解水制氢气,是清洁能源研究的主攻方向,研究工作之一集中在n-型半导体光电化学电池方面.如图是n-型半导体光电化学电池光解水制氢的基本原理示意图,图中的半导体导带是未充填电子的能级最低的能带,半导体价带是已充填价电子的能级最高的能带,图中的e-为电子、h+为空穴.在光照下,电子(e-)由价带跃迁到导带后,然后流向对电极.下列说法不正确的是( )
太阳能发电和阳光分解水制氢气,是清洁能源研究的主攻方向,研究工作之一集中在n-型半导体光电化学电池方面.如图是n-型半导体光电化学电池光解水制氢的基本原理示意图,图中的半导体导带是未充填电子的能级最低的能带,半导体价带是已充填价电子的能级最高的能带,图中的e-为电子、h+为空穴.在光照下,电子(e-)由价带跃迁到导带后,然后流向对电极.下列说法不正确的是( )
 太阳能发电和阳光分解水制氢气,是清洁能源研究的主攻方向,研究工作之一集中在n-型半导体光电化学电池方面.如图是n-型半导体光电化学电池光解水制氢的基本原理示意图,图中的半导体导带是未充填电子的能级最低的能带,半导体价带是已充填价电子的能级最高的能带,图中的e-为电子、h+为空穴.在光照下,电子(e-)由价带跃迁到导带后,然后流向对电极.下列说法不正确的是( )
太阳能发电和阳光分解水制氢气,是清洁能源研究的主攻方向,研究工作之一集中在n-型半导体光电化学电池方面.如图是n-型半导体光电化学电池光解水制氢的基本原理示意图,图中的半导体导带是未充填电子的能级最低的能带,半导体价带是已充填价电子的能级最高的能带,图中的e-为电子、h+为空穴.在光照下,电子(e-)由价带跃迁到导带后,然后流向对电极.下列说法不正确的是( )| A. | 对电极表面发生的电极反应式为:4H++4e-→2H2 | |
| B. | 电池的总反应式为:2H2O$\stackrel{hv}{→}$O2+2H2↑ | |
| C. | 整个过程中实现了太阳能向电能化学能等的转化 | |
| D. | 装置中电流的方向是从半导体电极流向对电极 |
13.下列说法正确的是( )
| A. | 重结晶是利用混合物中各组分在某种溶剂中的溶解度不同而使它们相互分离的方法 | |
| B. | 蒸馏时,如果温度计水银球的位置偏高,会导致得到的馏分的沸点偏低 | |
| C. | 在氢氧化镁悬浊液中加入氯化铵溶液,悬浊液溶解证明了氯化铵溶液水解呈酸性 | |
| D. | 用标准NaOH溶液滴定待测食醋溶液时,锥形瓶水洗后未用待测液润洗,碱式滴定管尖嘴部分有气泡,滴定后气泡消失,则测定结果偏低 |
12.下列说法正确的是( )
| A. | 标准状况下,将2.24L Cl2溶于水,可得到HClO分子的数目是0.1NA | |
| B. | NA个Fe(OH)3胶体粒子的质量为107g | |
| C. | 8.0gCu2S和CuO的混合物中含有铜原子数为0.1NA | |
| D. | 2.3gNa与氧气完全反应,反应中转移的电子数介于0.1NA到0.2NA之间 |
11.化学与生活、社会发展息息相关,下列有关说法不正确的是( )
| A. | “霾尘积聚难见路人”,雾霾所形成的气溶胶有丁达尔效应 | |
| B. | “熬胆矾铁釜,久之亦化为铜”,该过程发生了置换反应 | |
| C. | “玉不琢不成器”,“百炼方能成钢”发生的均为化学变化 | |
| D. | 古剑“沈卢”“以剂钢为刃,柔铁为茎干,不尔则多断折”,剂钢指的是铁的合金 |
10.短周期主族元素X、Y、Z、W的原子序数依次增大.Y原子最外层电子数是内层电子数的3倍,X与Z位于同一主族,且与Y不在同一周期,W元素的最高正化合价与最低负化合价的代数和为零,下列说法正确的是( )
| A. | Y的气态氢化物的沸点在同主族中最高,所以其气态氢化物最稳定 | |
| B. | Y、W形成的化合物与Y、Z形成的化合物中所含化学键相同 | |
| C. | 简单离子半径:Z>Y | |
| D. | 单质的氧化性:Y>W |
9.设NA为阿伏加德罗常数的值,下列叙述不正确的是( )
0 156688 156696 156702 156706 156712 156714 156718 156724 156726 156732 156738 156742 156744 156748 156754 156756 156762 156766 156768 156772 156774 156778 156780 156782 156783 156784 156786 156787 156788 156790 156792 156796 156798 156802 156804 156808 156814 156816 156822 156826 156828 156832 156838 156844 156846 156852 156856 156858 156864 156868 156874 156882 203614
| A. | 46g乙醇中存在的共价键总数为8NA | |
| B. | 0.5 mol•L-1 CuCl2溶液中含有的Cl-个数为NA | |
| C. | 标准状况下,H2和CO混合气体8.96L在足量O2中充分燃烧消耗O2分子数为0.2NA | |
| D. | 在反应4Cl2+8NaOH═6NaCl+NaClO+NaClO3+4H2O中,消耗1mol Cl2时转移的电子总数为1.5NA |
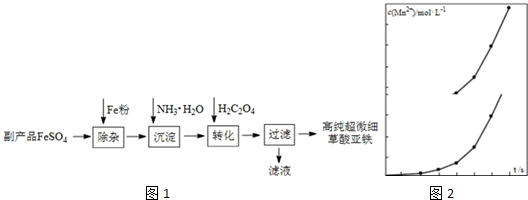
 .
. +nH2O.
+nH2O.