1.无水硫酸亚铁是白色粉末,溶于水,水溶液为浅绿色,常见其七水合物(绿矾FeSO4•7H2O ),在潮湿空气中易氧化成难溶于水的棕黄色碱式硫酸铁Fe(OH)SO4.主要用于净水、照相制版及治疗缺铁性贫血等.
某化学兴趣小组欲确定某FeSO4•7H2O样品加热后的产物,实验步骤如下:
①检查装置的气密性;②称取2.78g样品,置于B试管中;③打开活塞K,从C处通入某种气体;④关闭K,对试管B充分加热;⑤打开活塞K,从C处再通入该气体.
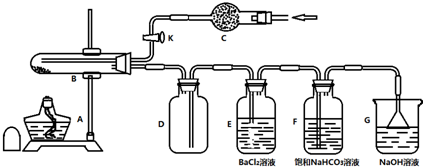
(1)E中产生白色沉淀,说明FeSO4•7H2O分解有SO3生成.
(2)步骤③中从C处通入的气体作用为将装置中的空气全部赶出,并将FeSO4•7H2O的分解产物全部排出,该气体可以为C.
A.SO2 B.Cl2 C.N2 D.NH3
若不通入气体,则E中发生的副反应为2SO2+O2+2BaCl2+2H2O=2BaSO4↓+4HCl.
(3)甲同学将F中反应后溶液共100mL取出,用0.020mol•L-1的酸性KMnO4溶液进行滴定,KMnO4溶液应盛装在酸式滴定管中.滴定过程中反应的离子方程式为:2MnO4-+5SO32-+6H+=2Mn2++5SO42-+3H2O;滴定完毕,三次实验记录KMnO4标准溶液的读数如下:
通过计算,甲同学认为B中的固体产物化学式为Fe2O3.
(4)设计实验证明FeSO4•7H2O水溶液呈酸性的原因是Fe2+的水解:取少量FeSO4•7H2O水溶液于试管中,先加Fe粉,再滴入几滴石蕊试液,试管中溶液微红,然后加热试管中的溶液,若溶液红色加深,则说明FeSO4•7H2O水溶液呈酸性的原因是Fe2+的水解.
某化学兴趣小组欲确定某FeSO4•7H2O样品加热后的产物,实验步骤如下:
①检查装置的气密性;②称取2.78g样品,置于B试管中;③打开活塞K,从C处通入某种气体;④关闭K,对试管B充分加热;⑤打开活塞K,从C处再通入该气体.

(1)E中产生白色沉淀,说明FeSO4•7H2O分解有SO3生成.
(2)步骤③中从C处通入的气体作用为将装置中的空气全部赶出,并将FeSO4•7H2O的分解产物全部排出,该气体可以为C.
A.SO2 B.Cl2 C.N2 D.NH3
若不通入气体,则E中发生的副反应为2SO2+O2+2BaCl2+2H2O=2BaSO4↓+4HCl.
(3)甲同学将F中反应后溶液共100mL取出,用0.020mol•L-1的酸性KMnO4溶液进行滴定,KMnO4溶液应盛装在酸式滴定管中.滴定过程中反应的离子方程式为:2MnO4-+5SO32-+6H+=2Mn2++5SO42-+3H2O;滴定完毕,三次实验记录KMnO4标准溶液的读数如下:
| 滴定次数实验数据 | 1 | 2 | 3 |
| V(样品)/mL | 20.00 | 20.00 | 20.00 |
| V(KMnO4)/mL(初读数) | 1.50 | 0.20 | 0.00 |
| V(KMnO4)/mL(终读数) | 19.85 | 20.22 | 19.98 |
(4)设计实验证明FeSO4•7H2O水溶液呈酸性的原因是Fe2+的水解:取少量FeSO4•7H2O水溶液于试管中,先加Fe粉,再滴入几滴石蕊试液,试管中溶液微红,然后加热试管中的溶液,若溶液红色加深,则说明FeSO4•7H2O水溶液呈酸性的原因是Fe2+的水解.
20.某有机物M的结构简式如图所示,下列说法正确的是( )
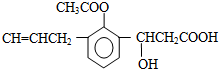

| A. | M中至少有8个碳原子共面 | |
| B. | M能发生还原、氧化、中和、缩聚、取代、加成、银镜等反应 | |
| C. | M中苯环上的一氯取代物有两种不同的结构 | |
| D. | 1molM消耗Na、NaOH、NaHCO3的物质的量的比是2:2:1 |
19.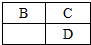 A、B、C、D、E均为短周期主族元素,B、C、D在周期表中的位置关系如图所示,A是短周期中原子半径最小的元素,A、B、C三种元素的原子序数之和等于D元素的原子序数,E是短周期中最活泼的金属元素.下列说法错误的是( )
A、B、C、D、E均为短周期主族元素,B、C、D在周期表中的位置关系如图所示,A是短周期中原子半径最小的元素,A、B、C三种元素的原子序数之和等于D元素的原子序数,E是短周期中最活泼的金属元素.下列说法错误的是( )
 A、B、C、D、E均为短周期主族元素,B、C、D在周期表中的位置关系如图所示,A是短周期中原子半径最小的元素,A、B、C三种元素的原子序数之和等于D元素的原子序数,E是短周期中最活泼的金属元素.下列说法错误的是( )
A、B、C、D、E均为短周期主族元素,B、C、D在周期表中的位置关系如图所示,A是短周期中原子半径最小的元素,A、B、C三种元素的原子序数之和等于D元素的原子序数,E是短周期中最活泼的金属元素.下列说法错误的是( )| A. | 氢化物的稳定性:B>D | B. | 简单离子的半径大小:D>E>C | ||
| C. | 简单阴离子的还原性:C<D | D. | A、B、C可形成离子化合物 |
18.某同学做同主族元素性质的相似性和递变性实验时,自己设计了一套实验方案,并记录了有关实验现象(见表,表中的“实验方案”与“实验现象”前后不一定是对应关系).
请你帮助该同学整理并完成实验报告.
(1)实验目的:探究同主族元素性质的相似性和递变性.
(2)实验用品:①试剂:金属钠、金属钾、新制氯水、溴水、0.1mol•L-1NaBr溶液、0.1mol•L-1NaI溶液、CCl4溶液等.
②仪器:试管、烧杯、胶头滴管、镊子、小刀、玻璃片等.
(3)实验内容(请把表中与实验方案对应的实验现象的标号和化学方程式补写完整):
(4)实验结论:同主族元素性质相似,自上而下元素金属性增强,非金属性减弱.
| 实验方案 | 实验现象 |
| ①将新制氯水滴加到NaBr溶液中,振荡后加入适量CCl4溶液,振荡,静置 | A.浮在水面上,熔成小球,四处游动,随后消失 |
| ②将一小块金属钠放入冷水中 | B.分层,上层无色,下层紫色 |
| ③将溴水滴加到NaI溶液中,振荡后加入适量CCl4溶液,振荡,静置 | C.浮在水面上,熔成小球,四处游动,并伴有轻微的爆炸声,很快消失 |
| ④将一小块金属钾放入冷水中 | D.分层,上层无色,下层红棕色 |
(1)实验目的:探究同主族元素性质的相似性和递变性.
(2)实验用品:①试剂:金属钠、金属钾、新制氯水、溴水、0.1mol•L-1NaBr溶液、0.1mol•L-1NaI溶液、CCl4溶液等.
②仪器:试管、烧杯、胶头滴管、镊子、小刀、玻璃片等.
(3)实验内容(请把表中与实验方案对应的实验现象的标号和化学方程式补写完整):
| 实验方案 | 实验现象 | 化学方程式 |
| ① | D | Cl2+2NaBr═2NaCl+Br2 |
| ② | A | 2Na+2H2O═2NaOH+H2↑ |
| ③ | B | Br2+2NaI═2NaBr+I2 |
| ④ | C | 2K+2H2O═2KOH+H2↑ |
17.现有A、B、C、D、E五种易溶于水的强电解质,它们由如下离子组成(各种离子不重复).
已知:①0.1mol/L A溶液中c(H+)>0.1mol/L;
②B溶液与其它四种溶液反应,均能产生沉淀;
③向C溶液中逐滴加入B溶液,有白色沉淀生成,当B溶液过量时,沉淀完全溶解.
回答下列问题:
(1)写出下列物质的化学式:AH2SO4、BBa(OH)2.
(2)D、E两种物质中必有一种是NH4HCO3,写出将少量该物质的稀溶液滴加到0,1mol/L B溶液中反应的离子方程式Ba2++2OH-+NH4++HCO3-=BaCO3↓+NH3H2O+H2O.
(3)用铝粉可除去废水中的NO3-.在pH为10.7左右的溶液中,加入铝粉除去NO3-,同时产生物质的量之比为1﹕1的氨气和氮气,该反应的还原产物是NH3、N2,除去0.1mol NO3-,要消耗铝5.4g,其对应离子方程式为6Al+3NO3-+3OH-=6AlO2-+NH3↑+N2↑.
| 阳离子 | H+、NH4+、Mg2+、Ba2+、Al3+ |
| 阴离子 | OH-、Cl-、HCO3-、NO3-、SO42- |
②B溶液与其它四种溶液反应,均能产生沉淀;
③向C溶液中逐滴加入B溶液,有白色沉淀生成,当B溶液过量时,沉淀完全溶解.
回答下列问题:
(1)写出下列物质的化学式:AH2SO4、BBa(OH)2.
(2)D、E两种物质中必有一种是NH4HCO3,写出将少量该物质的稀溶液滴加到0,1mol/L B溶液中反应的离子方程式Ba2++2OH-+NH4++HCO3-=BaCO3↓+NH3H2O+H2O.
(3)用铝粉可除去废水中的NO3-.在pH为10.7左右的溶液中,加入铝粉除去NO3-,同时产生物质的量之比为1﹕1的氨气和氮气,该反应的还原产物是NH3、N2,除去0.1mol NO3-,要消耗铝5.4g,其对应离子方程式为6Al+3NO3-+3OH-=6AlO2-+NH3↑+N2↑.
16.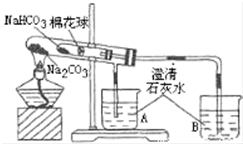 某小组同学通过对比实验了解Na2CO3和NaHCO3性质的异同,如表是他们撰写的实验报告的一部分.
某小组同学通过对比实验了解Na2CO3和NaHCO3性质的异同,如表是他们撰写的实验报告的一部分.
(1)请帮助该小组同学完成实验报告中放入内容有无水硫酸铜粉末的棉花球变蓝,A烧杯中没有明显现象,B烧杯中有白色沉淀生成.
(2)已知:20℃时Na2CO3的溶解度为20.5g.由实验②(填实验序号)现象可知,20℃时NaHCO3的溶解度小于20.5g;如果向饱和Na2CO3溶液中不断通入CO2气体,现象是白色晶体析出,化学方程式是Na2CO3+CO2+H2O=2NaHCO3↓.
(3)由实验④可以得出结论是碳酸钠的稳定性强于碳酸氢钠,用化学方程式说明得出结论的原因2NaHCO3$\frac{\underline{\;\;△\;\;}}{\;}$Na2CO3+CO2↑+H2O.
 某小组同学通过对比实验了解Na2CO3和NaHCO3性质的异同,如表是他们撰写的实验报告的一部分.
某小组同学通过对比实验了解Na2CO3和NaHCO3性质的异同,如表是他们撰写的实验报告的一部分. | 实验序号 | 实验步骤(内容) | 现象 |
| ① | 在贴有标签a、b的试管中分别加入1.0gNa2CO3固体和NaHCO3固体,观察外观. | / |
| ② | 继续向两试管中分别加入10.0mL水,用力振荡,观察现象. | / |
| ③ | 再分别向两试管中滴加2滴酚酞溶液,观察现象. | 溶液变红 |
| ④ | 加热大试管一段时间.(注:棉花球沾有无水硫酸铜粉末) | 有无水硫酸铜粉末的棉花球变蓝,A烧杯中没有明显现象,B烧杯中有白色沉淀生成 |
(2)已知:20℃时Na2CO3的溶解度为20.5g.由实验②(填实验序号)现象可知,20℃时NaHCO3的溶解度小于20.5g;如果向饱和Na2CO3溶液中不断通入CO2气体,现象是白色晶体析出,化学方程式是Na2CO3+CO2+H2O=2NaHCO3↓.
(3)由实验④可以得出结论是碳酸钠的稳定性强于碳酸氢钠,用化学方程式说明得出结论的原因2NaHCO3$\frac{\underline{\;\;△\;\;}}{\;}$Na2CO3+CO2↑+H2O.
14.铁在冷的浓硫酸中能发生钝化.某兴趣小组的同学发现将一定量的铁与浓硫酸加热时,观察到铁完全溶解,并产生大量气体.实验室现有下列试剂:0.01mol/L 酸性KMnO4溶液、0.1mol/L KI溶液、3%H2O2溶液、淀粉溶液、蒸馏水.请你协助他们探究所得溶液和气体的成分.
【提出猜想】
Ⅰ.所得溶液中的金属离子可能含有Fe2+和Fe3+中的一种或两种;
Ⅱ.所得气体中可能含有SO2、H2中的一种或两种.
【实验探究】
【问题讨论】
有同学提出,若另外选用KSCN溶液,则仅利用KSCN和H2O2两种溶液即可完成猜想Ⅰ的所有探究,判断该方法是否正确并进行评价:不正确,若溶液中含有Fe3+,则无法检验溶液中是否含有Fe2+.
【提出猜想】
Ⅰ.所得溶液中的金属离子可能含有Fe2+和Fe3+中的一种或两种;
Ⅱ.所得气体中可能含有SO2、H2中的一种或两种.
【实验探究】
| 实验操作 | 预期现象 | 结论 | |
| 验证猜想Ⅰ | 步骤①:取少量0.01mol/L酸性KMnO4溶液,滴入所得溶液 | 溶液紫红色褪去 | 含有Fe2+(或溶液紫红色不褪去,不含Fe2+) |
| 步骤②:另取少量所得溶液,滴加KI-淀粉溶液 | 含有Fe3+ | ||
| 验证猜想Ⅱ | 将所得气体通入如图装置: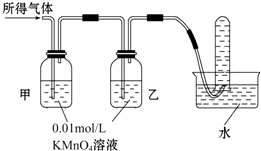 | 甲中KMnO4溶液褪色,乙中KMnO4溶液颜色不变,试管中收集到气体 | 含有两种气体 |
有同学提出,若另外选用KSCN溶液,则仅利用KSCN和H2O2两种溶液即可完成猜想Ⅰ的所有探究,判断该方法是否正确并进行评价:不正确,若溶液中含有Fe3+,则无法检验溶液中是否含有Fe2+.
13.设NA代表阿伏加德罗常数的数值,下列说法正确的是( )
0 156684 156692 156698 156702 156708 156710 156714 156720 156722 156728 156734 156738 156740 156744 156750 156752 156758 156762 156764 156768 156770 156774 156776 156778 156779 156780 156782 156783 156784 156786 156788 156792 156794 156798 156800 156804 156810 156812 156818 156822 156824 156828 156834 156840 156842 156848 156852 156854 156860 156864 156870 156878 203614
| A. | 在标准状况下,NA个水分子所占的体积约为22.4L | |
| B. | 5.6g铁与氯气完全反应,失去电子的数目为0.2NA | |
| C. | 1 mol Na2O2与足量CO2充分反应,转移的电子数为2NA | |
| D. | 在标准状况下,22.4L由N2、N2O组成的混合气体中所含的氮原子数为2NA |
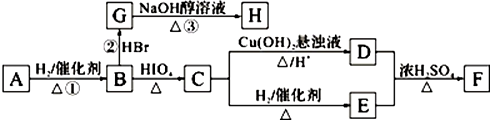
 .
. .
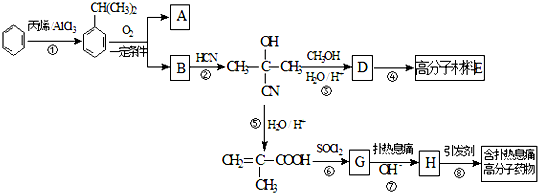
.
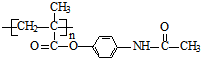 .
.
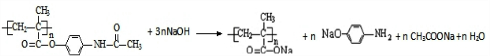
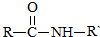 $\stackrel{Na溶液}{→}$RCOONa+R′-NH2
$\stackrel{Na溶液}{→}$RCOONa+R′-NH2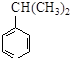 可转化为1mol A和1mol B,且A与FeCl3溶液作用显紫色,写出A的稀溶液与过量浓溴水发生反应的化学方程式
可转化为1mol A和1mol B,且A与FeCl3溶液作用显紫色,写出A的稀溶液与过量浓溴水发生反应的化学方程式 .
.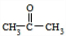 ;扑热息痛的结构简式为
;扑热息痛的结构简式为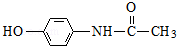 .
. .
.