17.设NA为阿伏加德罗常数的值,下列说法不正确的是( )
| A. | 标准状况下,22.4L乙醇含有2NA个碳子 | |
| B. | 常温常压下,17g羟基含有9NA个电子 | |
| C. | 28g乙烯和丙烯(C3H6)的混合气体中含有的碳原子数为2NA | |
| D. | 1molNa被完全氧化生成Na2O2,失去NA个电子 |
16.下列说法正确的是( )
| A. | 混合浓硫酸和乙醇时,应将乙醇慢慢注入到浓硫酸中 | |
| B. | 萃取、配制物质的量浓度的溶液都要用到玻璃棒 | |
| C. | 用丁达尔效应可鉴别溶液和胶体 | |
| D. | 可用氢氧化钠溶液除去乙酸乙酯中混有的乙酸 |
15.下列说法中不正确的是( )
| A. | SO2可以漂白纸浆和草帽辫 | |
| B. | 单质硅可用做半导体材料 | |
| C. | 小苏打可作食品的膨松剂 | |
| D. | 合成纤维和光导纤维都是新型无机非金属材料 |
14.已知正四面体形分子E和直线型分子F反应,生成四面体形分子L和直线型分子M.(组成E分子的元素的原子序数小于10,组成F分子的元素为第三周期的元素.)如图,则下列判断中正确的是 ( )
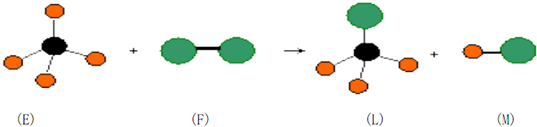

| A. | 常温常压下,L是一种液态有机物 | B. | E中化学键是极性键 | ||
| C. | F具有漂白性 | D. | 上述反应的类型是取代反应 |
13.设NA为阿伏加德罗常数的数值.下列叙述正确的是( )
| A. | 1.7g的OH-中含有的电子数为NA | |
| B. | 常温常压下,1.12LO2中所含氧原子数为NA | |
| C. | 0.1molNa2O2中含O2-数为0.2NA | |
| D. | 1L1mol/LH2SO4中,含有总离子数为3NA |
12.某学生对碱性工业废水样品进行研究,其实验操作或结论的描述,正确的是( )
| A. | 将废水加入紫色石蕊试剂中检验酸碱性 | |
| B. | 用玻璃棒蘸取废水样品,蘸在润湿的pH试纸上测定其pH | |
| C. | 测得该废水样品的pH=10,则废水样品中c(OH-)=10-10 mol/L | |
| D. | 该工业废水中c(H+)<c(OH-) |
11.下列化学用语中,说法正确的是( )
| A. | CO2分子的结构式O-C-O | B. | 乙醇的分子式C2H6O | ||
| C. | Mg2+结构示意图 | D. | NaCl的电子式 |
9.用NA表示阿伏加德罗常数的值.下列叙述正确的是( )
| A. | 1mol/LNaCl溶液含有NA个Na+ | |
| B. | 任意条件下,16gO3所含的原子数为NA | |
| C. | 1molFe与足量稀HNO3反应,转移3NA个电子 | |
| D. | 标准状况下,22.4LSO3所含的分子数为NA |
8.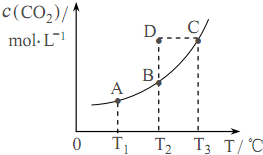 在密闭容器中存在下列平衡:CO(g)+H2O(g)?CO2(g)+H2(g);CO2(g)的平衡物质的量浓度c(CO2)与温度T的关系如图所示.下列说法正确的是( )
在密闭容器中存在下列平衡:CO(g)+H2O(g)?CO2(g)+H2(g);CO2(g)的平衡物质的量浓度c(CO2)与温度T的关系如图所示.下列说法正确的是( )
0 156669 156677 156683 156687 156693 156695 156699 156705 156707 156713 156719 156723 156725 156729 156735 156737 156743 156747 156749 156753 156755 156759 156761 156763 156764 156765 156767 156768 156769 156771 156773 156777 156779 156783 156785 156789 156795 156797 156803 156807 156809 156813 156819 156825 156827 156833 156837 156839 156845 156849 156855 156863 203614
 在密闭容器中存在下列平衡:CO(g)+H2O(g)?CO2(g)+H2(g);CO2(g)的平衡物质的量浓度c(CO2)与温度T的关系如图所示.下列说法正确的是( )
在密闭容器中存在下列平衡:CO(g)+H2O(g)?CO2(g)+H2(g);CO2(g)的平衡物质的量浓度c(CO2)与温度T的关系如图所示.下列说法正确的是( )| A. | 平衡状态A与C相比,平衡状态A的c(CO)小 | |
| B. | 在T2时,若反应处于状态D,则一定有V正<V逆 | |
| C. | 反应CO(g)+H2O(g)?CO2(g)+H2(g)的△H<0 | |
| D. | 若T1、T2时的平衡常数分别为K1、K2,则K1<K2 |
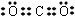 ;
;