15.设NA为阿伏加德罗常数的6值,下列说法正确的是( )
| A. | 常温常压下,16 g O2和32g O3的混合物中,含有O原子数目为3NA | |
| B. | 标准状况下,1 mol Na2O和1 mol Na2O2的混合物中,含有离子总数为7NA | |
| C. | 1 mol NaBH4中离子键的数目为2NA | |
| D. | 在K35ClO3+6H37Cl═KCl+3Cl2↑+3H2O中,若生成71 g Cl2,转移的电子数目为$\frac{5}{3}$NA |
12.已知在温度低于570℃时,还原铁粉与水蒸气反应的产物是FeO,高于570℃时,生成Fe3O4.老师用如图所示实验装置,完成了还原铁粉与水蒸气反应的演示实验.
甲同学为探究实验后试管内的固体含有哪些物质,进行了下列实验:( )
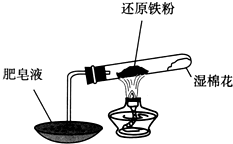
甲同学为探究实验后试管内的固体含有哪些物质,进行了下列实验:( )

| 实验编号 | 实验操作 | 实验现象 |
| ① | 取少量黑色粉末放入试管1中,加入盐酸,微热 | 黑色粉末逐渐溶解,溶液呈浅绿色;有少量气泡产生 |
| ② | 向试管1中滴加几滴KSCN溶液,振荡 | 溶液没有出现血红色 |
| A. | 试管内的固体一定含有铁粉 | |
| B. | 试管内的固体一定不含有Fe3O4 | |
| C. | 不能确定试管内的固体一定含有FeO | |
| D. | 可通过将试管内固体彻底还原,分析其质量减小的方法来确定是否含有Fe3O4 |
11.甲、乙、丙、丁4种物质分别含2 种或3 种元素,它们的分子中均含18个电子.甲是气态氢化物,在水中分步电离出两种阴离子.下列推断合理的是( )
| A. | 某钠盐溶液含甲电离出的阴离子,则该溶液显碱性,只能与酸反应 | |
| B. | 乙与氧气的摩尔质量相同,则乙一定含有极性键和非极性键 | |
| C. | 丙中含有第2周期ⅣA 族的元素,则丙可能是甲烷的卤代物 | |
| D. | 丁和甲中各元素质量比相同,则丁可能是C2H2 |
10.用NA表示阿伏加德罗常数,下列说法正确的是( )
| A. | 1.8g重水(D2O)中含有的中子数为NA | |
| B. | 1molCl2参加氧化还原反应,转移的电子数一定为2NA | |
| C. | T℃时pH=6的纯水中,含有10-6 NA个OH- | |
| D. | 电解精炼铜时,若转移NA个电子,阴极析出32 g铜 |
8.现有a mol/L 的NaX和b mol/L的NaY两种盐溶液.下列说法正确的是( )
0 156661 156669 156675 156679 156685 156687 156691 156697 156699 156705 156711 156715 156717 156721 156727 156729 156735 156739 156741 156745 156747 156751 156753 156755 156756 156757 156759 156760 156761 156763 156765 156769 156771 156775 156777 156781 156787 156789 156795 156799 156801 156805 156811 156817 156819 156825 156829 156831 156837 156841 156847 156855 203614
| A. | 若a=b且c(X-)=c(Y-)+c(HY),则HX为强酸 | |
| B. | 若a=b且pH(NaX)>pH(NaY),则c(X-)+c(OH-)>c(Y-)+c(OH-) | |
| C. | 若a>b且c(X-)=c(Y-),则酸性HX>HY | |
| D. | 若两溶液等体积混合,则c(Na+)=(a+b) mol/L(忽略混合过程中的体积变化) |
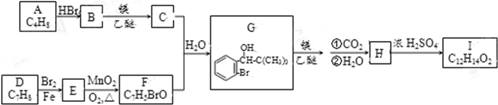
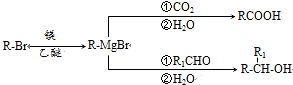
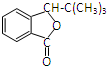 .
. .
.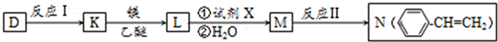
 .
.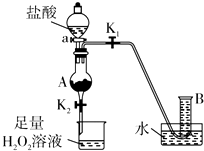 氯化铁是实验室中的重要试剂.某同学用m g含有铁锈(Fe2O3)的废铁屑来制取FeCl3•6H2O晶体,同时测定废铁屑中铁的质量分数,为此设计了如图装置(夹持装置略,气密性已检验):
氯化铁是实验室中的重要试剂.某同学用m g含有铁锈(Fe2O3)的废铁屑来制取FeCl3•6H2O晶体,同时测定废铁屑中铁的质量分数,为此设计了如图装置(夹持装置略,气密性已检验):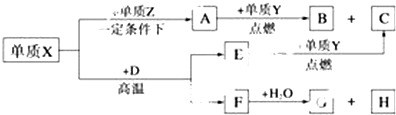
 ,A的电子式
,A的电子式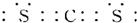 .
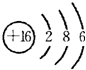
. 铜、镓、硒、硅等元素的化合物是生产第三代太阳能电池的重要材料.请回答:
铜、镓、硒、硅等元素的化合物是生产第三代太阳能电池的重要材料.请回答: