17. 已知X、Y、Z、R、Q为周期表中原子序数依次增大的前36号元素.相关信息如下:
已知X、Y、Z、R、Q为周期表中原子序数依次增大的前36号元素.相关信息如下:
请回答下列问题:
(1)YX3中心原子的杂化轨道类型是sp3,离子化合物YX5的电子式是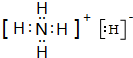 .
.
(2)CO与Y2属于等电子体,1 个CO分子中含有的π键数目是2个.
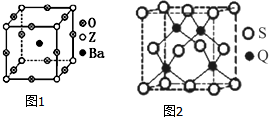
(3)工业上利用ZO2和碳酸钡在熔融状态下制取化合物A(A可看做一种含氧酸盐).A晶体的晶胞为正方体(如图1).
①制备A的化学反应方程式是TiO2+BaCO3═BaTiO3+CO2↑;
②在A晶体中,Z的配位数为6;
③在A晶体中,若将Z元素置于立方体的体心,Ba元素置于立方体的顶点,则O元素处于立方体的面心.
(4)R2+离子的外围电子层电子排布式为3d9.R2O的熔点比R2S的高(填“高”或“低”).
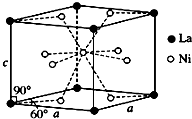
(5)Q元素和硫(S)元素能够形成化合物B.B晶体的晶胞为正方体(如图2),若晶胞棱长为540.0pm,则晶胞密度为$\frac{4×\frac{(65+32)g/mol}{6.02×1{0}^{23}mo{l}^{-1}}}{(540×1{0}^{-10}cm)^{3}}$=4.1g•cm-3(列式并计算).
 已知X、Y、Z、R、Q为周期表中原子序数依次增大的前36号元素.相关信息如下:
已知X、Y、Z、R、Q为周期表中原子序数依次增大的前36号元素.相关信息如下:| X元素是宇宙中最丰富的元素 |
| Y元素基态原子的核外p电子数比s电子数少1 |
| Z元素被誉为“太空金属”,也有“生物金属”之称,其基态原子次外层有2个未成对电子 |
| R元素在元素周期表的第十一列 |
| Q元素在周期表里与R元素在同一个分区 |
(1)YX3中心原子的杂化轨道类型是sp3,离子化合物YX5的电子式是
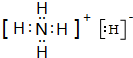 .
.(2)CO与Y2属于等电子体,1 个CO分子中含有的π键数目是2个.
(3)工业上利用ZO2和碳酸钡在熔融状态下制取化合物A(A可看做一种含氧酸盐).A晶体的晶胞为正方体(如图1).
①制备A的化学反应方程式是TiO2+BaCO3═BaTiO3+CO2↑;
②在A晶体中,Z的配位数为6;
③在A晶体中,若将Z元素置于立方体的体心,Ba元素置于立方体的顶点,则O元素处于立方体的面心.
(4)R2+离子的外围电子层电子排布式为3d9.R2O的熔点比R2S的高(填“高”或“低”).
(5)Q元素和硫(S)元素能够形成化合物B.B晶体的晶胞为正方体(如图2),若晶胞棱长为540.0pm,则晶胞密度为$\frac{4×\frac{(65+32)g/mol}{6.02×1{0}^{23}mo{l}^{-1}}}{(540×1{0}^{-10}cm)^{3}}$=4.1g•cm-3(列式并计算).
16.化学与生活密切相关.请判断下列说法是否正确(填“对”或“错”).
①纤维素作为人类的营养物质,在人体内具有重要的生理功能.对
②钢铁在潮湿的空气中被腐蚀,主要是在钢铁表面发生了电化学腐蚀的原因.对.
①纤维素作为人类的营养物质,在人体内具有重要的生理功能.对
②钢铁在潮湿的空气中被腐蚀,主要是在钢铁表面发生了电化学腐蚀的原因.对.
15.根据有机化合物的系统命名原则,下列烃的命名正确的是( )
| A. | 2-乙基戊烷 | B. | 2-甲基-1-乙基苯 | ||
| C. | 2,4,4-三甲基己烷 | D. | 3-甲基-2-丁烯 |
11.关于青蒿素和双氢青蒿素(结构如图)的下列说法中,错误的是( )
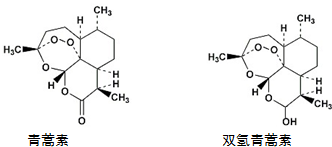

| A. | 青蒿素能发生还原反应 | |
| B. | 双氢青蒿素发生酯化反应和氧化反应 | |
| C. | 青蒿素分子中含有过氧键和酯基、醚键 | |
| D. | 双氢青蒿素分子中有2个六元环和2个七元环 |
10.下列各组离子在指定溶液中一定能大量共存的是( )
| A. | 25℃时,$\frac{c({H}^{+})}{c(O{H}^{-})}$=1×10-12溶液.Na+、SO32一、ClO-、CO32- | |
| B. | 能与金属铝反应放出氢气的溶液中:K+、Fe2+、Cl-、NO3- | |
| C. | 0.1mol/LBa (OH)2溶液中:Al3+、NH4+、NO3-、HCO3- | |
| D. | 0.1mol/L AlO2-溶液中:Na+、K+、SO32一、CO32- |
9.已知反应3SiH4(g)+4NH3(g)$\frac{\underline{\;高温\;}}{\;}$Si3N4(s)+12H2(g),相关说法不正确的是( )
| A. | NH3在该反应中作还原剂,被氧化 | |
| B. | Si3N4具有硬度大、熔点高,说明Si3N4可用作耐高温材料 | |
| C. | 标准状况下,22.4LNH3所含原子总数目为4×6.02×1023 | |
| D. | 该反应每生成1mol Si3N4转移电子总数目为12×6.02×1023 |
8.用如图所示的装置进行实验,能达到相应实验目的是( )

0 156659 156667 156673 156677 156683 156685 156689 156695 156697 156703 156709 156713 156715 156719 156725 156727 156733 156737 156739 156743 156745 156749 156751 156753 156754 156755 156757 156758 156759 156761 156763 156767 156769 156773 156775 156779 156785 156787 156793 156797 156799 156803 156809 156815 156817 156823 156827 156829 156835 156839 156845 156853 203614

| A. | 用图甲所示装置先放出水相,再放出有机相 | |
| B. | 用图乙所示装置制取少量氯气 | |
| C. | 用图丙所示装置蒸发浓缩FeCl3溶液制备纯净的FeCl3•6H2O | |
| D. | 用图丁所示装置验证光亮的铁钉在食盐水中可发生吸氧腐蚀 |
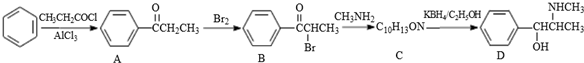
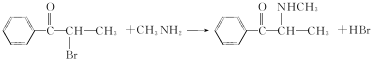 .C-D的反应类型为还原反应.
.C-D的反应类型为还原反应.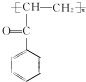 .
.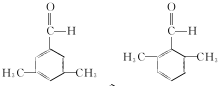 (写结构简式).
(写结构简式).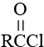 .参照上述合成路线,设计一条由苯和乙酸为起始原料制备
.参照上述合成路线,设计一条由苯和乙酸为起始原料制备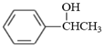 的合成路线:
的合成路线: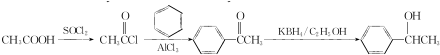 .
.
 .
. .
. )的合成路线:
)的合成路线: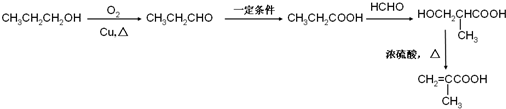 .
. 钛、铬、铁、镍、铜等金属及其化合物在工业上有重要用途.
钛、铬、铁、镍、铜等金属及其化合物在工业上有重要用途.