10.常温常压下,下列物质为液态的是( )
| A. | 白银 | B. | 白磷 | C. | 乙烯 | D. | 水银 |
9.对下列物质中锰元素化合价的判断,正确的是( )
| A. | KMnO4中为+3 | B. | MnSO4中为-2 | C. | K2MnO4中为+6 | D. | MnO2中为+2 |
8.在春暖花开的季节,广州处处鸟语花香,这里的“花香”体现的化学知识是( )
| A. | 分子是不可再分的 | B. | 分子只有在特定的季节才会运动 | ||
| C. | 分子是不停运动的 | D. | 分子只有在特定的空间才会运动 |
7.设NA为阿伏加德罗常数的值,下列叙述正确的是( )
| A. | 标准状况下,22.4L 水中所含原子总数为3NA | |
| B. | 1molNa2O2与足量CO2反应转移的电子数2NA | |
| C. | 标准状况下,44.8 L NO与22.4 LO2混合后气体中分子总数为3NA | |
| D. | 1 mol Na2O和Na2O2混合物中含有的阴、阳离子总数是3NA |
4.下列离子方程式正确的是( )
| A. | 氯化铝溶液中加入过量氨水:Al3++4NH3•H2O═[Al(OH)4]-+4NH4+ | |
| B. | MgSO4溶液中加入Ba(OH)2溶液:SO42-+Ba2+═BaSO4↓ | |
| C. | NaHCO3溶液加入少量Ca(OH)2溶液:2HCO3-+Ca2++2OH-═CaCO3↓+2H2O+CO32- | |
| D. | 硫化钠溶液显碱性:S2-+2H2O?H2S+2OH- |
3.下列有关的说法正确的是( )
| A. | 用活性炭除去冰箱中的异味是发生了化学反应 | |
| B. | 航天服主要成分是由碳化硅、陶瓷和碳纤维复合而成,它是一种新型无机非金属材料 | |
| C. | 碘是人体必需微量元素,所以要多吃富含碘化钾的食物 | |
| D. | 可以利用氯化铁溶液的酸性清除铜镜表面的铜锈 |
2.甲同学进行Fe2+还原性的实验,针对异常现象进行探究.
步骤一:制取FeCl2溶液.向0.1mol•L-1 FeCl3溶液中加足量铁粉振荡,静置后取上层清液,测得pH<1.
实验二:向1mL FeCl2溶液中滴加2滴0.1mol•L-1KSCN溶液,无现象;再滴加5滴5% H2O2溶液(物质的量浓度约为1.5mol•L-1、pH约为5),观察到溶液变红,大约10秒左右红色褪去,有气体生成(经检验为O2).
(1)用离子方程式表示步骤二中溶液变红的原因:2Fe2++H2O2+2H+═2Fe3++2H2O、Fe3++3SCN?Fe(SCN)3.
(2)甲探究步骤二中溶液褪色的原因:
Ⅰ.取褪色后溶液两份,一份滴加FeCl3溶液无现象;另一份滴加KSCN溶液出现红色;
Ⅱ.取褪色后溶液,滴加盐酸和BaCl2溶液,产生白色沉淀.
Ⅲ.向2mL 0.1mol•L-1 FeCl3溶液中滴加2滴0.1mol•L-1KSCN溶液,变红,通入O2,无明显变化.
①实验I的说明溶液红色褪去是因为SCN-发生了反应而不是Fe3+发生反应;
②实验III的目的是排除H2O2分解产生的O2氧化SCN-的可能.
得出结论:溶液褪色的原因是酸性条件下H2O2将SCN-氧化成SO42-.
(3)甲直接用FeCl2•4H2O配制0.15mol•L-1的FeCl2溶液,重复步骤二中的操作,发现液体红色并未褪去.进一步探究其原因:
Ⅰ.用激光笔分别照射红色液体和滴加了KSCN溶液的FeCl3溶液,前者有丁达尔效应,后者无.测所配FeCl2溶液的pH,约为3.由此,乙认为红色不褪去的可能原因是H2O2将Fe2+氧化为Fe3+,pH增大促进Fe3+水解形成红色Fe(OH)3胶体.
Ⅱ.查阅资料后推测,红色不褪去的原因还可能是pH较大时H2O2不能氧化SCN-.乙利用上述部分试剂,通过实验排除了这一可能.乙的实验操作及现象是:
步骤一:制取FeCl2溶液.向0.1mol•L-1 FeCl3溶液中加足量铁粉振荡,静置后取上层清液,测得pH<1.
实验二:向1mL FeCl2溶液中滴加2滴0.1mol•L-1KSCN溶液,无现象;再滴加5滴5% H2O2溶液(物质的量浓度约为1.5mol•L-1、pH约为5),观察到溶液变红,大约10秒左右红色褪去,有气体生成(经检验为O2).
(1)用离子方程式表示步骤二中溶液变红的原因:2Fe2++H2O2+2H+═2Fe3++2H2O、Fe3++3SCN?Fe(SCN)3.
(2)甲探究步骤二中溶液褪色的原因:
Ⅰ.取褪色后溶液两份,一份滴加FeCl3溶液无现象;另一份滴加KSCN溶液出现红色;
Ⅱ.取褪色后溶液,滴加盐酸和BaCl2溶液,产生白色沉淀.
Ⅲ.向2mL 0.1mol•L-1 FeCl3溶液中滴加2滴0.1mol•L-1KSCN溶液,变红,通入O2,无明显变化.
①实验I的说明溶液红色褪去是因为SCN-发生了反应而不是Fe3+发生反应;
②实验III的目的是排除H2O2分解产生的O2氧化SCN-的可能.
得出结论:溶液褪色的原因是酸性条件下H2O2将SCN-氧化成SO42-.
(3)甲直接用FeCl2•4H2O配制0.15mol•L-1的FeCl2溶液,重复步骤二中的操作,发现液体红色并未褪去.进一步探究其原因:
Ⅰ.用激光笔分别照射红色液体和滴加了KSCN溶液的FeCl3溶液,前者有丁达尔效应,后者无.测所配FeCl2溶液的pH,约为3.由此,乙认为红色不褪去的可能原因是H2O2将Fe2+氧化为Fe3+,pH增大促进Fe3+水解形成红色Fe(OH)3胶体.
Ⅱ.查阅资料后推测,红色不褪去的原因还可能是pH较大时H2O2不能氧化SCN-.乙利用上述部分试剂,通过实验排除了这一可能.乙的实验操作及现象是:
| 步骤 | 试剂及操作 | 现 象 |
| i | 取2 mL BaCl2溶液,滴加2滴0.1 mol•L-1KSCN溶液和5滴5% H2O2溶液 | 生成白色沉淀 |
| ii | 向i所得溶液中滴加0.1mol•L-1 FeCl3溶液 | 无明显现象 |
1.下列说法不正确的是( )
0 156631 156639 156645 156649 156655 156657 156661 156667 156669 156675 156681 156685 156687 156691 156697 156699 156705 156709 156711 156715 156717 156721 156723 156725 156726 156727 156729 156730 156731 156733 156735 156739 156741 156745 156747 156751 156757 156759 156765 156769 156771 156775 156781 156787 156789 156795 156799 156801 156807 156811 156817 156825 203614
| A. | 常温下,向醋酸钠溶液中滴加盐酸至溶液呈中性一定有:c(CH3COOH)=c(Cl-) | |
| B. | NaHSO4溶液中滴加Ba(OH)2至溶液恰好呈中性c(Na+)>c(SO42-)>c(OH-)=c(H+) | |
| C. | 某酸式盐NaHA溶液中一定有:c(OH-)+c(A2-)=c(H+)+c(H2A) | |
| D. | 0.5 mol/L 的Na2S溶液中:$\frac{1}{2}$ c(Na+)=c(H2S)+c(HS-)+c(S2-)=0.5 mol/L |
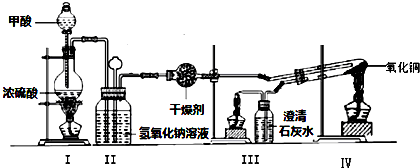
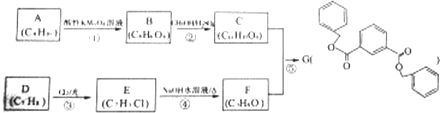
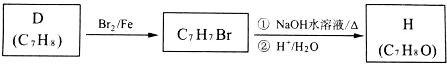
 .
.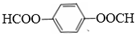 .
.