20.瓦斯爆炸是煤矿开采中的重大危害,一种瓦斯分析仪(图甲)能够在煤矿巷道中的甲烷浓度达到一定浓度时,可以通过传感器显示.该瓦斯分析仪工作原理类似燃料电池的工作原理,其装置如下图乙所示,其中的固体电解质是Y2O3-Na2O,O2-可以在其中自由移动.
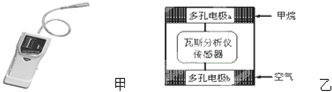
下列有关叙述正确的是( )

下列有关叙述正确的是( )
| A. | 电极b是正极,O2-由电极a流向电极b | |
| B. | 瓦斯分析仪工作时,电池内电路中电子由电极b流向电极a | |
| C. | 当固体电解质中有1 mol O2-通过时,电子转移4 mol | |
| D. | 电极a的反应式为:CH4+5O2--8e-═CO32-+2H2O |
19.下列离子方程式书写正确的是( )
| A. | 铜片与浓硫酸加热反应:Cu+4H++SO42-$\frac{\underline{\;\;△\;\;}}{\;}$ Cu2++SO2↑+2H2O | |
| B. | 向漂白精溶液中通入少量CO2:Ca2++2ClO-+H2O+CO2═CaCO3↓+2HClO | |
| C. | H2C2O4溶液能使KMnO4酸性溶液褪色 2MnO4-+5C2O42-+16H+═2Mn2++10CO2↑+8H2O | |
| D. | 向Fe(NO3)2溶液中加入过量的HI溶液 3Fe2++4H++NO3-═3Fe3++NO↑+2H2O |
18.NA表示阿伏伽德罗常数的数值,下列说法正确的是( )
| A. | 用铜作电极电解饱和食盐水,当线路中通过NA个电子时,阳极生成11.2L气体(标准状况下) | |
| B. | 把5.6g铁片投入到足量的冷的浓硝酸中,转移电子数为0.3NA | |
| C. | 12g石墨晶体中含有碳碳单键数为1.5NA | |
| D. | 15g-CH3中含有的电子数为10NA |
17.化学与生活密切相关,下列说法不正确的是( )
| A. | 糖类、油脂、蛋白质都能发生水解 | |
| B. | Na2CO3、NaHCO3可用作食用碱或工业用碱 | |
| C. | “地沟油”禁止食用,但可以用来制肥皂或生产燃料油 | |
| D. | 红葡萄酒密封储存时间越长,质量越好,原因之一是储存过程中生成了有香味的酯 |
15.硫酸亚铁是重要的亚铁盐,广泛用于医药、化工和防腐等领域.
(1)硫酸亚铁溶液呈酸性,其原因是Fe2++2H2O?Fe(OH)2+2H+(用离子方程式表示).
(2)硫酸亚铁在高温下会发生分解.某化学学习小组为探究硫酸亚铁在不同温度下的分解产物,进行了如下探究.请你完成下列问题:
【提出猜想】
①硫酸亚铁在不同温度下分解得到产物,可能是FeO和SO3(沸点44.8℃);也可能是Fe2O3、SO3和SO2.
【实验探究】
小组的同学根据猜想,设计了实验装置,并选择了可能用到的试剂如下:
A.品红溶液、B.KSCN溶液、C.BaCl2溶液 D.Ba(NO3)2溶液.
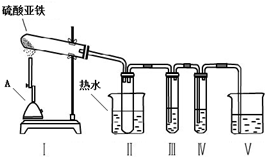
②为了得到较高温度,加热用的仪器A名称是酒精喷灯.
③为了检验气体产物中含有SO3,在装置Ⅲ应装的试剂是C(选填试剂序号),装置Ⅱ中装热水的作用是避免SO3冷却成液体.
④为了检验固体产物成分,取反应后的固体于试管中,加稀硫酸溶解,将所得溶液分成两份,进行如下实验:
⑤若生成的固体产物为Fe2O3和FeO,且其物质的量相等.则反应的化学方程式为3FeSO4 $\frac{\underline{\;高温\;}}{\;}$FeO+Fe2O3+SO2↑+2SO3↑.
(1)硫酸亚铁溶液呈酸性,其原因是Fe2++2H2O?Fe(OH)2+2H+(用离子方程式表示).
(2)硫酸亚铁在高温下会发生分解.某化学学习小组为探究硫酸亚铁在不同温度下的分解产物,进行了如下探究.请你完成下列问题:
【提出猜想】
①硫酸亚铁在不同温度下分解得到产物,可能是FeO和SO3(沸点44.8℃);也可能是Fe2O3、SO3和SO2.
【实验探究】
小组的同学根据猜想,设计了实验装置,并选择了可能用到的试剂如下:
A.品红溶液、B.KSCN溶液、C.BaCl2溶液 D.Ba(NO3)2溶液.

②为了得到较高温度,加热用的仪器A名称是酒精喷灯.
③为了检验气体产物中含有SO3,在装置Ⅲ应装的试剂是C(选填试剂序号),装置Ⅱ中装热水的作用是避免SO3冷却成液体.
④为了检验固体产物成分,取反应后的固体于试管中,加稀硫酸溶解,将所得溶液分成两份,进行如下实验:
| 操作步骤 | 预期实验现象 | 预期实验结论 |
| 向其中一份溶液中加入 KSCN溶液(或B). | 溶液变成血红色 | 固体中含有Fe2O3 |
| 向另一份溶液中滴加 2滴黄色K3[Fe(CN)6]溶液. | 产生蓝色沉淀 | 固体中含有FeO |
13.五种短周期元素的某些性质如表所示,下列说法正确的是( )
| 元素代号 | X | W | Y | Z | Q |
| 原子半径(×10-12m) | 37 | 71 | 74 | 77 | 186 |
| 主要化合价 | +1 | -1 | -2 | +4、-4 | +1 |
| A. | X和Q都属于金属元素 | |
| B. | Y和Z的基态原子s能级和p能级电子数相同 | |
| C. | Y和W的第一电离能大小比较:Y>W | |
| D. | X、Z形成的化合物分子中可能既有σ键又有π键 |
12.某化学小组在学习元素周期律后,对教材中Fe2+氧化为Fe3+的实验进一步思考,并提出问题:Cl2能将Fe2+氧化为Fe3+,那么Br2和I2能否将Fe2+氧化为Fe3+?
环节一:理论推测
部分同学认为Br2和I2都可能将Fe2+氧化为Fe3+,他们思考的依据是均为第ⅤⅡA单质,氧化性均较强.
部分同学认为Br2和I2都不能将Fe2+氧化为Fe3+,还有同学认为Br2能将Fe2+氧化为Fe3+而I2不能.他们思考的依据是从上到下卤素单质氧化性减弱.
环节二:设计实验进行验证
在大试管中加适量铁粉,加入10mL 稀盐酸,振荡试管,充分反应后,铁粉有剩余,取上层清液进行下列实验.
实验1:
环节三:实验现象的分析与解释
(1)同学甲认为①中现象说明溴水能将Fe3+氧化,离子方程式为2Fe2++Br2=2Fe3++2Br-.
同学乙认为应该补充实验,才能得出同学甲的结论.请你帮助同学乙完成实验:
实验2:
(2)该小组同学对②中溶液呈黄色的原因展开了讨论:
可能1:碘水与FeCl2溶液不反应,黄色是碘水稀释后的颜色.
可能2:碘水与FeCl2溶液发生反应,但FeCl3溶液也是黄色的,所以没有明显现象.
实验3:进行实验以确定可能的原因
同学丙认为该实验现象可以说明是“可能2”成立,同学丁认为不严谨,于是设计了实验4:
实验4:
你认为实验4设计的主要目的是亚铁离子与空气接触会被氧化,加入乙酸乙酯既可作为萃取剂又能起到液封的作用,减少空气对实验的影响.
同学丁根据实验4现象得出结论:在本次实验条件下,碘水与FeCl2溶液反应的程度很小.
(3)Cl2、Br2、I2氧化Fe3+的能力逐渐减弱,用原子结构解释原因:同一主族元素从上到下原子核外电子层数依次增多,原子半径逐渐增大,得电子能力逐渐减弱,氧化性减弱.
0 156630 156638 156644 156648 156654 156656 156660 156666 156668 156674 156680 156684 156686 156690 156696 156698 156704 156708 156710 156714 156716 156720 156722 156724 156725 156726 156728 156729 156730 156732 156734 156738 156740 156744 156746 156750 156756 156758 156764 156768 156770 156774 156780 156786 156788 156794 156798 156800 156806 156810 156816 156824 203614
环节一:理论推测
部分同学认为Br2和I2都可能将Fe2+氧化为Fe3+,他们思考的依据是均为第ⅤⅡA单质,氧化性均较强.
部分同学认为Br2和I2都不能将Fe2+氧化为Fe3+,还有同学认为Br2能将Fe2+氧化为Fe3+而I2不能.他们思考的依据是从上到下卤素单质氧化性减弱.
环节二:设计实验进行验证
在大试管中加适量铁粉,加入10mL 稀盐酸,振荡试管,充分反应后,铁粉有剩余,取上层清液进行下列实验.
实验1:
| 试管 | 操作 | 现象 |
| ① | 先向试管中加入2mL FeCl2溶液,再滴加少量红棕色的溴水,振荡试管 | 溶液为黄色 |
| ② | 先向试管中加入2mL FeCl2溶液,再滴加少量棕黄色的碘水,振荡试管 | 溶液为黄色 |
(1)同学甲认为①中现象说明溴水能将Fe3+氧化,离子方程式为2Fe2++Br2=2Fe3++2Br-.
同学乙认为应该补充实验,才能得出同学甲的结论.请你帮助同学乙完成实验:
实验2:
| 操作 | 应该观察到的现象 |
可能1:碘水与FeCl2溶液不反应,黄色是碘水稀释后的颜色.
可能2:碘水与FeCl2溶液发生反应,但FeCl3溶液也是黄色的,所以没有明显现象.
实验3:进行实验以确定可能的原因
| 操作 | 现象 |
| 向试管②所得溶液中继续加入0.5mLCCl4,充分振荡,静置一段时间后.取出上层溶液,滴加KSCN 溶液 | 静置后,上层溶液几乎无色,下层溶液为紫色;上层溶液滴加KSCN 溶液后,出现浅红色 |
实验4:
| 操作 | 现象 |
| 向另一支试管中加入2mL FeCl2溶液,滴加0.5mL碘水后,再加入0.5mL 乙酸乙酯,充分振荡,静置一段时间后.取出下层溶液,滴加KSCN 溶液 | 静置后,上层液为紫色,下层液几乎无色;下层溶液滴加KSCN溶液后,没有出现浅红色 |
同学丁根据实验4现象得出结论:在本次实验条件下,碘水与FeCl2溶液反应的程度很小.
(3)Cl2、Br2、I2氧化Fe3+的能力逐渐减弱,用原子结构解释原因:同一主族元素从上到下原子核外电子层数依次增多,原子半径逐渐增大,得电子能力逐渐减弱,氧化性减弱.
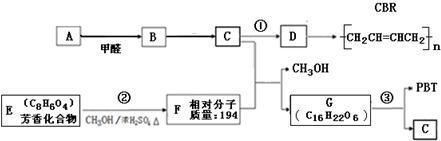
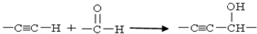
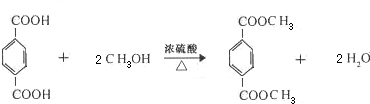 .E有多种芳香族同分异构体,其中红外光谱显示分子中含“-COO-”,核磁共振氢谱显示3个吸收峰,且峰面积之比为1:1:1的结构简式是
.E有多种芳香族同分异构体,其中红外光谱显示分子中含“-COO-”,核磁共振氢谱显示3个吸收峰,且峰面积之比为1:1:1的结构简式是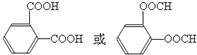 .
.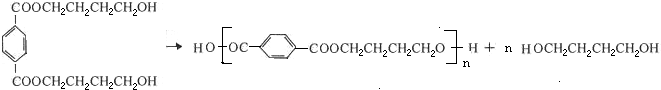 .
.