2.在一定温度下的定容密闭容器中,发生反应:A(s)+2B(g)?C(g)+D(g),当下列物理量不再变化时,不能表明反应已达平衡的标志是( )
| A. | A的质量 | B. | 混合气体的质量 | ||
| C. | B的物质的量 | D. | 气体的总物质的量 |
1.某烷烃4.5g充分燃烧,将生成的气体通入过量澄清的石灰水中,得沉淀30g,这种烷烃是( )
| A. | 甲烷 | B. | 乙烷 | C. | 丙烷 | D. | 丁烷 |
20.下列关于苯的说法中,正确的是( )
| A. | 通入氢气即可发生加成反应 | |
| B. | 分子中含有3个C-C单键和三个C═C双键 | |
| C. | 分子中C、H元素的质量比为6:1 | |
| D. | 在空气中燃烧时产生浓烈的黑烟 |
19.工业上设计将VOSO4中的K2SO4、SiO2杂质除去并回收得到V2O5的流程如下:
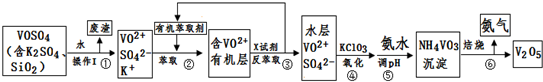
请回答下列问题:
(1)步骤①所得废渣的成分是SiO2(写化学式),操作I的名称过滤.
(2)步骤②、③的变化过程可简化为(下式R表示VO2+,HA表示有机萃取剂):R2(SO4)n(水层)+2nHA(有机层)?2RAn(有机层)+nH2SO4(水层)
②中萃取时必须加入适量碱,其原因是加入碱中和产生的酸,平衡右移提高了钒的萃取率.
③中X试剂为硫酸.
(3)④的离子方程式为NH3•H2O+VO3-═NH4VO3↓+OH-.
(4)25℃时,取样进行试验分析,得到钒沉淀率和溶液pH之间关系如表:
结合上表,在实际生产中,⑤中加入氨水,调节溶液的最佳pH为1.7-1.8.
若钒沉淀率为93.1%时不产生Fe(OH)3沉淀,则溶液中c(Fe3+)<2.6×10-3.
(已知:25℃时,Ksp[Fe(OH)3]=2.6×10-39)
(5)该工艺流程中,可以循环利用的物质有有机萃取剂和氨气.

请回答下列问题:
(1)步骤①所得废渣的成分是SiO2(写化学式),操作I的名称过滤.
(2)步骤②、③的变化过程可简化为(下式R表示VO2+,HA表示有机萃取剂):R2(SO4)n(水层)+2nHA(有机层)?2RAn(有机层)+nH2SO4(水层)
②中萃取时必须加入适量碱,其原因是加入碱中和产生的酸,平衡右移提高了钒的萃取率.
③中X试剂为硫酸.
(3)④的离子方程式为NH3•H2O+VO3-═NH4VO3↓+OH-.
(4)25℃时,取样进行试验分析,得到钒沉淀率和溶液pH之间关系如表:
| pH | 1.3 | 1.4 | 1.5 | 1.6 | 1.7 | 1.8 | 1.9 | 2.0 | 2.1 |
| 钒沉淀率% | 88.1 | 94.8 | 96.5 | 98.0 | 98.8 | 98.8 | 96.4 | 93.1 | 89.3 |
若钒沉淀率为93.1%时不产生Fe(OH)3沉淀,则溶液中c(Fe3+)<2.6×10-3.
(已知:25℃时,Ksp[Fe(OH)3]=2.6×10-39)
(5)该工艺流程中,可以循环利用的物质有有机萃取剂和氨气.
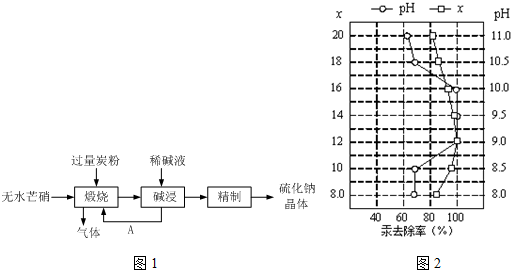
16.经初步检测蛇纹石矿由MgO、Fe2O3、Al2O3、SiO2等组成.分析如图1:
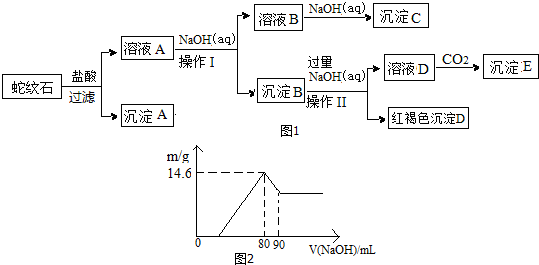
请回答下列问题:
(1)蛇纹石与盐酸充分反应后再过滤即可得溶液A.在过滤中用到的玻璃仪器有烧杯、玻璃棒、漏斗.
(2)沉淀B的组成是Al(OH)3、Fe(OH)3,向溶液A中逐滴加入NaOH溶液,以控制溶液pH在C的范围内可得到符合图1关系的沉淀B.(填写下列正确选项前的字母.有关氢氧化物沉淀的pH见下表,且pH达到7.8时,氢氧化铝开始溶解.)
A.1~3 B.3~5 C.5~7 D.7~8
(3)写出向溶液D中通入过量CO2反应的离子方程式:AlO2-+CO2+2H2O=Al(OH)3↓+HCO3-.
(4)向溶液A中逐滴加入5mol•mol-1NaOH溶液,经过操作I和操作II得到的沉淀质量与V[NaOH(aq)]有图2所示的数据关系.经分析蛇纹石中Fe2O3与Al2O3的物质的量之比为2:1.

请回答下列问题:
(1)蛇纹石与盐酸充分反应后再过滤即可得溶液A.在过滤中用到的玻璃仪器有烧杯、玻璃棒、漏斗.
(2)沉淀B的组成是Al(OH)3、Fe(OH)3,向溶液A中逐滴加入NaOH溶液,以控制溶液pH在C的范围内可得到符合图1关系的沉淀B.(填写下列正确选项前的字母.有关氢氧化物沉淀的pH见下表,且pH达到7.8时,氢氧化铝开始溶解.)
| 氢氧化物 | Fe(OH)3 | Al(OH)3 | Mg(OH)2 |
| 开始沉淀pH | 1.9 | 3.3 | 9.4 |
| 完全沉淀pH | 3.7 | 4.7 | 11 |
(3)写出向溶液D中通入过量CO2反应的离子方程式:AlO2-+CO2+2H2O=Al(OH)3↓+HCO3-.
(4)向溶液A中逐滴加入5mol•mol-1NaOH溶液,经过操作I和操作II得到的沉淀质量与V[NaOH(aq)]有图2所示的数据关系.经分析蛇纹石中Fe2O3与Al2O3的物质的量之比为2:1.
14.25℃、101kPa 下:
①2Na(s)+$\frac{1}{2}$O2(g)═Na2O(s)△H1=-414KJ/mol
②2Na(s)+O2(g)═Na2O2(s)△H2=-511KJ/mol
下列说法正确的是( )
①2Na(s)+$\frac{1}{2}$O2(g)═Na2O(s)△H1=-414KJ/mol
②2Na(s)+O2(g)═Na2O2(s)△H2=-511KJ/mol
下列说法正确的是( )
| A. | ①和②产物的阴阳离子个数比不相等 | |
| B. | ①和②生成等物质的量的产物,转移电子数不同 | |
| C. | 常温下Na与足量O2反应生成Na2O,随温度升高生成Na2O的速率逐渐加快 | |
| D. | 25℃、101kPa 下,Na2O2(s)+2 Na(s)═2Na2O(s)△H=-317kJ/mol |
13.不论以何种比例混合,将甲和乙两种混合气体同时通入过量的丙溶液中,一定能产生沉淀的组合是( )
0 156610 156618 156624 156628 156634 156636 156640 156646 156648 156654 156660 156664 156666 156670 156676 156678 156684 156688 156690 156694 156696 156700 156702 156704 156705 156706 156708 156709 156710 156712 156714 156718 156720 156724 156726 156730 156736 156738 156744 156748 156750 156754 156760 156766 156768 156774 156778 156780 156786 156790 156796 156804 203614
| 序号 | 甲 | 乙 | 丙 |
| ① | CO2 | SO2 | 石灰水 |
| ② | HCl | CO2 | 石灰水 |
| ③ | CO2 | SO2 | Ba(NO3)2 |
| ④ | Cl2 | SO2 | BaCl2 |
| ⑤ | CO2 | NH3 | CaCl2 |
| ⑥ | NO2 | SO2 | BaCl2 |
| A. | ①②③④⑤ | B. | 只有②③④ | C. | 只有①③④ | D. | ①②③④⑥ |