1.ClO2是一种杀菌消毒效率高、二次污染小的水处理剂.实验室中可通过以下反应制得ClO2:2KClO3+H2C2O4+H2SO4$\frac{\underline{\;\;△\;\;}}{\;}$2ClO2↑+K2SO4+2CO2↑+2H2O 下列说法不正确的是( )
| A. | CO2是氧化产物 | |
| B. | H2C2O4在反应中被氧化 | |
| C. | 1mol KClO3参加反应,转移的电子为1mol | |
| D. | H2C2O4的氧化性强于ClO2的氧化性 |
18.表是元素周期表一部分,列出了九种元素在周期表中的位置:
请用化学用语回答下列问题
(1)在上述元素中,非金属性最强的是F,在③~⑦元素中,原子半径最大的是Mg;
(2)①~⑨中元素最高价氧化物对应的水化物中酸性最强的是HClO4(填物质化学式).写出①和④的最高价氧化物对应的水化物反应的离子方程式Al(OH)3+OH-═AlO2-+2H2O.
(3)用电子式表示③和⑨形成的化合物的形成过程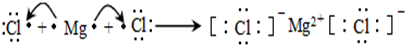 .
.
(4)表中元素①和⑦可以形成一种淡黄色物质X,写出X的电子式: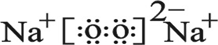 ,该物质所含化学键类型离子键和共价键,0.1mol X与水反应转移电子数为:0.1NA.
,该物质所含化学键类型离子键和共价键,0.1mol X与水反应转移电子数为:0.1NA.
| 族 周期 | IA | IIA | IIIA | IVA | VA | VIA | VIIA | 0 |
| 2 | ⑤ | ⑥ | ⑦ | ⑧ | ||||
| 3 | ① | ③ | ④ | ⑨ | ||||
| 4 | ② |
(1)在上述元素中,非金属性最强的是F,在③~⑦元素中,原子半径最大的是Mg;
(2)①~⑨中元素最高价氧化物对应的水化物中酸性最强的是HClO4(填物质化学式).写出①和④的最高价氧化物对应的水化物反应的离子方程式Al(OH)3+OH-═AlO2-+2H2O.
(3)用电子式表示③和⑨形成的化合物的形成过程
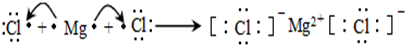 .
.(4)表中元素①和⑦可以形成一种淡黄色物质X,写出X的电子式:
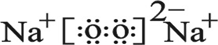 ,该物质所含化学键类型离子键和共价键,0.1mol X与水反应转移电子数为:0.1NA.
,该物质所含化学键类型离子键和共价键,0.1mol X与水反应转移电子数为:0.1NA.
14.下列实验方案能达到实验目的是( )
| 实验目的 | 实验方案 | |
| A | 证明溴乙烷发生消去反应有 乙烯生成 | 向试管中加入适量的溴乙烷和NaOH的乙醇溶液, 加热,将反应产生的气体通入溴的四氯化碳溶液 |
| B | 证明HCOOH结构中含有醛 基 | 将1mL 1mol/L HCOOH溶液加入装有银氨溶液 的试管中并水浴加热,观察有无银镜产生 |
| C | 除去甲烷中的乙烯 | 将混合气通入KMnO4溶液中洗气 |
| D | 制取乙烯气体 | 将无水乙醇和浓硫酸混合加热到140℃ |
| A. | A | B. | B | C. | C | D. | D |
13.下列分子式只表示一种纯净物的是( )
0 156608 156616 156622 156626 156632 156634 156638 156644 156646 156652 156658 156662 156664 156668 156674 156676 156682 156686 156688 156692 156694 156698 156700 156702 156703 156704 156706 156707 156708 156710 156712 156716 156718 156722 156724 156728 156734 156736 156742 156746 156748 156752 156758 156764 156766 156772 156776 156778 156784 156788 156794 156802 203614
| A. | C2H4O2 | B. | C3H6 | C. | CH2O | D. | C5H12 |
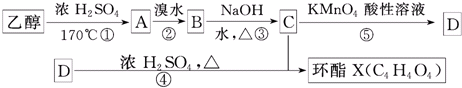
 +2H2O
+2H2O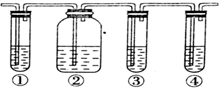

 ;由F生成一硝基产物的化学方程式为
;由F生成一硝基产物的化学方程式为 .
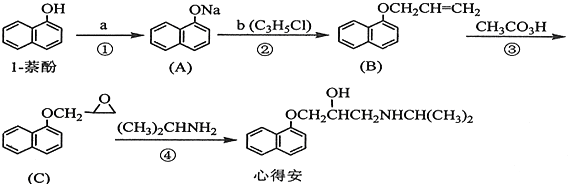
.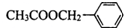 是其中的一种,它可以从茉莉花中提取,也可以用甲苯和乙醇为原料进行人工合成.一种合成路线如下:
是其中的一种,它可以从茉莉花中提取,也可以用甲苯和乙醇为原料进行人工合成.一种合成路线如下: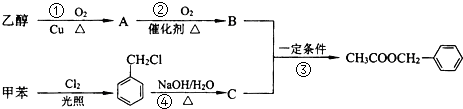
 +H2O$→_{△}^{氢氧化钠}$
+H2O$→_{△}^{氢氧化钠}$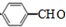 ;试写出遇FeCl3溶液显紫色,且符合以下条件的C的同分异构体的结构简式:
;试写出遇FeCl3溶液显紫色,且符合以下条件的C的同分异构体的结构简式: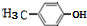
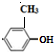 .
.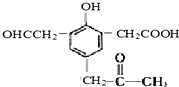 ,试回答:
,试回答: