1.下列分子中δ键与π键数之比为3:1的是( )
| A. | N2 | B. | C2H4 | C. | HCHO | D. | HCN |
16.下列叙述不正确的是( )
| A. | NH3易液化,液氨常作制冷剂 | |
| B. | NO、NO2都是有毒气体 | |
| C. | 铵盐受热易分解,因此贮存铵态氮肥时要密封保存,并放在阴凉通风处 | |
| D. | 稀HNO3和活泼金属反应时主要得到氢气 |
14.能正确表示下列反应的离子方程式是( )
0 156584 156592 156598 156602 156608 156610 156614 156620 156622 156628 156634 156638 156640 156644 156650 156652 156658 156662 156664 156668 156670 156674 156676 156678 156679 156680 156682 156683 156684 156686 156688 156692 156694 156698 156700 156704 156710 156712 156718 156722 156724 156728 156734 156740 156742 156748 156752 156754 156760 156764 156770 156778 203614
| A. | Cl2与水反应:Cl2+H2O═2H++ClO-+Cl- | |
| B. | CuSO4溶液中加入Ba(OH)2溶液:Ba2++SO42-═BaSO4↓ | |
| C. | 将鸡蛋壳在醋酸中溶解有气泡产生:CaCO3+2H+═Ca2++H2O+CO2↑ | |
| D. | 铁与盐酸反应:Fe+2H+═Fe2++H2↑ |
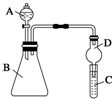 某同学为探究元素周期表中元素性质的递变规律,设计了如下系列实验.
某同学为探究元素周期表中元素性质的递变规律,设计了如下系列实验.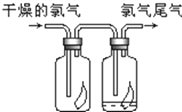 (1)瑞典化学家舍勒将软锰矿(主要成分MnO2)与浓盐酸混合加热,在世界上首先制得了氯气.写出该反应的离子方程式,并用双线桥画出电子转移的方向和数目.
(1)瑞典化学家舍勒将软锰矿(主要成分MnO2)与浓盐酸混合加热,在世界上首先制得了氯气.写出该反应的离子方程式,并用双线桥画出电子转移的方向和数目.
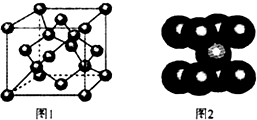 C、Be、Cl、Fe等元素及其化合物有重要的应用.
C、Be、Cl、Fe等元素及其化合物有重要的应用.