8.J、L、M、R、T是原子序数依次增大的短周期主族元素,J、R在周期表中的相对位置如右表;J元素最低负化合价的绝对值与其原子最外层电子数相等;M是地壳中含量最多的金属元素.
(1)M的离子结构示意图为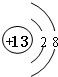 ;元素T周期表中位于第ⅦA族.
;元素T周期表中位于第ⅦA族.
(2)J和氢组成的化合物分子有4个原子,其结构式为H-C≡C-H.
(3)M和T形成的化合物在潮湿的空气中冒白色烟雾,反应的化学方程式为AlCl3+3H2O=Al(OH)3+3HCl↑.
(4)L的最简单气态氢化物甲的水溶液显碱性.
①在微电子工业中,甲的水溶液可作刻蚀剂H2O2 的清除剂,所发生反应的产物不污染环境,其化学方程式为2NH3•H2O+3H2O2=N2+8H2O.
②由甲与氧气、KOH 溶液构成原电池,负极会产生L的单质.则其负极反应式为2NH3-6e-+6OH-═N2+6H2O.
(5)由J、R形成的液态化合物JR2 0.2mol在O2中完全燃烧,生成两种气态氧化物,298K时放出热量215kJ. 该反应的热化学方程式为CS2(l)+3O2(g)=CO2(g)+2SO2(g)△H=-1075KJ/mol.
| J | ||||
| R |
 ;元素T周期表中位于第ⅦA族.
;元素T周期表中位于第ⅦA族.(2)J和氢组成的化合物分子有4个原子,其结构式为H-C≡C-H.
(3)M和T形成的化合物在潮湿的空气中冒白色烟雾,反应的化学方程式为AlCl3+3H2O=Al(OH)3+3HCl↑.
(4)L的最简单气态氢化物甲的水溶液显碱性.
①在微电子工业中,甲的水溶液可作刻蚀剂H2O2 的清除剂,所发生反应的产物不污染环境,其化学方程式为2NH3•H2O+3H2O2=N2+8H2O.
②由甲与氧气、KOH 溶液构成原电池,负极会产生L的单质.则其负极反应式为2NH3-6e-+6OH-═N2+6H2O.
(5)由J、R形成的液态化合物JR2 0.2mol在O2中完全燃烧,生成两种气态氧化物,298K时放出热量215kJ. 该反应的热化学方程式为CS2(l)+3O2(g)=CO2(g)+2SO2(g)△H=-1075KJ/mol.
7. 将CO2气体缓缓地通入到含KOH、Ba(OH)2和KAlO2的混合溶液中直至过量,生成沉淀的物质的量与所通CO2的体积关系如图所示.下列关于整个反应进程中的各种描述不正确的是( )
将CO2气体缓缓地通入到含KOH、Ba(OH)2和KAlO2的混合溶液中直至过量,生成沉淀的物质的量与所通CO2的体积关系如图所示.下列关于整个反应进程中的各种描述不正确的是( )
 将CO2气体缓缓地通入到含KOH、Ba(OH)2和KAlO2的混合溶液中直至过量,生成沉淀的物质的量与所通CO2的体积关系如图所示.下列关于整个反应进程中的各种描述不正确的是( )
将CO2气体缓缓地通入到含KOH、Ba(OH)2和KAlO2的混合溶液中直至过量,生成沉淀的物质的量与所通CO2的体积关系如图所示.下列关于整个反应进程中的各种描述不正确的是( )| A. | O~A段反应的离子方程式是Ba2++CO32-═BaCO3↓ | |
| B. | A~B段反应的离子方程式是2OH-+CO2═CO${\;}_{3}^{2-}$+H2O | |
| C. | A~B段与C~D段所发生的反应相同 | |
| D. | D~E段沉淀的减少是由于碳酸钡固体与CO2的水溶液反应所致 |
6.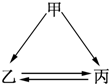 \如图所示的甲、乙、丙三种物质均含有相同的某种元素,箭头表示物质间的转化一步就能实现,则甲可能是( )
\如图所示的甲、乙、丙三种物质均含有相同的某种元素,箭头表示物质间的转化一步就能实现,则甲可能是( )
①Fe
②HNO3
③Na
④Si.
 \如图所示的甲、乙、丙三种物质均含有相同的某种元素,箭头表示物质间的转化一步就能实现,则甲可能是( )
\如图所示的甲、乙、丙三种物质均含有相同的某种元素,箭头表示物质间的转化一步就能实现,则甲可能是( )①Fe
②HNO3
③Na
④Si.
| A. | ①②③ | B. | ②③④ | C. | ①②④ | D. | ①②③④ |
5.下列化合物中既易发生取代反应,也可发生加成反应,还能使酸性KMnO4溶液褪色的是( )
| A. | 乙烷 | B. | 乙醇 | C. | 丙烯 | D. | 苯 |
4.北京奥运会“祥云”火炬使用的燃料为丙烷.下列关于丙烷的说法正确的是( )
0 156578 156586 156592 156596 156602 156604 156608 156614 156616 156622 156628 156632 156634 156638 156644 156646 156652 156656 156658 156662 156664 156668 156670 156672 156673 156674 156676 156677 156678 156680 156682 156686 156688 156692 156694 156698 156704 156706 156712 156716 156718 156722 156728 156734 156736 156742 156746 156748 156754 156758 156764 156772 203614
| A. | 分子中的碳原子在一条直线上 | B. | 其一氯代物只有一种 | ||
| C. | 能使酸性高锰酸钾溶液褪色 | D. | 结构简式为CH3 CH2 CH3 |