3.化学与生活密切相关.下列说法不正确的是( )
| A. | 乙烯可用作水果的催熟剂 | |
| B. | 二氧化硫可用作食品的漂白剂 | |
| C. | 交警可用酸性重铬酸钾来检测司机是否酒驾 | |
| D. | 黄铜(铜锌合金)制作的铜锣不易产生铜绿 |
2.x、y、z三种物质的分子组成分别符合烷烃、烯烃、炔烃的通式,若在一定条件下V L的x、y、z的混合气体可与V L的H2发生加成反应,则混合气体中x、y、z的体积比不可能是( )
| A. | 1:1:1 | B. | 3:2:3 | C. | 1:4:1 | D. | 3:2:1 |
20.已知2H2(g)+O2(g)═2H2O(g)△H1; 2H2(g)+O2(g)═2H2O(l)△H2.则下列关于△H1与△H2大小比较中正确的是( )
| A. | △H1>△H2 | B. | △H1<△H2 | C. | △H1=△H2 | D. | 无法确定 |
19.下列实验不能获得成功的是( )
| 选项 | 实验目的 | 实验步骤 |
| A | 探究催化剂对化学反应速率的影响 | 向H2O2溶液中滴加少量FeCl3溶液 |
| B | 探究乙醇能发生氧化反应 | 将铜丝在酒精灯加热后,立即伸入无水乙醇中 |
| C | 探究石蜡油分解的产物不都是烷烃 | 将石蜡油加强热产生的气体通入溴水中 |
| D | 探究浓度对反应速率的影响 | 取少量等质量的相同铁粉,分别加入1mol/L的硫酸和18mol/L的硫酸中,观察现象 |
| A. | A | B. | B | C. | C | D. | D |
18.成语“恶狗酒酸”中隐藏着一个寓言故事:人有市酒而甚美者,然至酒酸而不售,问里人其故.里人曰:公之狗甚狂,人有持器往者,狗辄迎面啮之,是以酒酸不售也. 下列关于“酒”的说法错误的是( )
| A. | “恶狗酒酸”的成语中涉及了氧化反应 | |
| B. | 饮用的白酒是纯净物,即乙醇 | |
| C. | 酿酒过程中发生了物理变化和化学变化 | |
| D. | 工业酒精中因含有剧毒物质甲醇而不能用来勾兑饮用酒水 |
17.硫酸锌被广泛应用于医药领域和工农业生产.工业上由氧化锌矿(主要成分为ZnO,另含ZnSiO3、FeCO3、CuO等)生产ZnSO4•7H2O的一种流程如图:
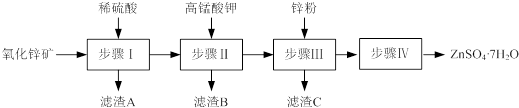
(1)步骤Ⅰ的操作是过滤,滤渣A的主要成分是H2SiO3.
(2)步骤Ⅰ加入稀硫酸进行酸浸时,需不断通入高温水蒸气的目的是H2SiO3+2NaOH=Na2SiO3+2H2O.
(3)步骤Ⅱ中,在pH约为5.1的滤液中加入高锰酸钾,生成Fe(OH)3和MnO(OH)2两种沉淀,该反应的离子方程式为3Fe2++MnO4-+8H2O=3Fe(OH)3↓+MnO(OH)2↓+5H+.
(4)步骤Ⅲ中,加入锌粉的作用是换出Cu,除去Cu2+.所得的滤液中含有的金属阳离子有Zn2+、K+.
(5)已知硫酸锌的溶解度与温度之间的关系如下表:
从硫酸锌溶液中获得硫酸锌晶体的实验操作为60℃条件下蒸发浓缩、降温结晶、过滤.
烘干操作需在减压低温条件下进行,原因是降低烘干的温度,防止ZnSO4•7H2O分解.
(6)取28.70g ZnSO4•7H2O加热至不同温度,剩余固体的质量变化如图所示.
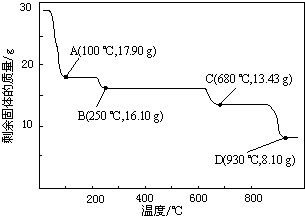
分析数据,680℃时所得固体的化学式为b.
a.ZnO b.Zn3O(SO4)2 c.ZnSO4 d.ZnSO4•H2O.

(1)步骤Ⅰ的操作是过滤,滤渣A的主要成分是H2SiO3.
(2)步骤Ⅰ加入稀硫酸进行酸浸时,需不断通入高温水蒸气的目的是H2SiO3+2NaOH=Na2SiO3+2H2O.
(3)步骤Ⅱ中,在pH约为5.1的滤液中加入高锰酸钾,生成Fe(OH)3和MnO(OH)2两种沉淀,该反应的离子方程式为3Fe2++MnO4-+8H2O=3Fe(OH)3↓+MnO(OH)2↓+5H+.
(4)步骤Ⅲ中,加入锌粉的作用是换出Cu,除去Cu2+.所得的滤液中含有的金属阳离子有Zn2+、K+.
(5)已知硫酸锌的溶解度与温度之间的关系如下表:
| 温度/℃ | 0 | 20 | 40 | 60 | 80 | 100 |
| 溶解度/g | 41.8 | 54.1 | 70.4 | 74.8 | 67.2 | 60.5 |
烘干操作需在减压低温条件下进行,原因是降低烘干的温度,防止ZnSO4•7H2O分解.
(6)取28.70g ZnSO4•7H2O加热至不同温度,剩余固体的质量变化如图所示.

分析数据,680℃时所得固体的化学式为b.
a.ZnO b.Zn3O(SO4)2 c.ZnSO4 d.ZnSO4•H2O.
16.某地有软锰矿和闪锌矿两座矿山,它们的组成(质量分数)如表:
科研人员开发了综合利用这两种资源的同槽酸浸工艺,工艺流程如图1所示.
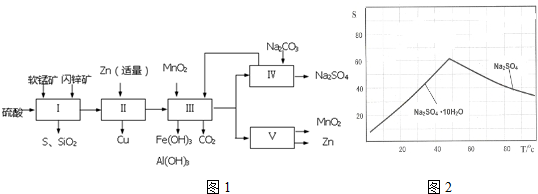
(1)流程Ⅰ所得滤液中含有MnSO4、ZnSO4、CuSO4、Fe2(SO4)3、Al2(SO4)3等,则流程Ⅰ中被氧化的物质有FeS、CuS种.
(2)流程Ⅱ中反应的离子方程式为Zn+Fe3+=Fe2++Zn2+、Zn+Cu2+=Cu+Zn2+.
(3)氢氧化物开始沉淀的pH如表:
流程Ⅲ中MnO2的作用是将Fe2+氧化成Fe3+,不直接生成Fe(OH)2沉淀的原因是使铁元素能全部沉淀.
(4)如图2是Na2SO4和Na2SO4•10H2O的溶解度(g/100g水)曲线,又知MnSO4和ZnSO4的溶解度随温度的升高而增大,则流程Ⅳ得到Na2SO4固体的操作是:将分离出MnCO3和ZnCO3后的滤液升温结晶、趁热过滤、乙醇洗涤、干燥,要“趁热”过滤的原因是防止形成Na2SO4•10H2O.
(5)流程Ⅴ的条件是电解,电解时均用惰性电极,阳极发生的电极反应可表示为Mn2+-2e-+2H2O=MnO2+4H+.
(6)取1.95g锌加入到12.00mL 18.4mol/L的浓硫酸中(反应中只生成一种还原产物),充分反应后,小心地将溶液稀释到1000mL,取出15.00mL,以酚酞为指示剂,用0.25mol/L的NaOH溶液滴定余酸,耗用NaOH溶液的体积为21.70mL.
①反应后溶液中多余的硫酸是0.18 mol.
②通过计算确定浓硫酸被还原的产物是S.
0 156577 156585 156591 156595 156601 156603 156607 156613 156615 156621 156627 156631 156633 156637 156643 156645 156651 156655 156657 156661 156663 156667 156669 156671 156672 156673 156675 156676 156677 156679 156681 156685 156687 156691 156693 156697 156703 156705 156711 156715 156717 156721 156727 156733 156735 156741 156745 156747 156753 156757 156763 156771 203614
| 软锰矿 | 闪锌矿 |
| MnO2约70%,SiO2约20%,Al2O3约4%,其余为水分 | ZnS约80%,FeS、CuS、SiO2共约7%,其余为水分 |

(1)流程Ⅰ所得滤液中含有MnSO4、ZnSO4、CuSO4、Fe2(SO4)3、Al2(SO4)3等,则流程Ⅰ中被氧化的物质有FeS、CuS种.
(2)流程Ⅱ中反应的离子方程式为Zn+Fe3+=Fe2++Zn2+、Zn+Cu2+=Cu+Zn2+.
(3)氢氧化物开始沉淀的pH如表:
| 氢氧化物 | Fe(OH)3 | Al(OH)3 | Fe(OH)2 |
| 开始沉淀pH | 1.5 | 3.3 | 7.6 |
(4)如图2是Na2SO4和Na2SO4•10H2O的溶解度(g/100g水)曲线,又知MnSO4和ZnSO4的溶解度随温度的升高而增大,则流程Ⅳ得到Na2SO4固体的操作是:将分离出MnCO3和ZnCO3后的滤液升温结晶、趁热过滤、乙醇洗涤、干燥,要“趁热”过滤的原因是防止形成Na2SO4•10H2O.
(5)流程Ⅴ的条件是电解,电解时均用惰性电极,阳极发生的电极反应可表示为Mn2+-2e-+2H2O=MnO2+4H+.
(6)取1.95g锌加入到12.00mL 18.4mol/L的浓硫酸中(反应中只生成一种还原产物),充分反应后,小心地将溶液稀释到1000mL,取出15.00mL,以酚酞为指示剂,用0.25mol/L的NaOH溶液滴定余酸,耗用NaOH溶液的体积为21.70mL.
①反应后溶液中多余的硫酸是0.18 mol.
②通过计算确定浓硫酸被还原的产物是S.


 .
. .
.