3.下列离子方程式书写正确的是( )
| A. | 硫酸铜与氢氧化钡反应:Ba2++SO42-═BaSO4↓ | |
| B. | 氯气通入水中:Cl2+H2O?2H++Cl-+ClO- | |
| C. | AlCl3溶液中滴加过量氨水:Al3++4OH-═AlO2-+2H2O | |
| D. | 金属钠与水反应:2Na+2 H2O═2Na++2OH-+H2↑ |
2.绿矾(FeSO4•7H2O)是治疗缺铁性贫血药品中的重要成分.下面是以市售铁屑(含少量锡、氧化铁等杂质)为原料生产纯净绿矾的一种方法:
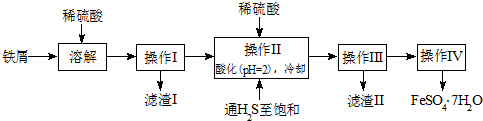
已知:室温下饱和H2S溶液的pH约为3.9;SnS沉淀完全时溶液的pH为1.6;FeS开始沉淀时溶液的pH为3.0,沉淀完全时的pH为5.5.
请回答下列问题:
(一)绿矾的制备
(1)检验制得的绿矾中是否含有Fe3+的实验操作是取少量溶于水配成溶液,滴加1~2滴KSCN溶液,振荡,若变为红色溶液则含有Fe3+,否则不含Fe3+.
(2)操作II中,通入硫化氢至饱和的目的是把Fe3+还原成Fe2+,除去溶液中的Sn2+,并防止Fe2+被氧化;在溶液中用硫酸酸化至pH=2的目的是防止Fe2+生成沉淀.
(3)操作IV的顺序依次为:蒸发浓缩、冷却结晶、过滤洗涤.
(二)绿矾中FeSO4•7H2O含量的测定
若用容量法测定绿矾中FeSO4•7H2O的含量.滴定反应是:5Fe2++MnO4-+8H+═5Fe3++Mn2++4H2O
实验方案如下:
①称取15.041g绿矾产品,溶解,在250mL容量瓶中定容.
②量取25.00mL待测溶液于锥形瓶中.
③用0.0500mol/L KMnO4溶液(硫酸酸化)滴定至终点,记录初读数和末读数.
④重复操作②③1~2次或做平行实验1~2次.
⑤数据处理.
(4)上述实验方案中的步骤④是重复操作②③1~2次或做平行实验1~2次.
(5)洁净的滴定管在滴定前必须进行的操作有:
①检验活塞是否漏水;②用蒸馏水洗涤2~3次,再用高锰酸钾标准溶液润洗滴定管2~3次;
③向滴定管中加入KMnO4标准溶液到0刻度以上,赶走尖嘴部位的气泡,调液面至0或0刻度线以下,初读数.
(三)数据处理
某小组同学的实验数据记录如下:(FeSO4•7H2O的摩尔质量为278g/mol)
(6)上述样品中FeSO4•7H2O的质量分数为0.975(用小数表示,保留三位小数).

已知:室温下饱和H2S溶液的pH约为3.9;SnS沉淀完全时溶液的pH为1.6;FeS开始沉淀时溶液的pH为3.0,沉淀完全时的pH为5.5.
请回答下列问题:
(一)绿矾的制备
(1)检验制得的绿矾中是否含有Fe3+的实验操作是取少量溶于水配成溶液,滴加1~2滴KSCN溶液,振荡,若变为红色溶液则含有Fe3+,否则不含Fe3+.
(2)操作II中,通入硫化氢至饱和的目的是把Fe3+还原成Fe2+,除去溶液中的Sn2+,并防止Fe2+被氧化;在溶液中用硫酸酸化至pH=2的目的是防止Fe2+生成沉淀.
(3)操作IV的顺序依次为:蒸发浓缩、冷却结晶、过滤洗涤.
(二)绿矾中FeSO4•7H2O含量的测定
若用容量法测定绿矾中FeSO4•7H2O的含量.滴定反应是:5Fe2++MnO4-+8H+═5Fe3++Mn2++4H2O
实验方案如下:
①称取15.041g绿矾产品,溶解,在250mL容量瓶中定容.
②量取25.00mL待测溶液于锥形瓶中.
③用0.0500mol/L KMnO4溶液(硫酸酸化)滴定至终点,记录初读数和末读数.
④重复操作②③1~2次或做平行实验1~2次.
⑤数据处理.
(4)上述实验方案中的步骤④是重复操作②③1~2次或做平行实验1~2次.
(5)洁净的滴定管在滴定前必须进行的操作有:
①检验活塞是否漏水;②用蒸馏水洗涤2~3次,再用高锰酸钾标准溶液润洗滴定管2~3次;
③向滴定管中加入KMnO4标准溶液到0刻度以上,赶走尖嘴部位的气泡,调液面至0或0刻度线以下,初读数.
(三)数据处理
某小组同学的实验数据记录如下:(FeSO4•7H2O的摩尔质量为278g/mol)
| 实验次数 | 初读数(mL) | 末读数(mL) |
| 1 | 0.20 | 21.40 |
| 2 | 0.00 | 21.00 |
| 3 | 1.60 | 26.60 |
1.常温下,现有电解质溶液:①NaClO ②NaOH ③NaHCO3 ④CH3COONa,当几种溶液的pH相同时,其物质的量浓度由大到小的顺序排列正确的是( )
| A. | ②①③④ | B. | ①③④② | C. | ④③①② | D. | ③④②① |
19.下列表达正确的是( )
| A. | NaHS在水中的电离方程式为:NaHS═Na++H++S2- | |
| B. | 已知某温度下Ksp(CH3COOAg)=2.8×10-3,此温度下浓度均为0.1 mol•L-1的AgNO3溶液和CH3COONa溶液等体积混合一定能产生CH3COOAg沉淀 | |
| C. | 0.1mol/L CH3COOH溶液与0.05mol/L NaOH溶液等体积混合,所得溶液中:2c(H+)+c(CH3COOH)=c(CH3COO-)+2c(OH-) | |
| D. | 0.2mol/LNH3•H2O溶液与0.1mol/L盐酸等体积混合后,溶液显碱性,则:c(Cl-)>c(NH4+)>c(H+)>c(OH-) |
18.下列说法中不正确的是( )
| A. | 对氯甲苯、1,2-二氯乙烷、3-甲基-1-丁烯的结构简式分别为: 、CH2Cl-CH2Cl、 、CH2Cl-CH2Cl、 | |
| B. | 2,3,4一三甲基戊烷的核磁共振氢谱中出现四组峰 | |
| C. | 3,4一二甲基己烷的一氯代产物有4种 | |
| D. | 甲苯、硝基苯、2-甲基丙烯分子中的所有碳原子处于同一平面上 |
17. 人们研究金星大气成分,发现金星大气中有一种称之为羰基硫(COS)的分子,已知羰基硫分子中所有原子的最外层都满足8电子结构,结合已学知识,判断有关说法正确的是( )
人们研究金星大气成分,发现金星大气中有一种称之为羰基硫(COS)的分子,已知羰基硫分子中所有原子的最外层都满足8电子结构,结合已学知识,判断有关说法正确的是( )
 人们研究金星大气成分,发现金星大气中有一种称之为羰基硫(COS)的分子,已知羰基硫分子中所有原子的最外层都满足8电子结构,结合已学知识,判断有关说法正确的是( )
人们研究金星大气成分,发现金星大气中有一种称之为羰基硫(COS)的分子,已知羰基硫分子中所有原子的最外层都满足8电子结构,结合已学知识,判断有关说法正确的是( )| A. | 羰基硫属于非极性分子 | |
| B. | 羰基硫的电子式为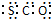 | |
| C. | 羰基硫的沸点比CO2低 | |
| D. | 羰基硫分子中三个原子处于同一直线上 |
16.构造原理揭示的电子排布能级顺序,实质是各能级能量高低.若以E(nl)表示某能级的能量,以下各式中正确的是( )
| A. | E(5s)>E(4f)>E(4s)>E(3d) | B. | E(4f)>E(3d)>E(4s)>E(3p) | C. | E(5d)>E(4d)>E(3d)>E(2d) | D. | E(5s)>E(4s)>E(4f)>E(3d) |
14.下列A、B两种元素的原子序数,其中可以组成AB2型离子化合物的( )
0 156567 156575 156581 156585 156591 156593 156597 156603 156605 156611 156617 156621 156623 156627 156633 156635 156641 156645 156647 156651 156653 156657 156659 156661 156662 156663 156665 156666 156667 156669 156671 156675 156677 156681 156683 156687 156693 156695 156701 156705 156707 156711 156717 156723 156725 156731 156735 156737 156743 156747 156753 156761 203614
| A. | 6和8 | B. | 19和16 | C. | 12和17 | D. | 7和8 |
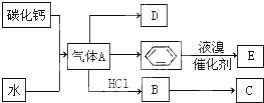
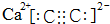 ;D的空间构型为平面结构,键角为120°;
;D的空间构型为平面结构,键角为120°; +Br2 $\stackrel{FeBr_{3}}{→}$
+Br2 $\stackrel{FeBr_{3}}{→}$ +HBr,其反应类型为取代反应
+HBr,其反应类型为取代反应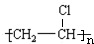 其反应类型为加聚反应
其反应类型为加聚反应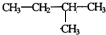 .
.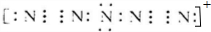 .
.