3.下列关于浓硫酸的叙述中,正确的是( )
| A. | 常温时与锌反应生成大量氢气 | |
| B. | 置于敞口容器中,经过一段时间后质量将减少 | |
| C. | 常温时与铁、铝不反应 | |
| D. | 稀释时将浓硫酸沿器壁慢慢加到水中并不断搅拌 |
20.如图所示的装置能够组成原电池的是( )
| A. | 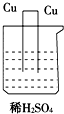 | B. | 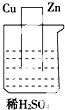 | C. | 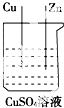 | D. | 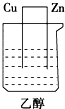 |
19.下列叙述不正确的是( )
| A. | 液氨汽化吸热,故液氨常做制冷剂 | |
| B. | 为防止粮食、罐头、水果等食品腐烂,常用氮气做保护气 | |
| C. | 浓硝酸和浓硫酸与铜反应都能表现出强氧化性和酸性 | |
| D. | 实验室可用氯化铵固体与氢氧化钠固体共热制氨气 |
18.1L水中溶有Mg(HCO3)2和CaCl2的浓度分别是b mol/L和2b mol/L,现用一种试剂(适量)把Ca2+、Mg2+除去,这种试剂最好选用( )
| A. | Ca(OH)2 | B. | NaOH | C. | NaHCO3 | D. | Na2CO3 |
17.NA为阿伏加德罗常数的值,下列说法正确的是( )
| A. | 一定条件下,将1 mol N2和3 mol H2混合,充分反应后转移的电子数为6NA | |
| B. | 6.4 g由S2、S4、S8组成的混合物含硫原子数为0.2 NA | |
| C. | 0.1mol/LNH4Cl溶液中Cl-离子数为0.1NA | |
| D. | 2.24LNH3和CH4的混合气体,所含电子数为2NA |
15.下列各组中属于同位素的是( )
| A. | 40K与40Ca | B. | 35Cl2和37Cl2 | C. | D与T | D. | O3和O2 |
14.铝土矿是工业炼铝的主要原料,某铝土矿样品组成如下:
主要成分:Al2O3杂质:Fe2O3、SiO2及其他不溶且不参与化学反应的物质为测定该样品中Al的含量,某化学兴趣小组设计了如下两个方案:
【查阅资料】各相关离子开始沉淀和沉淀完全时溶液的pH如表:
方案一:将铝土矿加足量盐酸溶解,再调节pH,使Fe3+沉淀完全而Al3+不沉淀.需调节pH范围应是3.2~3.4,若想得到氯化铝固体需将其溶液通入HCl气流中直至蒸干.
方案二:

(1)②反应的离子方程式为OH-+CO2=CO32-+H2O,2AlO2-+CO2+3H2O=CO32-+2Al(OH)3↓.CO2不可过量的原因是防止SiO32-被沉淀.
(2)若在步骤②中加入乙酸乙酯调节pH,加热也可得到d的沉淀,写出生成d沉淀的化学方程式AlO2-+CH3COOCH2CH3+2H2O$\frac{\underline{\;\;△\;\;}}{\;}$CH3COO-+Al(OH)3↓+CH3CH2OH.
0 156563 156571 156577 156581 156587 156589 156593 156599 156601 156607 156613 156617 156619 156623 156629 156631 156637 156641 156643 156647 156649 156653 156655 156657 156658 156659 156661 156662 156663 156665 156667 156671 156673 156677 156679 156683 156689 156691 156697 156701 156703 156707 156713 156719 156721 156727 156731 156733 156739 156743 156749 156757 203614
主要成分:Al2O3杂质:Fe2O3、SiO2及其他不溶且不参与化学反应的物质为测定该样品中Al的含量,某化学兴趣小组设计了如下两个方案:
【查阅资料】各相关离子开始沉淀和沉淀完全时溶液的pH如表:
| Al3+ | Fe3+ | AlO2- | SiO32- | |
| 开始沉淀时 | 3.4 | 1.9 | 10.6 | 7.3 |
| 沉淀完全时 | 4.7 | 3.2 | 9.3 | 5.3 |
方案二:

(1)②反应的离子方程式为OH-+CO2=CO32-+H2O,2AlO2-+CO2+3H2O=CO32-+2Al(OH)3↓.CO2不可过量的原因是防止SiO32-被沉淀.
(2)若在步骤②中加入乙酸乙酯调节pH,加热也可得到d的沉淀,写出生成d沉淀的化学方程式AlO2-+CH3COOCH2CH3+2H2O$\frac{\underline{\;\;△\;\;}}{\;}$CH3COO-+Al(OH)3↓+CH3CH2OH.