13.下列反应属于吸热反应的是( )
| A. | Mg与盐酸反应 | B. | NH4Cl的分解反应 | ||
| C. | Na在Cl2燃烧 | D. | NaOH溶液与CH3COOH溶液反应 |
12.关于σ键和π键的比较,下列说法不正确的是( )
| A. | σ键是轴对称的,π键是镜像对称的 | |
| B. | σ键是“头碰头”式重叠,π键是“肩并肩”式重叠 | |
| C. | σ键不能断裂,π键容易断裂 | |
| D. | H原子只能形成σ键,O原子可以形成σ键和π键 |
11.价层电子对互斥理论(简称VSEPR理论)可用于预测简单分子的立体构型.其要点可以概括为:
Ⅰ.用AXnEm表示只含一个中心原子的分子组成,A为中心原子,X为与中心原子相结合的原子,E为中心原子最外层未参与成键的电子对(称为孤电子对),(n+m)称为价层电子对数.分子中的价层电子对总是互相排斥,均匀地分布在中心原子周围的空间;
Ⅱ.分子的空间构型是指分子中的原子在空间的排布,不包括中心原子未成键的孤电子对;
Ⅲ.分子中价层电子对之间的斥力主要顺序为:
ⅰ.孤电子对之间的斥力>孤电子对与共用电子对之间的斥力>共用电子对之间的斥力;ⅱ.双键与双键之间的斥力>双键与单键之间的斥力>单键与单键之间的斥力;ⅲ.X原子得电子能力越弱,A-X形成的共用电子对之间的斥力越强;ⅳ.其他.请仔细阅读上述材料,回答下列问题:
(1)根据要点Ⅰ可以画出AXnEm的VSEPR理想模型,请填写下表:
(2)请用VSEPR模型解释CO2为直线形分子的原因:CO2属AX2E0,n+m=2,故为直线形;
(3)用价层电子对互斥理论(VSEPR)判断下列分子或离子的空间构型:
Ⅰ.用AXnEm表示只含一个中心原子的分子组成,A为中心原子,X为与中心原子相结合的原子,E为中心原子最外层未参与成键的电子对(称为孤电子对),(n+m)称为价层电子对数.分子中的价层电子对总是互相排斥,均匀地分布在中心原子周围的空间;
Ⅱ.分子的空间构型是指分子中的原子在空间的排布,不包括中心原子未成键的孤电子对;
Ⅲ.分子中价层电子对之间的斥力主要顺序为:
ⅰ.孤电子对之间的斥力>孤电子对与共用电子对之间的斥力>共用电子对之间的斥力;ⅱ.双键与双键之间的斥力>双键与单键之间的斥力>单键与单键之间的斥力;ⅲ.X原子得电子能力越弱,A-X形成的共用电子对之间的斥力越强;ⅳ.其他.请仔细阅读上述材料,回答下列问题:
(1)根据要点Ⅰ可以画出AXnEm的VSEPR理想模型,请填写下表:
| n+m | 2 | |
| VSEPR理想模型 | 正四面体形 | |
| 价层电子对 之间的理想键角 | 109°28′ |
(3)用价层电子对互斥理论(VSEPR)判断下列分子或离子的空间构型:
| 分子 | |||
| 或离子 | SnCl2 | CCl4 | ClO${\;}_{4}^{-}$ |
| 立体构型 |
10.A、B为同主族的两元素,A在B的上一周期,若A的原子序数为n,则B的原子序数不可能为( )
| A. | n+8 | B. | n+16 | C. | n+18 | D. | n+32 |
8.“长征二号”火箭所用的主要燃料叫做“偏二甲肼”,已知该化合物的相对分子质量为60,其中含碳的质量分数为40%,氢的质量分数为13.33%,其余是氮元素,则“偏二甲肼”的化学式为( )
| A. | C2H8N2 | B. | CH4N | C. | C3H10N | D. | CH6N3 |
4.下列化合物分子,在核磁共振氢谱图中能给出三种信号峰的是( )
0 156562 156570 156576 156580 156586 156588 156592 156598 156600 156606 156612 156616 156618 156622 156628 156630 156636 156640 156642 156646 156648 156652 156654 156656 156657 156658 156660 156661 156662 156664 156666 156670 156672 156676 156678 156682 156688 156690 156696 156700 156702 156706 156712 156718 156720 156726 156730 156732 156738 156742 156748 156756 203614
| A. | CH3CH2CH3 | B. | CH3-O-CH3 | C. | 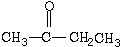 | D. | 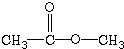 |
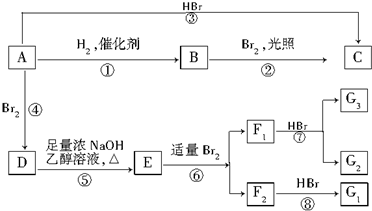
 )(F1和F2互为同分异构体)(G1和G2互为同分异构体)
)(F1和F2互为同分异构体)(G1和G2互为同分异构体) .
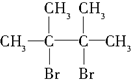
.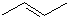 某有机物X的键线式为
某有机物X的键线式为 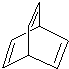
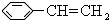 ,该芳香烃Z在一定条件下可发生聚合反应,写出其反应的化学方程
,该芳香烃Z在一定条件下可发生聚合反应,写出其反应的化学方程 .
.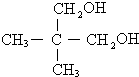 .
.