17.下列有关物质性质的说法错误的是( )
| A. | 酸性:H2SO4>HClO4 | B. | 原子半径:Na>Mg | ||
| C. | 热稳定性:HCl>HI | D. | 还原性:S2->Cl- |
16.下列有关NH4Fe(SO4)2水溶液的叙述正确的是( )
| A. | 该溶液中,H+、Mg2+、NO3-、Cl-可以大量共存 | |
| B. | 该溶液能使红色石蕊试纸变蓝,也能使淀粉碘化钾试纸变蓝 | |
| C. | 该溶液和足量Ba(OH)2溶液反应的离子方程式为:Fe3++SO42-+Ba2++3OH-═Fe(OH)3↓+BaSO4↓ | |
| D. | 该溶液与过量锌粉反应的离子方程式为:Zn+2Fe3+═2Fe2++Zn2+ |
15.NA代表阿伏加德罗常数,下列叙述正确的是( )
| A. | 0.1 mol丙烯酸中含有双键的数目为0.1NA | |
| B. | 常温常压下,Cu、Zn、稀硫酸构成的原电池中,正极产生1.12 L H2时,转移的电子数应为0.1NA | |
| C. | 一定条件下定容容器中充入3molH2(g)和1 mol N2(g)发生反应:H2(g)+N2(g)?2NH3 (g);△H=-QkJ/mol,当该反应放出0.25QkJ的热量时,容器中的氢分子数共有2.75 NA | |
| D. | 在50 g质量分数为46%的乙醇水溶液中,含有的氢原子总数为6NA |
14.为了提纯下列物质(括号内为杂质),有关除杂试剂和分离方法的选择均正确的是( )
| 选项 | 被提纯的物质 | 除杂试剂 | 分离方法 |
| A | 溴苯(溴) | 水 | 分液 |
| B | 乙酸乙酯(乙酸) | NaOH溶液 | 分液 |
| C | 苯(苯酚) | NaOH溶液 | 分液 |
| D | 甲烷(乙烯) | KMnO4酸性溶液 | 洗气 |
| A. | A | B. | B | C. | C | D. | D |
13.100mL6mol/LH2SO4跟过量的锌粉反应,在一定温度下,为了减缓反应速率,但又不影响生成氢气的总量.可向反应物中加入适量的( )
| A. | 碳酸钠(固体) | B. | 水 | C. | 硫酸钾溶液 | D. | 硫酸铵(固体) |
12.已知C3N4晶体很可能具有比金刚石更大的硬度,且原子间以单键结合.下列有关C3N4晶体的说法中正确的是( )
| A. | C3N4晶体是分子晶体 | |
| B. | C 原子sp3杂化,与4个处于4面体顶点的N 原子形成共价键 | |
| C. | C3N4晶体中C、N原子个数之比为4:3 | |
| D. | C3N4晶体中粒子间通过离子键结合 |
11.判断下列说法不正确的是( )
| A. | 干冰熔化或升华时,CO2分子内的C=O键会被破坏 | |
| B. | 乙炔与氢气反应会变成乙烯,碳原子的杂化类型由sp变为sp2 | |
| C. | 物质的状态变化,只需克服分子间作用力 | |
| D. | 分子中不可能含有离子键 |
10.下列常见分子的中心原子的杂化轨道类型是SP3的是( )
| A. | NH4+ | B. | CH4 | C. | SO2 | D. | CO2 |
8.常温下,0.1mol•L-1的下列溶液中,有关微粒的物质的量浓度关系正确的是( )
0 156555 156563 156569 156573 156579 156581 156585 156591 156593 156599 156605 156609 156611 156615 156621 156623 156629 156633 156635 156639 156641 156645 156647 156649 156650 156651 156653 156654 156655 156657 156659 156663 156665 156669 156671 156675 156681 156683 156689 156693 156695 156699 156705 156711 156713 156719 156723 156725 156731 156735 156741 156749 203614
| A. | NH4Cl溶液:c(Cl-)>c(NH4+)>c(OH-)>c(H+) | |
| B. | (NH4)2Fe(SO4)2溶液:c(SO42-)>c(NH4+)>c(Fe2+)>c(H+) | |
| C. | Na2CO3溶液:c(Na+)+c(H+)=c(CO32-)+c(HCO3-)+c(OH-) | |
| D. | NaHCO3溶液:c(H+)+c(H2CO3)=c(OH-)+c(CO32-) |
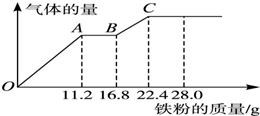 某稀硫酸和稀硝酸的混合溶液200mL,向其中逐渐加入铁粉,产生气体的量随铁粉质量增加的变化如图所示.
某稀硫酸和稀硝酸的混合溶液200mL,向其中逐渐加入铁粉,产生气体的量随铁粉质量增加的变化如图所示.