7.短周期元素X和Y可组成化合物XY2,X的原子序数为a时,Y的原子序数可能为( )
①a+1 ②a+2 ③a+5 ④a-3 ⑤a-6 ⑥a-8.
①a+1 ②a+2 ③a+5 ④a-3 ⑤a-6 ⑥a-8.
| A. | ②③④⑤⑥ | B. | ②③④⑤ | C. | ①②③④⑤ | D. | ①②③④⑤⑥ |
6.用NA代表阿伏加德罗常数的值,下列有关说法正确的是( )
| A. | 3mol NO2与足量H2O反应,转移的电子数为NA | |
| B. | 常温常压下,22.4L氦气含有NA个氦原子 | |
| C. | 锂在氧气中燃烧,1 mol O2作氧化剂时得到的电子数为2NA | |
| D. | 常温常压下,17克NH3中含有共价键的数目为3NA |
5.反应4NH3(g)+5O2(g)═4NO(g)+6H2O(g)在10L的密闭容器中进行,半分钟后,水蒸气的物质的量增加了0.45mol,则此反应的平均速率v(x)(反应物的消耗速率或产物的生成速率)可表示为( )
| A. | v(NH3)=0.010mol/(L•s) | B. | v(O2)=0.0010mol/(L•s) | ||
| C. | v(NO)=0.0010mol/(L•s) | D. | v(H2O)=0.045mol/(L•s) |
2.在标准状况下进行甲、乙、丙三组实验,三组各取30mL同浓度的盐酸溶液,加入同一种镁铝合金粉末,产生气体,有关数据列表如下:
(1)甲组实验中,盐酸过量 (填“过量”“适量”或“不足量”),乙组实验中,盐酸不足量(填“过量”“适量”或“不足量”).参考合适的数据计算出盐酸的物质的量浓度为1mol/L.
(2)参考合适的数据组合求得的Mg、Al的物质的量之比为1:1.
(3)在丙组实验之后,向容器中加入1mol•L-1的氢氧化钠溶液,能使合金中的铝恰好溶解,不形成含铝的沉淀,并使Mg2+刚好沉淀完全,再过滤出不溶固体,求滤液中各溶质的物质的量和所加入氢氧化钠溶液的体积.
| 实验序号 | 甲 | 乙 | 丙 |
| 合金质量(mg) | 255 | 385 | 459 |
| 生成气体体积(mL) | 280 | 336 | 336 |
(2)参考合适的数据组合求得的Mg、Al的物质的量之比为1:1.
(3)在丙组实验之后,向容器中加入1mol•L-1的氢氧化钠溶液,能使合金中的铝恰好溶解,不形成含铝的沉淀,并使Mg2+刚好沉淀完全,再过滤出不溶固体,求滤液中各溶质的物质的量和所加入氢氧化钠溶液的体积.
1.下列说法正确的是( )
| A. | S在纯氧中燃烧可生成SO3 | |
| B. | 用澄清石灰水可鉴别CO2和SO2 | |
| C. | SO2能使KMnO4溶液褪色 | |
| D. | CO2通入CaCl2溶液中能产生白色沉淀考点:考查S、SO2、CO2的性质以及鉴别 |
18.下列关于苯的性质的说法中,正确的是( )
| A. | 苯不溶于水,密度比水大 | |
| B. | 苯在空气中燃烧产生大量的黑烟 | |
| C. | 苯与溴水能发生加成反应生成溴苯 | |
| D. | 苯分子中存在碳碳双键,故能使酸性KMnO4溶液褪色 |
17.1molM(表示金属单质)溶于某种浓度的硝酸中,生成dmolM2+、fmolM3+、gmolNO、hmolNO2,下列有关叙述中,不正确的是( )
0 156542 156550 156556 156560 156566 156568 156572 156578 156580 156586 156592 156596 156598 156602 156608 156610 156616 156620 156622 156626 156628 156632 156634 156636 156637 156638 156640 156641 156642 156644 156646 156650 156652 156656 156658 156662 156668 156670 156676 156680 156682 156686 156692 156698 156700 156706 156710 156712 156718 156722 156728 156736 203614
| A. | 反应中生成(2g+h)molH2O | B. | 2d+3f=3g+h | ||
| C. | 2<3g+h<3 | D. | h随着d增大而增大 |
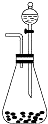 如图是一套实验室制气装置,某课外活动小组欲利用这套装置快速制取氧气和氯化氢气体,供选用的试剂有:A.浓H2SO4,B.浓盐酸,C.食盐,D.MnO2,?E.H2O2(aq)?,F.KClO3,G.KMnO4溶液,试完成下列问题:
如图是一套实验室制气装置,某课外活动小组欲利用这套装置快速制取氧气和氯化氢气体,供选用的试剂有:A.浓H2SO4,B.浓盐酸,C.食盐,D.MnO2,?E.H2O2(aq)?,F.KClO3,G.KMnO4溶液,试完成下列问题: