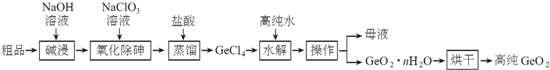
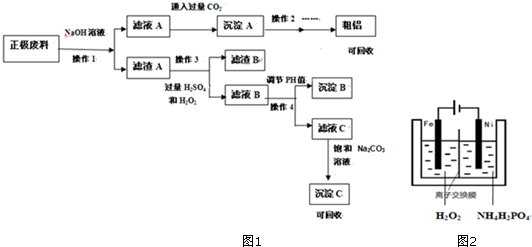
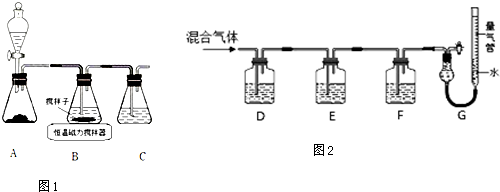
16.按官能团分类,下列说法不正确的是( )
| A. | 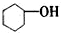 属于醇类 属于醇类 | B. |  属于羧酸 属于羧酸 | C. | 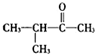 属于酮类 属于酮类 | D. |  属于酚类 属于酚类 |
15.新兴大脑营养学研究表明:大脑的发育与生长与不饱和脂肪有密切的联系,从深海鱼油中提取的被称作“脑黄金”的DHA就是一种不饱和程度很高的脂肪酸,它的分子中含6个碳碳双键,化学名称为:二十六碳六烯酸,它的分子组成应是( )
| A. | C25H50COOH | B. | C26H47COOH | C. | C26H41COOH | D. | C25H39COOH |
14.Y是一种皮肤病用药,它可以由原料X经过多步反应合成.

下列说法正确的是( )

下列说法正确的是( )
| A. | X与Y互为同分异构体 | |
| B. | 1mol X最多可以与5mol H2发生加成反应 | |
| C. | 产物Y能发生氧化、加成、取代、消去反应 | |
| D. | 1 molY最多能与2mol NaOH发生反应 |
13.X、Y、Z、W均为短周期元素,原子序数依次递增.X与W位于同一主族,Y、Z、W同周期,Z原子的最外层电子数是最内层电子数的3倍,Y、Z、W原子的最外层电子数之和为15.下列说法正确的是( )
0 156537 156545 156551 156555 156561 156563 156567 156573 156575 156581 156587 156591 156593 156597 156603 156605 156611 156615 156617 156621 156623 156627 156629 156631 156632 156633 156635 156636 156637 156639 156641 156645 156647 156651 156653 156657 156663 156665 156671 156675 156677 156681 156687 156693 156695 156701 156705 156707 156713 156717 156723 156731 203614
| A. | X的最高价氧化物对应水化物的酸性大于W | |
| B. | Z的气态氢化物的稳定性大于W | |
| C. | YZ和ZW2所含化学键类型相同 | |
| D. | 简单离子半径:r(Y2+)<r(X-)<r(W-)<r(Z2-) |