8.下列说法中正确的是( )
| A. | 元素周期表是按相对原子质量逐渐增大的顺序从左到右排列的 | |
| B. | 最外层电子数相同的元素一定属于同一族 | |
| C. | 非金属元素的最外层电子数都大于或等于4 | |
| D. | 同周期元素的电子层数相同 |
7.在一定温度下的定容密闭容器中,当下列物理量不再变化时,不能表明反应A(s)+2B(g)?C(g)+D(g)已达到平衡的是( )
| A. | 混合气体的压强 | B. | 混合气体的密度 | ||
| C. | 气体的平均摩尔质量 | D. | 反应物A的质量 |
5.铁盐是中学化学常见的盐.下面是以富含硫酸亚铁的工业废液为原料生产氧化铁和制备草酸亚铁晶体(FeC2O3•xH2O )的工艺流程图(部分操作和条件略).

请回答下列问题:
已知:①pH>4时,Fe2+易被氧气氧化;②NH4HCO3在热水中会分解;
③几种物质的溶解度(g/l00g H2O)如下
(1)流程图步骤Ⅰ中,在提纯时需要加足量的铁屑的原因是除去废液中的2Fe3+(或Fe+2Fe3+=3Fe2+).
(2)在生产氧化铁的步骤Ⅲ中,生成FeCO3的离子方程式是Fe2++2HCO3-=FeCO3↓+CO2↑+H2O.
(3)上述流程图制备草酸亚铁过程中,用稀硫酸调溶液pH至1〜2的目的是防止亚铁离子水解,防止亚铁离子氧化趁热过滤的原因是增大杂质的溶解度(防止低温时杂质析出),影响产品的纯度.
(4)己知煅烧FeCO3的化学方程式是4FeCO3+O2═2Fe2O3+4CO2.现煅烧464.0kg的FeCO3,得到316.8kg产品.若产品中杂质只有FeO.则该产品中Fe2O3的质量是288.0kg.
(5)已知:某温度时,Ksp(FeC2O4)=1.0×10-6.Ksp(CaC2O4)=2.0×10-9,此温度下,FeC2O4若要在CaCl2溶液中开始转化为CaC2O4,则CaCl2的浓度必须不低于2.0×10-6mol•L-1.
(6)草酸(HzC2O4)是一种二元弱酸,广泛分布于动植物体中.已知0.1mol•L-1KHC2O4溶液呈酸性.下列说法正确的是ac(填字母序号)a、0.1mol•L-1KHC2O4溶液中:c(K+)+c(H+)═c(HC2O4-)+2c(C2O42-)+c(OH- )
b.0.1mol•L-1KHC2O4溶液中:c(K+)>c(HC2O4-)>c((H2C2O4)>c(C2O42-)
C.0.1mol/LKHC2O4溶液中滴加等浓度NaOH溶液至中性:c(K+)>c(Na+)
d.浓度均为0.lmol•L-1KHC2O4和K2C2O4的混合溶液中:2c(K+)═c(HC2O4-)+c(C2O42-)

请回答下列问题:
已知:①pH>4时,Fe2+易被氧气氧化;②NH4HCO3在热水中会分解;
③几种物质的溶解度(g/l00g H2O)如下
| FeS04•7H2O | (NH4)2SO4 | FeSO4•(NH4)2SO4•6H2O | |
| 20℃ | 48 | 75 | 37 |
| 60℃ | 101 | 88 | 38 |
(2)在生产氧化铁的步骤Ⅲ中,生成FeCO3的离子方程式是Fe2++2HCO3-=FeCO3↓+CO2↑+H2O.
(3)上述流程图制备草酸亚铁过程中,用稀硫酸调溶液pH至1〜2的目的是防止亚铁离子水解,防止亚铁离子氧化趁热过滤的原因是增大杂质的溶解度(防止低温时杂质析出),影响产品的纯度.
(4)己知煅烧FeCO3的化学方程式是4FeCO3+O2═2Fe2O3+4CO2.现煅烧464.0kg的FeCO3,得到316.8kg产品.若产品中杂质只有FeO.则该产品中Fe2O3的质量是288.0kg.
(5)已知:某温度时,Ksp(FeC2O4)=1.0×10-6.Ksp(CaC2O4)=2.0×10-9,此温度下,FeC2O4若要在CaCl2溶液中开始转化为CaC2O4,则CaCl2的浓度必须不低于2.0×10-6mol•L-1.
(6)草酸(HzC2O4)是一种二元弱酸,广泛分布于动植物体中.已知0.1mol•L-1KHC2O4溶液呈酸性.下列说法正确的是ac(填字母序号)a、0.1mol•L-1KHC2O4溶液中:c(K+)+c(H+)═c(HC2O4-)+2c(C2O42-)+c(OH- )
b.0.1mol•L-1KHC2O4溶液中:c(K+)>c(HC2O4-)>c((H2C2O4)>c(C2O42-)
C.0.1mol/LKHC2O4溶液中滴加等浓度NaOH溶液至中性:c(K+)>c(Na+)
d.浓度均为0.lmol•L-1KHC2O4和K2C2O4的混合溶液中:2c(K+)═c(HC2O4-)+c(C2O42-)
4.现拟在实验室里利用空气和镁粉为原料,制取少量纯净的氮化镁(Mg3N2).已知实验中加热条件下可能发生的以下反应:
可供选择的装置和药品如图所示(镁粉和还原铁粉均已干燥,装置内所发生的反应都是完全的,整套装置的末端与干燥管相连接),请回答下列问题:
(1)为了实现实验目的,在设汁实验方案时,除装置A、E、F外,还应选择的装置有B、D(填字母代号);选择装置F的目的是为了除去空气中的氧气.
(2)连接并检査装置的气密性.实验开始时,打开自来水的开关,将空气从储气瓶压入反应装置,则气流流经导管的顺序是j→h→g→d→c→k→l(或l→k)→a→b(或b→a)(填字母代号).
(3)通入气体后,如果同时点燃A、F装置的酒精灯,对实验结果中所得产品的质量比理论值大 (填“大“或“小”),其一原因是同时点燃酒精灯,A中硬质玻璃管中的空气没有排净,其中的氧气、少量二氧化碳和水蒸气与镁反应,生成了氧化镁.另一原因是由于镁全部本该生成氮化镁,装置F中的还原铁粉没有达到反应温度时,氧气不能除尽,导致氧气与装置A中的镁粉反应,使部分镁生成了氧化镁.
(4)请设计一个实验,验证产物是氮化镁:取适量产物放入试卷中,滴加蒸馏水,将湿润的红色石蕊试纸靠近试管口,如果试管中的溶液出现浑浊,红色石蕊试纸变蓝,则可以证明有氮化镁生成.
| 反应物 | 生成物 | 反应物 | 生成物 |
| 镁和氧气 | 氧化镁 | 镁和水 | 氧化镁和氢气 |
| 镁和氮气 | 氮化镁 | 氮化镁和水 | 氢氧化镁和氨气 |
| 镁和二氧化碳 | 氧化镁和碳 |

(1)为了实现实验目的,在设汁实验方案时,除装置A、E、F外,还应选择的装置有B、D(填字母代号);选择装置F的目的是为了除去空气中的氧气.
(2)连接并检査装置的气密性.实验开始时,打开自来水的开关,将空气从储气瓶压入反应装置,则气流流经导管的顺序是j→h→g→d→c→k→l(或l→k)→a→b(或b→a)(填字母代号).
(3)通入气体后,如果同时点燃A、F装置的酒精灯,对实验结果中所得产品的质量比理论值大 (填“大“或“小”),其一原因是同时点燃酒精灯,A中硬质玻璃管中的空气没有排净,其中的氧气、少量二氧化碳和水蒸气与镁反应,生成了氧化镁.另一原因是由于镁全部本该生成氮化镁,装置F中的还原铁粉没有达到反应温度时,氧气不能除尽,导致氧气与装置A中的镁粉反应,使部分镁生成了氧化镁.
(4)请设计一个实验,验证产物是氮化镁:取适量产物放入试卷中,滴加蒸馏水,将湿润的红色石蕊试纸靠近试管口,如果试管中的溶液出现浑浊,红色石蕊试纸变蓝,则可以证明有氮化镁生成.
2.硼有两种天然同位素${\;}_{5}^{10}$B和${\;}_{5}^{11}$B,硼元素的近似相对原子质量为10.80,则${\;}_{5}^{11}$B的质量百分比是( )
| A. | 80% | B. | 大于80% | C. | 小于80% | D. | 无法计算 |
1.下列各组中两种微粒所含电子数不相等的是( )
| A. | H3O+和OH - | B. | CO和N2 | C. | HNO2和NO2- | D. | CO2和NO2 |
20.铝制品抗腐蚀性极强,原因是( )
| A. | 铝的金属活动性极差 | B. | 空气中没有能与铝反应的物质 | ||
| C. | 其表面的氧化膜致密 | D. | 铝制品被人为地进行了防腐处理 |
19.化学科学需要借助化学专用语言来描述,下列有关化学用语正确的是( )
0 156504 156512 156518 156522 156528 156530 156534 156540 156542 156548 156554 156558 156560 156564 156570 156572 156578 156582 156584 156588 156590 156594 156596 156598 156599 156600 156602 156603 156604 156606 156608 156612 156614 156618 156620 156624 156630 156632 156638 156642 156644 156648 156654 156660 156662 156668 156672 156674 156680 156684 156690 156698 203614
| A. | 原子核内有10个中子的氧原子:${\;}_{8}^{18}$O | |
| B. | 氧的原子结构示意图: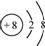 | |
| C. | NaCl的电子式: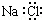 | |
| D. | 质量数为37的氯原子:${\;}_{37}^{17}$Cl |
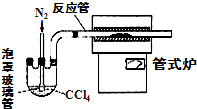 铬主要以铁合金(如铬铁)形式用于生产不锈钢及各种合金钢,铬元素形成的化合物很多,常见的有Cr2O3、CrCl3、H2CrO4,、H2Cr2O7等,请回答下列问题:
铬主要以铁合金(如铬铁)形式用于生产不锈钢及各种合金钢,铬元素形成的化合物很多,常见的有Cr2O3、CrCl3、H2CrO4,、H2Cr2O7等,请回答下列问题: