19.下列有关命名的说法正确的是( )
| A. | 按系统命名法,有机物 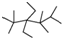 的命名为2,3,3,5,5五甲基-4,4-二乙基己烷 的命名为2,3,3,5,5五甲基-4,4-二乙基己烷 | |
| B. |  主链上的碳原子数是5 主链上的碳原子数是5 | |
| C. | 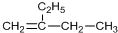 加氢后可以得到3-甲基戊烷 加氢后可以得到3-甲基戊烷 | |
| D. |  的名称是1,3,4-三甲基苯 的名称是1,3,4-三甲基苯 |
18.下列关于同系物的说法不正确的是( )
| A. | 分子式为C3H8与C6H14的两种有机物一定互为同系物 | |
| B. | 具有相同通式的有机物不一定互为同系物 | |
| C. | 含有相同官能团,且相对分子量相差14的有机物一定互为同系物 | |
| D. | 互为同系物的有机物,其化学性质相似 |
14.如图所示装置中,通电后可观察到Cu极溶解,下列说法正确的是( )
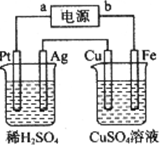

| A. | a极是直流电源的正极 | |
| B. | Fe极是阳极 | |
| C. | Pt极产生的气体体积是Ag极产生气体体积的2倍 | |
| D. | 硫酸铜溶液的浓度变大 |
13.己知氧化还原反应:KClO3+6HCl=KCl+3Cl2↑+3H2O 其中1mol氧化剂在反应中得到的电子为( )
| A. | 1 mol | B. | 5 mol | C. | 6 mol | D. | 2 mol |
12.亚硝酸钠(NaNO2)是一种工业盐,实验室可用如下装置(略去部分夹持仪器)制备.
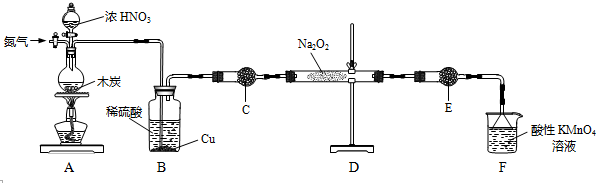
已知:①2NO+Na2O2→2NaNO2
②3NaNO2+3HCl→3NaCl+HNO3+2NO↑+H2O
③5NO${\;}_{2}^{-}$+2MnO${\;}_{4}^{-}$+6H+→NO${\;}_{3}^{-}$+2Mn2++3H2O
④NO和Na2O2都能使酸性高锰酸钾溶液褪色.
⑤实验结束后,将B瓶中的溶液经蒸发浓缩、冷却结晶、过滤可得CuSO4•5H2O.
(1)装置A中发生反应的化学方程式为C+4HNO3(浓) $\frac{\underline{\;\;△\;\;}}{\;}$CO2↑+4NO2↑+2H2O.
(2)反应前检验装置气密性的操作为关闭活塞,用手捂住烧瓶底部,观察B中长导管液面是否下降,加热装置A前,先通一段时间N2,目的是排除装置内的空气.
(3)充分反应后,检验装置D中产物的方法是:取产物少许置于试管中,加入稀硫酸(或稀盐酸),试管内有气泡产生且在试管上方产生红棕色气体,则产物是NaNO2(注明试剂、现象).
(4)为测定产物中亚硝酸钠的含量,称取4.000g产物样品溶于水配成250mL溶液,取25.00mL溶液于锥形瓶中,用0.1000mol•L-1酸性KMnO4溶液进行滴定,实验所得数据如下表所示:
第一组实验数据出现异常,造成这种异常的原因可能是BD(填字母),
A.锥形瓶洗净后未干燥 B.滴定管用蒸馏水洗净后未用标准液润洗
C.振荡时有液体溅出来 D.锥形瓶用蒸馏水洗净后再用待测液润洗
(5)根据表中数据,计算出产物中亚硝酸钠的质量分数86.25%.
(6)设计合理实验比较0.1mol•L-1NaNO2溶液中NO${\;}_{2}^{-}$的水解程度和0.1mol•L-1HNO2溶液中HNO2的电离程度相对大小.(简要说明实验步骤、现象和结论,仪器和药品自选)方法①:配制浓度均为0.1 mol•L-1NaNO2和HNO2的混合液,测溶液的pH,若pH大于7,则NO2-的水解程度大于HNO2的电离程度,若pH<7,则NO2-的水解程度小于HNO2的电离程度.方法②:用pH试纸或pH计分别测定0.1 mol•L-1NaNO2溶液和0.1 mol•L-1HNO2溶液的pH,若HNO2溶液中氢离子浓度大于NaNO2溶液中的氢氧根浓度,则NO2-的水解程度小于HNO2的电离程度,反之,NO2-的水解程度大于HNO2的电离程度.

已知:①2NO+Na2O2→2NaNO2
②3NaNO2+3HCl→3NaCl+HNO3+2NO↑+H2O
③5NO${\;}_{2}^{-}$+2MnO${\;}_{4}^{-}$+6H+→NO${\;}_{3}^{-}$+2Mn2++3H2O
④NO和Na2O2都能使酸性高锰酸钾溶液褪色.
⑤实验结束后,将B瓶中的溶液经蒸发浓缩、冷却结晶、过滤可得CuSO4•5H2O.
(1)装置A中发生反应的化学方程式为C+4HNO3(浓) $\frac{\underline{\;\;△\;\;}}{\;}$CO2↑+4NO2↑+2H2O.
(2)反应前检验装置气密性的操作为关闭活塞,用手捂住烧瓶底部,观察B中长导管液面是否下降,加热装置A前,先通一段时间N2,目的是排除装置内的空气.
(3)充分反应后,检验装置D中产物的方法是:取产物少许置于试管中,加入稀硫酸(或稀盐酸),试管内有气泡产生且在试管上方产生红棕色气体,则产物是NaNO2(注明试剂、现象).
(4)为测定产物中亚硝酸钠的含量,称取4.000g产物样品溶于水配成250mL溶液,取25.00mL溶液于锥形瓶中,用0.1000mol•L-1酸性KMnO4溶液进行滴定,实验所得数据如下表所示:
| 滴定次数 | 1 | 2 | 3 | 4 |
| KMnO4溶液体积/mL | 20.60 | 20.02 | 20.00 | 19.98 |
A.锥形瓶洗净后未干燥 B.滴定管用蒸馏水洗净后未用标准液润洗
C.振荡时有液体溅出来 D.锥形瓶用蒸馏水洗净后再用待测液润洗
(5)根据表中数据,计算出产物中亚硝酸钠的质量分数86.25%.
(6)设计合理实验比较0.1mol•L-1NaNO2溶液中NO${\;}_{2}^{-}$的水解程度和0.1mol•L-1HNO2溶液中HNO2的电离程度相对大小.(简要说明实验步骤、现象和结论,仪器和药品自选)方法①:配制浓度均为0.1 mol•L-1NaNO2和HNO2的混合液,测溶液的pH,若pH大于7,则NO2-的水解程度大于HNO2的电离程度,若pH<7,则NO2-的水解程度小于HNO2的电离程度.方法②:用pH试纸或pH计分别测定0.1 mol•L-1NaNO2溶液和0.1 mol•L-1HNO2溶液的pH,若HNO2溶液中氢离子浓度大于NaNO2溶液中的氢氧根浓度,则NO2-的水解程度小于HNO2的电离程度,反之,NO2-的水解程度大于HNO2的电离程度.
10.硅及其化合物在材料领域中应用广泛,下列叙述中不正确的是( )
0 156488 156496 156502 156506 156512 156514 156518 156524 156526 156532 156538 156542 156544 156548 156554 156556 156562 156566 156568 156572 156574 156578 156580 156582 156583 156584 156586 156587 156588 156590 156592 156596 156598 156602 156604 156608 156614 156616 156622 156626 156628 156632 156638 156644 156646 156652 156656 156658 156664 156668 156674 156682 203614
| A. | 硅单质可用来制造太阳能电池 | |
| B. | 装碱性溶液的玻璃试剂瓶不能用玻璃塞 | |
| C. | 二氧化硅是制造光导纤维的材料 | |
| D. | 自然界硅元素的贮量丰富,并存在大量的单质硅 |
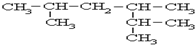
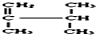 系统名称为2,3-二甲基-1-丁烯;
系统名称为2,3-二甲基-1-丁烯;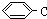 ≡C-CH=CH-CH3,共面的碳原子最多有12个,共线的碳原子最多有6个.
≡C-CH=CH-CH3,共面的碳原子最多有12个,共线的碳原子最多有6个. 表示的分子式C6H14.
表示的分子式C6H14.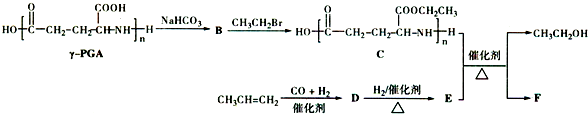
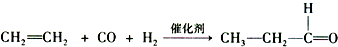
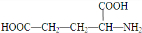 .
.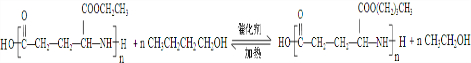 .
.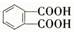 )反应生成的产物DBP(C16H22O4)是广泛使用的增塑剂之一.DBP有多种同分异构体,其中符合下列条件的DBP的同分异构体有12种,写出其中一种同分异构体的结构简式
)反应生成的产物DBP(C16H22O4)是广泛使用的增塑剂之一.DBP有多种同分异构体,其中符合下列条件的DBP的同分异构体有12种,写出其中一种同分异构体的结构简式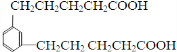 .
.