19.t℃时Ag2CrO4在水中的沉淀溶解平衡曲线如图所示.下列说法正确的是( )
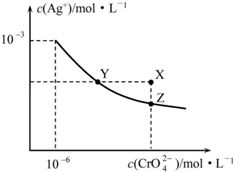

| A. | 在t℃时,Ag2CrO4的Ksp=1×10-9 | |
| B. | X点有Ag2CrO4沉淀生成 | |
| C. | 通过加热蒸发可以使溶液由Y点变到Z点 | |
| D. | 在饱和Ag2CrO4溶液中加入K2CrO4,可使溶液由Y点变到X点最终变到Z点 |
17.碳酸钠的用途很广,可用做冶金、纺织、漂染等工业的基本原料.请根据题意回答下列问题:
Ⅰ.世界最早工业生产碳酸钠的方法是路布兰(N.Leblanc)法.其流程如下:
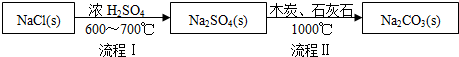
(1)流程I的另一产物是HCl,流程Ⅱ的反应分步进行:a.Na2SO4+4C $\frac{\underline{\;1000℃\;}}{\;}$ Na2S+4CO↑;
b.Na2S与石灰石发生复分解反应,总反应方程式可表示为Na2SO4+4C+CaCO3$\frac{\underline{\;1000℃\;}}{\;}$Na2CO3+CaS+4CO↑.
Ⅱ.1862年,比利时人索尔维(Ernest Solvay)用氨碱法生产碳酸钠.反应原理如下:
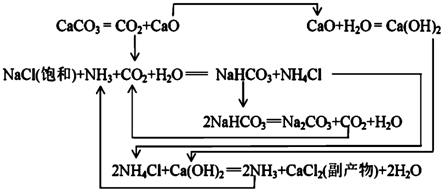
20℃时一些物质在水中的溶解度/g•(100gH2O)-1
(2)氨碱法生成纯碱的原料是食盐、石灰石、NH3,可循环利用的物质有CaO、CO2、NH4Cl、NH3.
(3)饱和NaCl溶液通NH3和CO2能生成NaHCO3的原因有:反应体系中NaHCO3溶解度最小,反应消耗水,NaHCO3相对分子质量最大.
Ⅲ.我国化工专家侯德榜研究出联合制碱法,其反应原理和氨碱法类似,但将制氨和制碱联合,提高了原料利用率.
(4)生产中需向分离出NaHCO3后所得的溶液中加入NaCl固体并通入NH3,在0~10℃(填温度范围)下析出NH4Cl.(填化学式)

Ⅰ.世界最早工业生产碳酸钠的方法是路布兰(N.Leblanc)法.其流程如下:
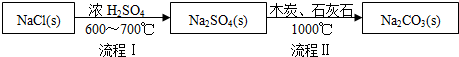
(1)流程I的另一产物是HCl,流程Ⅱ的反应分步进行:a.Na2SO4+4C $\frac{\underline{\;1000℃\;}}{\;}$ Na2S+4CO↑;
b.Na2S与石灰石发生复分解反应,总反应方程式可表示为Na2SO4+4C+CaCO3$\frac{\underline{\;1000℃\;}}{\;}$Na2CO3+CaS+4CO↑.
Ⅱ.1862年,比利时人索尔维(Ernest Solvay)用氨碱法生产碳酸钠.反应原理如下:

20℃时一些物质在水中的溶解度/g•(100gH2O)-1
| NaCl | NH4Cl | NaHCO3 | NH4HCO3 | Na2CO3 |
| 35.9 | 37.2 | 9.6 | 21.7 | 21.5 |
(3)饱和NaCl溶液通NH3和CO2能生成NaHCO3的原因有:反应体系中NaHCO3溶解度最小,反应消耗水,NaHCO3相对分子质量最大.
Ⅲ.我国化工专家侯德榜研究出联合制碱法,其反应原理和氨碱法类似,但将制氨和制碱联合,提高了原料利用率.
(4)生产中需向分离出NaHCO3后所得的溶液中加入NaCl固体并通入NH3,在0~10℃(填温度范围)下析出NH4Cl.(填化学式)

15.具有下列电子层结构的原子和离子,其对应元素一定属于同一周期的是( )
| A. | 两原子N层上都有1个s电子,一个原子有d电子,另一个原子无d电子 | |
| B. | 最外层电子排布为2s22p6的原子和最外层电子排布为2s22p6的离子 | |
| C. | 原子核外M层上的s、p轨道都充满电子,而d轨道上没有电子的两种原子 | |
| D. | 两原子的核外全部都是s电子 |
14.某元素的最外层电子数为2,价电子数为5,并且是同族中原子序数最小的元素,关于该元素的判断错误的是( )
| A. | 电子排布式为:1s22s22p63s23p63d34s2 | |
| B. | 该元素为VB | |
| C. | 元素为ⅢB族元素 | |
| D. | 该元素属于过渡元素 |
13.下列叙述中正确的是( )
| A. | pH相同的CH3COONa溶液、C6H5ONa溶液、Na2CO3溶液、NaOH溶液:c(CH3COONa)>c(C6H5ONa )>c(Na2CO3)>c(NaOH ) | |
| B. | 在常温下,10 mL 0.02 mol•L-1HCl溶液与10 mL 0.02 mol•L-1 Ba(OH)2溶液充分混合,若混合后溶液的体积为20 mL,则溶液的pH=10 | |
| C. | 将pH=3的一元弱酸HA和pH=11的NaOH溶液充分混合后一定有:c(OH-)<c(H+)<c(Na+)<c(A-) | |
| D. | 将0.2 mol•L-1的盐酸与0.1 mol•L-1的NaAlO2溶液等体积混合,其溶液中离子浓度由小到大的顺序为:c(OH-)<c(Al3+)<c(H+)<c(Na+)<c(Cl-) |
12.六种短周期元素A、B、C、D、E、F的原子序数依次增大,其中A与E同主族,B与F同主族,E与F同周期.已知常温下单质A与E的状态不同,D的核电荷数是B的最外层电子数的2倍,单质F是一种重要的半导体材料.则下列推断中正确的是( )
| A. | D、E两种元素仅可组成化学式为E2D的化合物 | |
| B. | 原子半径:E>F>C>D | |
| C. | F与D形成的化合物性质很不活泼,不与任何酸反应 | |
| D. | 元素的非金属性:D>C>F>B |
10.下列反应在一定条件下可以完成的是( )
①非金属置换金属的反应
②弱酸可以生成强酸的反应
③没有水生成,也没有沉淀和气体生成的复分解反应
④有单质参加的非氧化还原反应
⑤铜置换出氢气的反应.
0 156486 156494 156500 156504 156510 156512 156516 156522 156524 156530 156536 156540 156542 156546 156552 156554 156560 156564 156566 156570 156572 156576 156578 156580 156581 156582 156584 156585 156586 156588 156590 156594 156596 156600 156602 156606 156612 156614 156620 156624 156626 156630 156636 156642 156644 156650 156654 156656 156662 156666 156672 156680 203614
①非金属置换金属的反应
②弱酸可以生成强酸的反应
③没有水生成,也没有沉淀和气体生成的复分解反应
④有单质参加的非氧化还原反应
⑤铜置换出氢气的反应.
| A. | ①②③ | B. | ①②④ | C. | ②③④⑤ | D. | ①②③④⑤ |
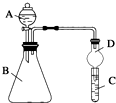 某同学为探究元素周期表中元素性质的递变规律,设计了如下系列实验.
某同学为探究元素周期表中元素性质的递变规律,设计了如下系列实验.
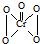 ,该反应
,该反应 ,它是由极性共价键形成的极性分子.
,它是由极性共价键形成的极性分子. ,写出该反应的化学方程式IBr+H2O=HBr+HIO.
,写出该反应的化学方程式IBr+H2O=HBr+HIO.