19.M元素的一个原子失去两个电子并转移到Y元素的两个原子中,形成离子化合物Z,下列 说法不正确的是( )
| A. | Z的熔点较高 | B. | Z可以表示为M2Y | ||
| C. | Z可能易溶于水 | D. | M形成+2价的阳离子 |
17.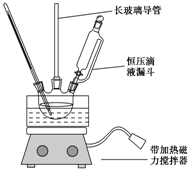 硝基苯是重要的化工原料,用途广泛.实验室用如图装置制备硝基苯,步骤如下:
硝基苯是重要的化工原料,用途广泛.实验室用如图装置制备硝基苯,步骤如下:
①取100mL烧杯,用20mL浓硫酸与18mL浓硝酸配制混和酸,加入恒压滴液漏斗中,把18mL苯加入三颈烧瓶中.
②向室温下的苯中逐滴加入混酸,边滴边搅拌,混和均匀.
③在50~60℃下发生反应,直至反应结束.
④分离出产物后,依次用蒸馏水和100mL 0.1mol/L的Na2CO3溶液洗涤,最后再用蒸馏水洗涤得到粗产品.
⑤向粗产品加入固体D除去水,然后蒸馏,得到纯净的硝基苯.
可能用到的有关数据列表如下
(1)写出该反应的化学方程式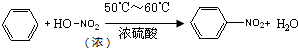 .
.
(2)配制混酸应在烧杯中先加入浓硝酸,长玻璃管作用是冷凝回流,恒压滴液漏斗的优点是使混合酸能顺利流下.
(3)反应温度控制在50~60℃的原因是防止副反应发生,反应结束后产物在下层(填“上”或者“下”),分离混酸和产品的操作名称是分液.
(4)实验前要配制100mL 0.1mol/L的Na2CO3溶液,需要用到的玻璃仪器除了玻璃棒、烧杯还有100ml容量瓶、胶头滴管.
(5)用Na2CO3溶液洗涤之后再用蒸馏水洗涤时,怎样验证液体已洗净?取最后一次洗涤液,向溶液中加入氯化钙,无沉淀生成,说明已洗净.
(6)固体D的名称为无水氯化钙.
 硝基苯是重要的化工原料,用途广泛.实验室用如图装置制备硝基苯,步骤如下:
硝基苯是重要的化工原料,用途广泛.实验室用如图装置制备硝基苯,步骤如下:①取100mL烧杯,用20mL浓硫酸与18mL浓硝酸配制混和酸,加入恒压滴液漏斗中,把18mL苯加入三颈烧瓶中.
②向室温下的苯中逐滴加入混酸,边滴边搅拌,混和均匀.
③在50~60℃下发生反应,直至反应结束.
④分离出产物后,依次用蒸馏水和100mL 0.1mol/L的Na2CO3溶液洗涤,最后再用蒸馏水洗涤得到粗产品.
⑤向粗产品加入固体D除去水,然后蒸馏,得到纯净的硝基苯.
可能用到的有关数据列表如下
| 物 质 | 熔点/℃ | 沸点/℃ | 密度(20℃)/g•cm-3 | 溶解性 |
| 苯 | 5.5 | 80 | 0.88 | 微溶于水 |
| 硝基苯 | 5.7 | 210.9 | 1.205 | 难溶于水 |
| 浓硝酸 | - | 83 | 1.4 | 易溶于水 |
| 浓硫酸 | - | 338 | 1.84 | 易溶于水 |
 .
.(2)配制混酸应在烧杯中先加入浓硝酸,长玻璃管作用是冷凝回流,恒压滴液漏斗的优点是使混合酸能顺利流下.
(3)反应温度控制在50~60℃的原因是防止副反应发生,反应结束后产物在下层(填“上”或者“下”),分离混酸和产品的操作名称是分液.
(4)实验前要配制100mL 0.1mol/L的Na2CO3溶液,需要用到的玻璃仪器除了玻璃棒、烧杯还有100ml容量瓶、胶头滴管.
(5)用Na2CO3溶液洗涤之后再用蒸馏水洗涤时,怎样验证液体已洗净?取最后一次洗涤液,向溶液中加入氯化钙,无沉淀生成,说明已洗净.
(6)固体D的名称为无水氯化钙.
14.下列各组离子中,因发生氧化还原反应而不能大量共存的是( )
| A. | Na+ OH- SO42- HCO3- | B. | OH- NH4+ SO42- Ba2+ | ||
| C. | Fe2+ H+ SO42- NO3- | D. | H+ K+ Cl- HCO3- |
13.下列溶液中不能区别SO2和CO2气体的是( )
①石灰水 ②酸性KMnO4溶液 ③溴水 ④用硝酸酸化的Ba(NO3)2溶液 ⑤品红溶液.
0 156468 156476 156482 156486 156492 156494 156498 156504 156506 156512 156518 156522 156524 156528 156534 156536 156542 156546 156548 156552 156554 156558 156560 156562 156563 156564 156566 156567 156568 156570 156572 156576 156578 156582 156584 156588 156594 156596 156602 156606 156608 156612 156618 156624 156626 156632 156636 156638 156644 156648 156654 156662 203614
①石灰水 ②酸性KMnO4溶液 ③溴水 ④用硝酸酸化的Ba(NO3)2溶液 ⑤品红溶液.
| A. | ①②③⑤ | B. | ②③④⑤ | C. | 只有① | D. | ①② |

 为了充分应用资源,用工业废碱液(Ca(OH)2、NaOH)与烟道气(回收成份SO2)来制取石膏(CaSO4•2H2O)和过二硫酸钠(Na2S2O8).设计简要流程如下:
为了充分应用资源,用工业废碱液(Ca(OH)2、NaOH)与烟道气(回收成份SO2)来制取石膏(CaSO4•2H2O)和过二硫酸钠(Na2S2O8).设计简要流程如下: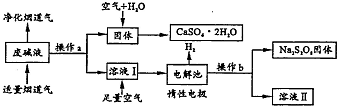
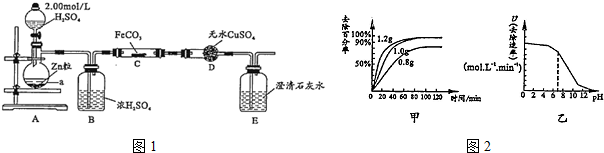
 ③
③ .
.