11.下列变化中,吸收的热量用于克服分子间作用力的是( )
| A. | 加热金属铝使之熔化 | B. | 液态SO3受热蒸发 | ||
| C. | 加热HI气体使之分解 | D. | 加热石英晶体使之熔化 |
9.环丙烷可作为全身麻醉剂,环己烷是重要的有机溶剂.下面是部分环烷烃及烷烃衍生物的结构简式、键线式和某些有机化合物的反应式(其中Pt、Ni是催化剂且催化性能相当)

回答下列问题:
(1)环烷烃与相同碳原子数的烯烃(或相对分子质量相同的烯烃)是同分异构体.
(2)从反应①~③可以看出,最容易发生开环加成反应的环烷烃是环丙烷(填名称),判断依据为在都使用催化剂的条件下,加成反应的温度最低.
(3)环烷烃还可与卤素单质、卤化氢发生类似的开环加成反应,如环丁烷与HBr在一定条件下反应,其化学方程式为 (不需注明反应条件)
(不需注明反应条件)
(4)写出鉴别环丙烷与丙烯的一种方法,试剂酸性高锰酸钾溶液;现象与结论使酸性高锰酸钾溶液退色的是丙烯,另一种是环丙烷(或溴水,使溴水退色的是丙烯).
(5)已知某烯烃在酸性高锰酸钾的作用下只产生一种有机物C3H6O,其产物物质的量是原烯烃的两倍且其氢核磁共振谱图上只有一个峰,则该烯烃的结构简式为C(CH3)2=C(CH3)2,系统名称为2,3-二甲基-2-丁烯.
| 结构简式 |  |  | Br-CH2-CH2-CH(CH3)-CH2-Br |
| 键线式 |  (环己烷) (环己烷) |  (环丁烷) (环丁烷) |  |

回答下列问题:
(1)环烷烃与相同碳原子数的烯烃(或相对分子质量相同的烯烃)是同分异构体.
(2)从反应①~③可以看出,最容易发生开环加成反应的环烷烃是环丙烷(填名称),判断依据为在都使用催化剂的条件下,加成反应的温度最低.
(3)环烷烃还可与卤素单质、卤化氢发生类似的开环加成反应,如环丁烷与HBr在一定条件下反应,其化学方程式为
 (不需注明反应条件)
(不需注明反应条件)(4)写出鉴别环丙烷与丙烯的一种方法,试剂酸性高锰酸钾溶液;现象与结论使酸性高锰酸钾溶液退色的是丙烯,另一种是环丙烷(或溴水,使溴水退色的是丙烯).
(5)已知某烯烃在酸性高锰酸钾的作用下只产生一种有机物C3H6O,其产物物质的量是原烯烃的两倍且其氢核磁共振谱图上只有一个峰,则该烯烃的结构简式为C(CH3)2=C(CH3)2,系统名称为2,3-二甲基-2-丁烯.
7.二甲醚(CH3OCH3)被称为21世纪的新型燃料,它清洁、高效,具有优良的环保性能.也可替代氟利昂作制冷剂等,对臭氧层无破坏作用.请填写下列空白:
(1)二甲醚的核磁共振氢谱图中有1个吸收峰,官能团名称是醚键.
(2)二甲醚的同分异构体A与浓硫酸混合,加热到170℃时生成有机物B:
①写出A的官能团电子式为 ;B与溴水反应生成的物质名称为1,2-二溴乙烷;
;B与溴水反应生成的物质名称为1,2-二溴乙烷;
②德国化学家第尔斯和他的学生阿尔德首次发现和记载一种新型反应而获得1950年诺贝尔化学奖,该反应是一种环加成反应:凡含有双键或三键的不饱和化合物,可以和链状或环状含共轭双烯体系发生1,4加成反应,通常生成一个六元环,该反应条件温和,产率很高,是有机化学合成反应中非常重要的碳碳键形成的手段之一,也是现代有机合成里常用的反应之一请根据以上信息写出2-甲基-1,3-丁二烯(含共轭双烯体系)与B反应化学方程式CH2=C(CH3)CH=CH2+CH2=CH2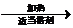
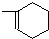 .
.
(3)二甲醚、空气、氢氧化钾溶液、多孔石墨电极构成燃料电池,则负极电极反应式是CH3OCH3+16OH--12e-=2CO32-+11H2O.
(4)反应2CH3OH(g)═CH3OCH3(g)+H2O(g)某温度下的平衡常数为225.此温度下,在密闭容器中加入CH3OH,反应到某时刻测得各组分的浓度如下:
①比较此时正、逆反应速率的大小:v(正)> v(逆)(填“>”、“<”或“=”);
②若开始只加入CH3OH,经10min后反应达到平衡,计算达到平衡时CH3OH转化率 α(CH3OH)=96.8%(计算结果用百分数表示,保留小数后一位).
(1)二甲醚的核磁共振氢谱图中有1个吸收峰,官能团名称是醚键.
(2)二甲醚的同分异构体A与浓硫酸混合,加热到170℃时生成有机物B:
①写出A的官能团电子式为
 ;B与溴水反应生成的物质名称为1,2-二溴乙烷;
;B与溴水反应生成的物质名称为1,2-二溴乙烷;②德国化学家第尔斯和他的学生阿尔德首次发现和记载一种新型反应而获得1950年诺贝尔化学奖,该反应是一种环加成反应:凡含有双键或三键的不饱和化合物,可以和链状或环状含共轭双烯体系发生1,4加成反应,通常生成一个六元环,该反应条件温和,产率很高,是有机化学合成反应中非常重要的碳碳键形成的手段之一,也是现代有机合成里常用的反应之一请根据以上信息写出2-甲基-1,3-丁二烯(含共轭双烯体系)与B反应化学方程式CH2=C(CH3)CH=CH2+CH2=CH2
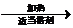
 .
.(3)二甲醚、空气、氢氧化钾溶液、多孔石墨电极构成燃料电池,则负极电极反应式是CH3OCH3+16OH--12e-=2CO32-+11H2O.
| 物质 | CH3OH | CH3OCH3 | H2O |
| 浓度(mol•L-1) | 0.44 | 0.60 | 0.60 |
①比较此时正、逆反应速率的大小:v(正)> v(逆)(填“>”、“<”或“=”);
②若开始只加入CH3OH,经10min后反应达到平衡,计算达到平衡时CH3OH转化率 α(CH3OH)=96.8%(计算结果用百分数表示,保留小数后一位).
5.某有机物的核磁共振氢谱图中有三个吸收峰,且面积之比为1:2:3,质谱图表明该有机物的相对分子质量为70,红外光谱表征到该有机物中有C=C和C=O的存在.下列说法正确的是( )
| A. | 该物质的分子式为C3H8O | |
| B. | 分子中共有6种化学环境不同的氢原子 | |
| C. | 该有机物的结构简式为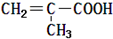 | |
| D. | 该有机物可能与新制的氢氧化铜反应 |
3.某溶液中可能含有下列6种离子中的某几种:Cl-、SO42-、CO32-、NH4+、Na+、K+.为确认溶液组成进行如下实验:(1)向200ml上述溶液中加入足量BaCl2溶液,反应后将沉淀过滤、洗涤、干燥,得沉淀4.30g,向沉淀中加入过量的盐酸,有2.33g沉淀不溶.(2)向(1)的滤液中加入足量的NaOH溶液,加热,产生能使湿润的红色石蕊试纸变蓝的气体1.12L(已换算成标准状况,假定产生的气体全部逸出).由此可以得出关于原溶液组成的正确结论是( )
0 156467 156475 156481 156485 156491 156493 156497 156503 156505 156511 156517 156521 156523 156527 156533 156535 156541 156545 156547 156551 156553 156557 156559 156561 156562 156563 156565 156566 156567 156569 156571 156575 156577 156581 156583 156587 156593 156595 156601 156605 156607 156611 156617 156623 156625 156631 156635 156637 156643 156647 156653 156661 203614
| A. | c(CO32-)=0.01mol•L-1,c(NH4+)<c(SO42-) | |
| B. | 如果上述6种离子都存在,则c(Cl-)>c(SO42-) | |
| C. | 一定存在SO42-、CO32-、NH4+,可能存在Cl-、Na+、K+ | |
| D. | 一定存在SO42-、CO32-、NH4+、Cl-,一定不存在Na+、K+ |
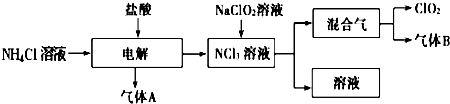
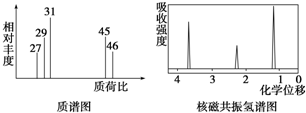
 ,B的结构简式
,B的结构简式 或
或 ;
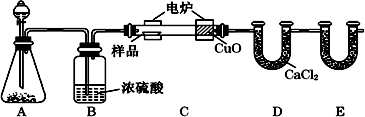
;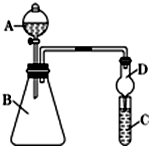 小明和同班同学为探究元素周期表中元素性质的递变规律,设计了如下系列实验.
小明和同班同学为探究元素周期表中元素性质的递变规律,设计了如下系列实验.