18.已知某有机物A的红外光谱和核磁共振氢谱如下图所示,下列说法中正确的( )
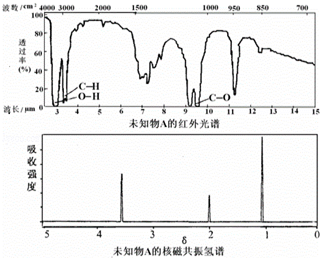

| A. | 由红光外谱可知,该有机物中有三种不同的化学键 | |
| B. | 由核磁共振氢谱可知,该有机物分子中有两种不同化学环境的氢原子 | |
| C. | 仅由核磁共振氢谱即可得知其分子中的氢原子总数 | |
| D. | 若A的化学式为C2H6O,则其结构简式为CH3-O-CH3 |
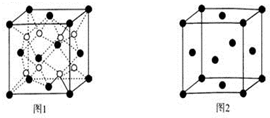
17. 某同学在研究前18号元素时发现,可以将它们排成如图所示的“蜗牛”形状,图中每个弧线上的“.”代表一种元素,其中O点代表氢元素.下列说法中错误的是( )
某同学在研究前18号元素时发现,可以将它们排成如图所示的“蜗牛”形状,图中每个弧线上的“.”代表一种元素,其中O点代表氢元素.下列说法中错误的是( )
 某同学在研究前18号元素时发现,可以将它们排成如图所示的“蜗牛”形状,图中每个弧线上的“.”代表一种元素,其中O点代表氢元素.下列说法中错误的是( )
某同学在研究前18号元素时发现,可以将它们排成如图所示的“蜗牛”形状,图中每个弧线上的“.”代表一种元素,其中O点代表氢元素.下列说法中错误的是( )| A. | 离O点越远的元素原子半径不一定越大 | |
| B. | 图中直线相连的元素处于不是同一族 | |
| C. | B元素是图中金属性最强的元素 | |
| D. | A、B两种元素组成的化合物中可能含有共价键 |
14.下列溶液中各微粒的浓度关系正确的是( )
| A. | 常温下,等pH的氨水、KOH溶液、Ba(OH)2溶液中:c(NH4+)=c(K+)=2c(Ba2+) | |
| B. | 常温时向NH4HSO4溶液中滴加NaOH溶液至pH=7:c(NH4+)+c(Na+)=c(SO42-) | |
| C. | AgCl的Ksp=1.8×10-10 mol2•L-2,在任何含AgCl固体的溶液中,c(Ag+)=c(Cl-)且Ag+与Cl-浓度的乘积等于1.8×10-10 mol2•L-2 | |
| D. | 将10 mL 0.1 mol/L Na2SO3溶液逐滴滴加到10 mL 0.1 mol/L盐酸中:c(Na+)>c(Cl-)>c(HSO3-)>c(SO32-) |
12.某化学兴趣小组为了探究铝电极在原电池中的作用,设计并进行了以下一系列实验,实验结果记录如下:
试根据表中的实验现象回答下列问题:
(1)实验1、2中Al所作的电极(正极或负极)是否相同(填“相同”或“不相同”)不相同.
(2)对实验3完成下列填空:
①石墨为正极,电极反应式:6H++6e-═3H2↑.
②电池总反应的离子方程式:2Al+6H+═2Al3++3H2↑.
(3)实验4中铝作负极 (“负极”或“正极”),铝电极的电极反应式Al-3e-+4OH-═AlO2-+2H2O,电池总反应的化学方程式为2Al+2NaOH+2H2O═2NaAlO2+3H2↑.
| 编号 | 电极材料 | 电解质溶液 | 电流计指针偏转方向 |
| 1 | Mg、Al | 稀盐酸 | 偏向Al |
| 2 | Al、Cu | 稀盐酸 | 偏向Cu |
| 3 | Al、C(石墨) | 稀盐酸 | 偏向石墨 |
| 4 | Mg、Al | 氢氧化钠溶液 | 偏向Mg |
(1)实验1、2中Al所作的电极(正极或负极)是否相同(填“相同”或“不相同”)不相同.
(2)对实验3完成下列填空:
①石墨为正极,电极反应式:6H++6e-═3H2↑.
②电池总反应的离子方程式:2Al+6H+═2Al3++3H2↑.
(3)实验4中铝作负极 (“负极”或“正极”),铝电极的电极反应式Al-3e-+4OH-═AlO2-+2H2O,电池总反应的化学方程式为2Al+2NaOH+2H2O═2NaAlO2+3H2↑.
11.ClO2是一种消毒杀菌效率高、二次污染小的水处理剂.实验室可通过以下反应制得ClO2:2KClO3+H2C2O4+H2SO4═2ClO2↑+K2SO4+2CO2↑+2H2O下列说法正确的是( )
0 156458 156466 156472 156476 156482 156484 156488 156494 156496 156502 156508 156512 156514 156518 156524 156526 156532 156536 156538 156542 156544 156548 156550 156552 156553 156554 156556 156557 156558 156560 156562 156566 156568 156572 156574 156578 156584 156586 156592 156596 156598 156602 156608 156614 156616 156622 156626 156628 156634 156638 156644 156652 203614
| A. | KClO3在反应中得到电子 | |
| B. | ClO2是氧化产物 | |
| C. | H2C2O4在反应中被氧化 | |
| D. | 1 mol KClO3参加反应,有2 mol电子转移 |
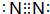 ,Z的原子结构示意图
,Z的原子结构示意图 .
.
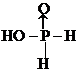 .H3PO2是一元(填“一”、“二”或“三”)酸.
.H3PO2是一元(填“一”、“二”或“三”)酸.