20.下列实验不能获得成功的是( )
①将水和溴乙烷混合加热制乙醇
②将乙醇与浓硫酸共热至140℃来制取乙烯
③用电石和水制取乙炔
④苯、浓溴水和铁粉混合,反应后可制得溴苯
⑤将乙醇和3mol•L -1的硫酸按体积比1:3混和共热至170℃制乙烯.
①将水和溴乙烷混合加热制乙醇
②将乙醇与浓硫酸共热至140℃来制取乙烯
③用电石和水制取乙炔
④苯、浓溴水和铁粉混合,反应后可制得溴苯
⑤将乙醇和3mol•L -1的硫酸按体积比1:3混和共热至170℃制乙烯.
| A. | 只有②④⑤ | B. | 只有①②④ | C. | 只有②④ | D. | 只有①②④⑤ |
19.用NA表示阿伏加德罗常数,下列说法正确的是( )
| A. | 0.2 mol H2O2完全分解转移的电子数为0.4 NA | |
| B. | 1L密度为1.84g•cm-3质量分数为98%的硫酸溶液中,所含氢原子数为36.8NA | |
| C. | 在常温常压下,2.24 L SO2与O2混合气体中所含氧原子数为0.2 NA | |
| D. | 在标准状况下,2.8 g N2和2.8 g CO所含电子数均为1.4 NA |
16.能充分说明可逆反应N2(g)+O2(g)?2NO(g)已达到平衡状态的是( )
| A. | O2的消耗速率等于NO的消耗速率 | |
| B. | 容器内始终有N2、O2和NO共存 | |
| C. | 容器内反应混合物的总物质的量不随时间改变 | |
| D. | V正(N2)=V逆(N2) |
15.下列结论错误的个数是( )
①微粒半径:r(K+)>r(S2-)
②氢化物的稳定性:HCl>H2S
③还原性:Cl->I-
④氧化性:Cl2>S
⑤酸性:H2SO4>H3PO4
⑥非金属性:O>N
⑦金属性:Mg<Ca.
①微粒半径:r(K+)>r(S2-)
②氢化物的稳定性:HCl>H2S
③还原性:Cl->I-
④氧化性:Cl2>S
⑤酸性:H2SO4>H3PO4
⑥非金属性:O>N
⑦金属性:Mg<Ca.
| A. | 1个 | B. | 2个 | C. | 3个 | D. | 4个 |
14.设NA代表阿佛加德罗常数,下列说法正确的是( )
| A. | 常温常压下,3.2g O2和3.2g O3所含氧原子数都是0.2NA | |
| B. | 常温下,0.1mol•L-1NH4NO3溶液中,含有的氮原子数是0.2NA | |
| C. | 0.1molN2与足量的H2反应,转移的电子数是0.6NA | |
| D. | 2.24LCO和CO2的混合气体中所含的碳原子数一定是NA |
13.A、B、C、D、E、F是中学化学中常见的六种短周期元素,有关位置及信息如下:A的气态氢化物能使湿润的红色石蕊试纸变蓝;C单质在实验室一般保存在煤油中;F的最高价氧化物对应的水化物既能与酸反应又能与碱反应,G单质是日常生活中用量最大的金属,易被腐蚀.请回答下列问题:
(1)G元素在周期表中的位置是第四周期第Ⅷ族.
(2)A与B可组成质量比为7:16的三原子分子,该分子与水反应的化学方程式:3NO2+H2O=2HNO3+NO;
(3)同温同压下,将a L A氢化物的气体和b L D的氢化物气体通入水中,若a=b,则所得溶液的pH<7(填“>“或“<”或“=”),若所得溶液的pH=7,则a>b(填“>“或“<”或“=”)
(4)写出F的单质与NaOH溶液反应的离子方程式:2Al+2OH-+2H2O=2AlO2-+3H2↑.
(5)已知一定量的E单质能在B2(g)中燃烧,其可能的产物及能量关系如图1所示:请写出一定条件下EB2(g)与E(s)反应生成EB(g)的热化学方程式CO2(g)+C(s)=2CO(g)△H=+172.5kJ/mol.
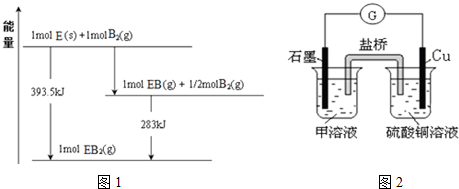
(6)若在D与G组成的某种化合物的溶液甲中,加入铜片,溶液会慢慢变为蓝色,依据产生该现象的反应原理,所设计的原电池如图2所示,其反应中正极反应式为Fe3++e-=Fe2+.
| … | E | A | B | ||
| C | … | D |
(2)A与B可组成质量比为7:16的三原子分子,该分子与水反应的化学方程式:3NO2+H2O=2HNO3+NO;
(3)同温同压下,将a L A氢化物的气体和b L D的氢化物气体通入水中,若a=b,则所得溶液的pH<7(填“>“或“<”或“=”),若所得溶液的pH=7,则a>b(填“>“或“<”或“=”)
(4)写出F的单质与NaOH溶液反应的离子方程式:2Al+2OH-+2H2O=2AlO2-+3H2↑.
(5)已知一定量的E单质能在B2(g)中燃烧,其可能的产物及能量关系如图1所示:请写出一定条件下EB2(g)与E(s)反应生成EB(g)的热化学方程式CO2(g)+C(s)=2CO(g)△H=+172.5kJ/mol.

(6)若在D与G组成的某种化合物的溶液甲中,加入铜片,溶液会慢慢变为蓝色,依据产生该现象的反应原理,所设计的原电池如图2所示,其反应中正极反应式为Fe3++e-=Fe2+.
12.下列物质既能发生消去反应,又能氧化成醛的是( )
| A. | CH3CH2CH2OH | B. | (CH3)3CCH2OH | C. | HOCH2CHBrCH3 | D. | CH3OH |
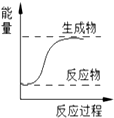
11.下列反应符合如图所示的反应是( )
0 156452 156460 156466 156470 156476 156478 156482 156488 156490 156496 156502 156506 156508 156512 156518 156520 156526 156530 156532 156536 156538 156542 156544 156546 156547 156548 156550 156551 156552 156554 156556 156560 156562 156566 156568 156572 156578 156580 156586 156590 156592 156596 156602 156608 156610 156616 156620 156622 156628 156632 156638 156646 203614

| A. | 金属钠与水的反应 | B. | 氢气燃烧 | ||
| C. | 浓硫酸的稀释 | D. | Ba(OH)2•8H2O和NH4Cl (固体)混合 |
