14. 污水治理越来越引起人们重视,可以通过膜电池除去废水中的乙酸钠和对氯苯酚(
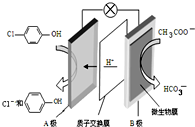
污水治理越来越引起人们重视,可以通过膜电池除去废水中的乙酸钠和对氯苯酚( ),其原理如图所示,下列说法不正确的( )
),其原理如图所示,下列说法不正确的( )
 污水治理越来越引起人们重视,可以通过膜电池除去废水中的乙酸钠和对氯苯酚(
污水治理越来越引起人们重视,可以通过膜电池除去废水中的乙酸钠和对氯苯酚( ),其原理如图所示,下列说法不正确的( )
),其原理如图所示,下列说法不正确的( )| A. | 电流方向从B极沿导线经小灯泡流向A极 | |
| B. | A为电池的正极,发生还原反应 | |
| C. | A极的电极反应式为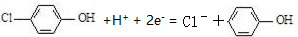 | |
| D. | 当外电路中有0.2mole-转移时,进入A极区的H+的个数为0.2NA |
13.下列反应既是离子反应,又是氧化还原反应的是( )
| A. | Zn 粒与稀硫酸反应制取氢气 | |
| B. | 二氧化碳与氢氧化钠溶液反应生成碳酸钠 | |
| C. | 氧化铁在高温下与一氧化碳反应 | |
| D. | 碳酸钠溶液与石灰乳混合 |
9.下列现象或事实可用同一原理解释的是( )
| A. | 浓硫酸和浓盐酸长期暴露在空气中浓度降低 | |
| B. | SO2和FeSO4溶液使酸性高锰酸钾的紫色褪去 | |
| C. | 漂白粉、活性炭、Na2O2都能使红墨水褪色 | |
| D. | 亚硫酸钠溶液和氯化铝溶液在空气中蒸干不能得到对应的溶质 |
8.下列判断正确的是( )
①阴离子都只有还原性
②NO2溶于水时发生氧化还原反应
③1mol Cl2参加反应转移电子数一定为2NA
④BaSO3和H2O2的反应为氧化还原反应.
①阴离子都只有还原性
②NO2溶于水时发生氧化还原反应
③1mol Cl2参加反应转移电子数一定为2NA
④BaSO3和H2O2的反应为氧化还原反应.
| A. | ②④ | B. | ②③ | C. | ③④ | D. | ①④ |
6.一定条件下反应2AB(g)?A2(g)+B2(g)达到平衡状态的标志是( )
| A. | 单位时间内生成nmolA2,同时消耗2n molAB | |
| B. | AB的消耗速率等于A2的消耗速率 | |
| C. | 容器内,3种气体AB、A2、B2共存 | |
| D. | 容器中各组分的体积分数不随时间变化 |
5.草药莪术根茎中含有一种色素,它的结构简式为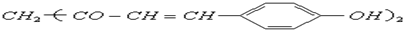 ,用它制成的试纸可以检验溶液的酸碱性.能够跟1mol该化合物起反应的Br2水溶液或H2的最大用量分别是( )
,用它制成的试纸可以检验溶液的酸碱性.能够跟1mol该化合物起反应的Br2水溶液或H2的最大用量分别是( )
0 156444 156452 156458 156462 156468 156470 156474 156480 156482 156488 156494 156498 156500 156504 156510 156512 156518 156522 156524 156528 156530 156534 156536 156538 156539 156540 156542 156543 156544 156546 156548 156552 156554 156558 156560 156564 156570 156572 156578 156582 156584 156588 156594 156600 156602 156608 156612 156614 156620 156624 156630 156638 203614
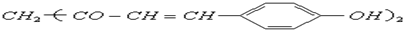 ,用它制成的试纸可以检验溶液的酸碱性.能够跟1mol该化合物起反应的Br2水溶液或H2的最大用量分别是( )
,用它制成的试纸可以检验溶液的酸碱性.能够跟1mol该化合物起反应的Br2水溶液或H2的最大用量分别是( )| A. | 3mol 3mol | B. | 3mol 5mol | C. | 6 mol 10 mol | D. | 6 mol 8 mol |