4.在通常条件下,下列各组物质的性质排列不正确的是( )
| A. | 密度:苯<水<溴苯 | B. | 沸点:戊烷>2-甲基丁烷>丙烷 | ||
| C. | 酸性:HCO3-<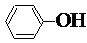 <H2CO3 <H2CO3 | D. | 与Na反应的速率:水>苯酚>乙醇 |
3.有八种物质:①乙酸、②苯、③聚乙烯、④苯酚、⑤2-丁炔、⑥甲醛、⑦邻-二甲苯、⑧环己烯,既能使酸性高锰酸钾溶液褪色又能与溴水反应使之褪色的是( )
| A. | ④⑤⑥⑧ | B. | ④⑤⑦⑧ | C. | ③④⑤⑧ | D. | ③④⑤⑦⑧ |
2.羟基扁桃酸是药物合成的重要中间体,它可由苯酚和乙醛酸反应制得,下列有关说法正确的是( )
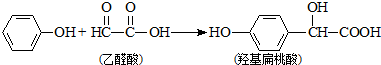
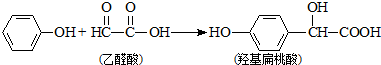
| A. | 苯酚和羟基扁桃酸互为同系物 | |
| B. | 常温下,1mol羟基扁桃酸只能与2molBr2反应发生加成反应 | |
| C. | 羟基扁桃酸分子中至少有12个原子共平面 | |
| D. | 乙醛酸的核磁共振氢谱中只有1个吸收峰 |
1.液体燃料电池相比于气体燃料电池具有体积小,无需气体存储装置等优点.一种以肼(N2H4)燃料的电池装置如图装置①该电池用空气中的氧气作为氧化剂,KOH作为电解质.下列叙述不正确的是( )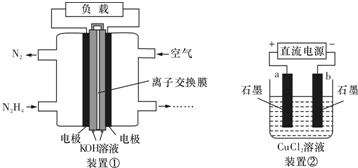

| A. | 该燃料电池负极发生的电极反应为:N2H4+4OH--4e-═N2+4H2O | |
| B. | 用该燃料电池作为装置②的直流电源,产生1molCl2至少需要通入0.5molN2H4 | |
| C. | 该燃料电池的电极材料应采用多孔导电材料,以提高电极反应物质在电极表面的吸附量,并使它们与电解质溶液充分接触 | |
| D. | 该燃料电池中,电子从右侧电极经过外电路流向左侧电极,溶液中OH-则迁移到左侧 |
20.下列叙述不正确的是( )
| A. | pH=11的NaOH溶液与pH=3的醋酸溶液等体积混合,滴入石蕊溶液呈红色 | |
| B. | 在稀溶液中,H+(aq)+OH-(aq)═H2O(l)△H=-57.3kJ•mol-1,若将含0.5molH2SO4的浓硫酸与含1mol NaOH的溶液混合,放出的热量大于57.3 kJ | |
| C. | Zn 具有还原性和导电性,可用作锌锰干电池的负极材料 | |
| D. | 由2 mol H原子形成1 mol H-H键要吸收热量 |
19.在一定温度的恒容容器中,当下列物理量不再发生变化时,表明反应A(s)+3B(g)═2C(g)+D(g)已达平衡状态的是( )
| A. | 混合气体的压强 | B. | 混合气体的总物质的量 | ||
| C. | 混合气体的平均相对分子质量 | D. | v(B)=3V(D) |
18.A、B属于短周期元素,A的阳离子与B的阴离子具有相同的电子层结构.以下关于A、B的比较中,不正确的是( )
| A. | 原子半径:A<B | B. | 原子序数:A>B | ||
| C. | 原子最外层电子数:B>A | D. | 元素所在的周期数:A>B |
17.下列离子方程式书写错误的是( )
| A. | 铝粉投入到NaOH溶液中:2Al+2H2O+2OH-═2AlO2-+3H2↑ | |
| B. | Al(OH)3溶于NaOH溶液中:Al(OH)3+OH-═AlO2-+2H2O | |
| C. | FeCl2溶液跟Cl2反应:2Fe2++Cl2═2Fe3++2Cl- | |
| D. | AlCl3溶液中加入足量的氨水:Al3++3OH-═Al(OH)3↓ |
16.下列物质间的转化能一步实现的是( )
0 156443 156451 156457 156461 156467 156469 156473 156479 156481 156487 156493 156497 156499 156503 156509 156511 156517 156521 156523 156527 156529 156533 156535 156537 156538 156539 156541 156542 156543 156545 156547 156551 156553 156557 156559 156563 156569 156571 156577 156581 156583 156587 156593 156599 156601 156607 156611 156613 156619 156623 156629 156637 203614
| A. | Na2CO3-→NaOH | B. | CaCO3-→Ca(OH)2 | C. | NaNO3-→NaCl | D. | CuO-→Cu(OH)2 |