13.如表是元素周期表的一部分,回答下列有关问题:
(1)写出下列元素符号:①N,⑥Si,⑦S.
(2)在这些元素中,最活泼的金属元素是K,最活泼的非金属元素是F,最不活泼的元素是Ar.
(3)在这些元素的最高价氧化物对应水化物中,酸性最强的是HClO4,碱性最强的是KOH,呈两性的氢氧化物是Al(OH)3;
(4)在这些元素中,原子半径最小的是K,原子半径最大的是F.
(5)在③与④中,化学性质较活泼的是Na,怎样用化学实验证明?答:钠跟水剧烈反应,放出氢气,并生成强碱;Mg跟沸水才反应,放出氢气,并生成中强碱 Mg(OH)2.
| 族 周期 | Ⅰ | Ⅱ | Ⅲ | Ⅳ | Ⅴ | Ⅵ | Ⅶ | 0 |
| 2 | ① | ② | ||||||
| 3 | ③ | ④ | ⑤ | ⑥ | ⑦ | ⑧ | ⑨ | |
| 4 | ⑩ | ⑪ | ⑫ |
(2)在这些元素中,最活泼的金属元素是K,最活泼的非金属元素是F,最不活泼的元素是Ar.
(3)在这些元素的最高价氧化物对应水化物中,酸性最强的是HClO4,碱性最强的是KOH,呈两性的氢氧化物是Al(OH)3;
(4)在这些元素中,原子半径最小的是K,原子半径最大的是F.
(5)在③与④中,化学性质较活泼的是Na,怎样用化学实验证明?答:钠跟水剧烈反应,放出氢气,并生成强碱;Mg跟沸水才反应,放出氢气,并生成中强碱 Mg(OH)2.
12.化学与科学、技术、社会、环境密切相关,下列说法正确的是( )
| A. | 研制乙醇汽油技术,能够降低机动车尾气中有害气体的排放 | |
| B. | 联合制碱法生产纯碱时,在饱和食盐水中先通入二氧化碳,再通入氨气 | |
| C. | 接触法制备硫酸的过程中,在吸收塔内是用大量的水吸收三氧化硫 | |
| D. | 工业上通过电解熔融氧化铝制备金属铝时,常常加入冰晶石作助熔剂 |
10.某的化合物化学式为:K3[Fe(C2O4)3],下列有关说法正确的是( )
| A. | 铁元素的化合价是+3 | |
| B. | 铁离子的配位数是3 | |
| C. | C2O42-中碳原子的杂化方式为sp3 | |
| D. | 该物质中含有离子键,配位键和极性共价键 |
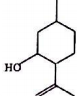
8.异胡薄荷醉(结构如图所示)是合成青蒿素的原料之一,下列说法正确的是( )
0 156442 156450 156456 156460 156466 156468 156472 156478 156480 156486 156492 156496 156498 156502 156508 156510 156516 156520 156522 156526 156528 156532 156534 156536 156537 156538 156540 156541 156542 156544 156546 156550 156552 156556 156558 156562 156568 156570 156576 156580 156582 156586 156592 156598 156600 156606 156610 156612 156618 156622 156628 156636 203614

| A. | 其分子式为C10H18O | B. | 含有1个手性碳原子 | ||
| C. | 能发生消去反应 | D. | 可与FeCl3溶液反应显示紫色 |
 已知前四周期六种元素A、B、C、D、E、F的核电荷数依次增大.B原子的p轨道半充满,其氢化物沸点是同族元素中最低的,D原子得到一个电子后3p轨道全充满,A与C能形成AC型离子化合物,其中的阴、阳离子相差一个电子层.E4+离子和氩原子的核外电子排布相同,F元素含量决定了人体内血红蛋白携氧能力的大小.请回答:
已知前四周期六种元素A、B、C、D、E、F的核电荷数依次增大.B原子的p轨道半充满,其氢化物沸点是同族元素中最低的,D原子得到一个电子后3p轨道全充满,A与C能形成AC型离子化合物,其中的阴、阳离子相差一个电子层.E4+离子和氩原子的核外电子排布相同,F元素含量决定了人体内血红蛋白携氧能力的大小.请回答: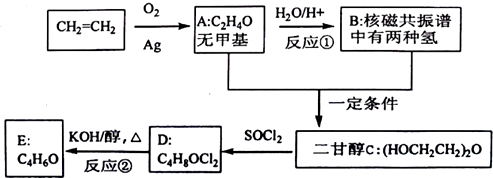
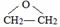 、DClCH2CH2OCH2CH2Cl.
、DClCH2CH2OCH2CH2Cl.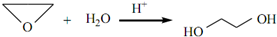 ;反应②ClCH2CH2OCH2CH2Cl+2KOH$→_{△}^{乙醇}$CH2=CH-O-CH=CH2+2KCl+2H2O.
;反应②ClCH2CH2OCH2CH2Cl+2KOH$→_{△}^{乙醇}$CH2=CH-O-CH=CH2+2KCl+2H2O.
 CH2-CHCl
CH2-CHCl .
.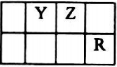 己知X、Y、Z、Q、R是原子序数依次增大的短周期元素,X和Q位于同主族,Y、Z、R在元素周期表中的相对位置如图所示,其中Q与R属于同周期.且R的单质常温下是一种黄绿色气体,X2Z2分子和R-离子具有相同的电子数,请回答:
己知X、Y、Z、Q、R是原子序数依次增大的短周期元素,X和Q位于同主族,Y、Z、R在元素周期表中的相对位置如图所示,其中Q与R属于同周期.且R的单质常温下是一种黄绿色气体,X2Z2分子和R-离子具有相同的电子数,请回答: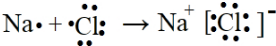 .
.